新型コロナウイルスの治療薬の中でも、世界中で開発が急がれている「飲み薬」の、開発の状況、承認や供給の見通しなどについて、最新ニュースをまとめています。
「飲み薬」の開発・承認・供給は
目次 ※ クリックすると各項目に移動 ※ タップすると各項目に移動
新型コロナ「ゾコーバ」服用で半年後の後遺症リスク半減(2/23)
2023年2月23日

新型コロナウイルスに感染したあとで続く、のどの痛みやけん怠感など後遺症とみられる症状について、塩野義製薬は治験の結果、感染したときに飲み薬の「ゾコーバ」を服用した人では、半年後に症状が出るリスクが半分ほどに下がったと発表しました。
ゾコーバは発熱などの症状が改善するまでの期間が1日早まるとされ、重症化リスクが低い人も使える、新型コロナの初めての飲み薬として、2022年11月12歳以上への投与が緊急承認されました。
塩野義製薬は日本時間の2月22日、アメリカで開かれた感染症の学会で発表した最終段階の治験の結果を発表しました。
それによりますと、治験に参加した1800人余りのうち、新型コロナに感染したあと一定程度の症状があり、ゾコーバを服用した患者で半年後にせきやのどの痛み、けん怠感、味覚障害など、14の症状のうちのいずれかを訴えたのは14.5%でした。
一方、偽の薬を服用した人で症状を訴えたのは26.3%で、会社ではゾコーバを服用した人では、後遺症とみられる症状が出るリスクが45%下がったとしています。
また、集中力や思考力の低下、物忘れや不眠などの神経症状が出るリスクも33%下がったとしています。
塩野義製薬は「1年後の時点まで追跡調査を続ける」としていて、さらに別の治験でよい結果が得られれば、後遺症の予防に使える薬としての追加の承認申請を目指すとしています。
新型コロナ「XBB.1.5」に飲み薬の効果確認 研究グループ発表(2023/2/15)
2023年2月15日

新型コロナウイルスのオミクロン株の1つで、免疫の働きを逃れやすいとされ、アメリカで主流となっている「XBB.1.5」に対して、飲み薬などの効果が確認できたとする実験の結果を、東京大学などの研究グループが発表しました。
この研究は、東京大学医科学研究所の河岡義裕特任教授らのグループが、感染症分野の国際的な雑誌「ランセット・インフェクシャス・ディジーズ」に発表しました。
研究グループは、飲み薬の「ラゲブリオ」と「パキロビッド」「ゾコーバ」、それに、点滴で投与する「レムデシビル」を使って、患者から取った「XBB.1.5」の増殖を抑えられるか実験しました。
その結果、ウイルスの増殖を抑える効果は、従来型のウイルスや2022年春ごろに広がったオミクロン株の「BA.2」に対してと、同程度みられたということです。
また、ワクチンの効果について、従来型のワクチンを4回接種した人の血液では、「XBB.1.5」に対する中和抗体の働きは、ほとんど確認できませんでしたが、5回目にオミクロン株対応のワクチンを接種した人の血液では、低い水準ながらも中和抗体の働きがみられたということです。
「XBB.1.5」に対して、オミクロン株対応のワクチンで免疫が高められるほか、抗ウイルス薬は効果があると考えられるとしていて、河岡特任教授は「患者が薬にアクセスしやすい対応が取られればいいと思う」と話しています。
新型コロナ飲み薬「ゾコーバ」処方できる医療機関拡大へ(2022/12/13)
2022年12月13日
11月、使用が承認された新型コロナウイルスの飲み薬「ゾコーバ」について、厚生労働省は12月15日から都道府県が選定した医療機関でも処方できるようにすると発表しました。
塩野義製薬が開発した新型コロナウイルスの飲み薬「ゾコーバ」は重症化リスクが低い患者でも軽症の段階から服用できるのが特徴で、11月22日に国が使用を緊急承認しました。
安全対策として当初の2週間程度は、薬が働く仕組みが同様のファイザーの飲み薬を処方した実績がある医療機関などから供給を始め、12月12日の時点でおよそ4800の医療機関などが登録されていました。
その後、大きな問題は報告されなかったことから、厚生労働省は12月15日から特に条件を設けず都道府県が選定した医療機関での処方や薬局での調剤ができるようにすると発表しました。
そのうえで、安定的に供給できるよう厚生労働省は塩野義製薬と追加で100万人分を購入する契約を結んだということとです。
処方可能な医療機関について今後、都道府県などのウェブサイトで公開するとしています。
一方、塩野義製薬によりますと、使用の承認後、12月4日までに推定で1024人が「ゾコーバ」を使用したということで、5人が頭痛や下痢などの症状を訴えたものの、重篤な副作用は報告されなかったということです。
使用した患者の年代は、20代から50代までがおよそ75%を占めたということです。
加藤厚労相「治療薬の普及に取り組む」

加藤厚生労働大臣は記者会見で「きのう製薬会社と100万人分の薬剤の追加購入の契約を行い、今後、感染拡大した場合でも、必要とする人に確実に処方することが可能となった。ゾコーバは、低リスクの患者でも高熱など強い症状があれば使用可能な薬で、新たな治療の選択肢である治療薬の普及に向けて引き続き取り組んでいく」と述べました。
新たな変異ウイルスに対する飲み薬効果確認 東大研究グループ(12/8)
2022年12月8日
新型コロナウイルスのオミクロン株のうち、国内でも検出される割合が増えてきている「BQ.1.1」などの新たな変異ウイルスに対して、飲み薬の効果が確認できたとする実験結果を東京大学の研究グループが発表しました。

この研究は東京大学医科学研究所の河岡義裕特任教授らのグループが行い、医学雑誌の「ニューイングランド・ジャーナル・オブ・メディシン」に発表しました。
研究グループは、患者からとった、免疫からより逃れやすいとされる「BQ.1.1」と別の変異ウイルス「XBB」の増殖を抑えられるか、さまざまな治療薬を使って実験しました。
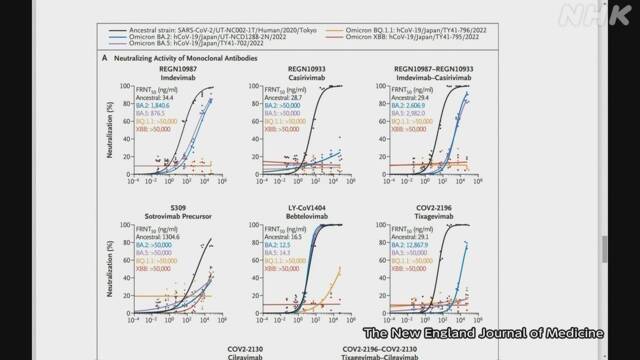
その結果、飲み薬の「ラゲブリオ」と「パキロビッド」、それに点滴で投与する抗ウイルス薬「レムデシビル」では増殖を抑える効果は、当初広がった従来型のウイルスや「BA.5」に対してと同じ程度だったことが分かりました。
一方で、人工的に作った抗体を投与する抗体医薬は、いずれも効果が著しく下がっていたとしています。
現在も感染の主流は「BA.5」ですが、「BQ.1.1」が検出される割合は東京都で11月中旬までの1週間で7%となるなど、新たな変異ウイルスが増えてきています。
河岡特任教授は「抗ウイルス薬が有効であるというのはとてもいいニュースだと思う」と話しています。
【QAで】新型コロナ 塩野義飲み薬「ゾコーバ」効果や特長は?(11/22)
2022年11月22日

新型コロナウイルスの新たな飲み薬「ゾコーバ」について、厚生労働省は使用を承認しました。
重症化リスクが低い患者も軽症の段階から服用できるのが特長の治療薬で、国内の製薬会社が開発した初めての飲み薬となります。
どんな薬なの?効果は?
QA方式でまとめました。
Q.「ゾコーバ」とは?

使用が承認されたのは塩野義製薬が開発した新型コロナウイルスの飲み薬「ゾコーバ」です。
軽症の段階から服用できる新型コロナウイルスの飲み薬で、重症化するリスクが高い患者を対象にしていたこれまでの薬と違い、重症化リスクの低い患者でも服用できるのが特長です。
これまで新型コロナの治療薬として承認されたのは飲み薬や点滴など9種類で、軽症・中等症の患者に使える薬もありましたが、糖尿病やさまざまな呼吸器疾患、肥満など重症化リスクのある人に限られていました。重症化リスクの低い人に対する治験は行われていなかった上、供給量も限られていました。
「ゾコーバ」は、いわばインフルエンザの「タミフル」のように広く使えるイメージの飲み薬で、12歳以上なら重症化リスクが低い人でも使えるということです。
11月22日に開かれた厚生労働省の専門家会議では、発熱などの症状を改善する効果が認められたことなどから「有効性が推定される」と評価し、使用を認めることを了承しました。
国内の製薬会社が開発した初めての飲み薬でもあり、医療機関などへの安定した供給につながることも期待されています。
Q.薬の効果は?
「ゾコーバ」について、塩野義製薬は2022年9月下旬、最終段階の治験で発熱などの症状が出る期間が短くなり、症状を改善する効果が確認されたと発表しました。
治験は、日本など3か国で2022年2月から7月中旬にかけて重症化リスクがない人やワクチンを接種した人を含めた、12歳から60代までの軽症から中等症のコロナ患者1821人を対象に行われたものです。

発症から3日以内に服用を開始したグループでは、オミクロン株に特徴的なせきや喉の痛み、鼻水・鼻づまり、けん怠感、発熱・熱っぽさの5つの症状すべてが7日前後でなくなり、症状が出ていた期間が約24時間短縮されたということです。
Q.どんなふうに作用する薬?
新型コロナウイルスは感染すると細胞内に侵入し、ウイルスそのもののRNAをコピーして増えていきますが、新たな薬「ゾコーバ」はコピーの準備段階で働く酵素を機能しなくすることでウイルスの増殖を抑えます。
薬が働くこうした仕組みは、すでに新型コロナウイルスの薬として承認されているアメリカの製薬大手ファイザーが開発した飲み薬「パキロビッドパック」と同様となっています。
Q.副作用は?
治験では投与は1日1回、5日間行われましたが、4日目の段階でウイルスの量が30分の1程度に減り、重篤な副作用はなかったとしています。
さらに、実験では現在、主流となっているオミクロン株の「BA.5」を含む変異ウイルスに対しても高い効果を示したとしています。
一方で、動物実験では胎児に影響があったことから、妊娠中や妊娠の可能性のある女性は服用できません。また慢性の病気の治療で薬を服用している場合などほかの薬との飲み合わせによっては副作用が出るおそれもあるので、適切に注意喚起を行うとしています。
Q.使えるのはいつから?

「ゾコーバ」について、厚生労働省は塩野義製薬と100万人分を購入する契約を締結していて、12月はじめごろには医療現場で使用できるよう、流通システムができしだい、供給を開始するとしています。
また妊娠中の女性などは使用が禁止されていることや、複数の医薬品が併用禁止になっていることから、最初の2週間程度は、安全対策として、薬が働く仕組みが同様のアメリカの製薬大手ファイザーが開発した飲み薬、「パキロビッドパック」を処方した実績のある医療機関や薬局に限定する予定です。
その後は特段の要件は設けず、各都道府県が選定した医療機関での処方や薬局での調剤ができる体制を整えたうえで、処方可能な医療機関については、都道府県などのウェブサイトで公開するとしています。
Q.「ゾコーバ」承認で必要な対策は変わる?
新型コロナの感染拡大が始まって3年近くになりますが、鍵を握る対策として早い段階から挙げられていたのが「ワクチン」、そして「治療薬」でした。
ワクチンは広く使用されるようになりましたが、大事なのは感染しても重症化しないことです。感染後、早い段階で使える薬があると重症化する人を減らすことができます。
治療薬として比較的使用しやすいとされる「飲み薬」が加わることは、コロナが排除できない中で暮らしていくためには重要なことです。
一方で、「ワクチン」と「使いやすい治療薬」の両方が使えるようになっても、感染して重症化するケースはあり得るので、引き続き場面に応じて適切にマスクを使うことや、密を避けることといった感染対策、それにワクチンの接種が重要だと専門家は指摘しています。
Q.新型コロナの治療に詳しい専門家は

新型コロナの治療に詳しい愛知医科大学の森島恒雄客員教授は「新型コロナに感染して、軽症で済むか症状が重くなるか分からないなかで、重症化リスクがない人にも投与できる薬は医療現場で望まれてきた」と話しています。
また薬の効果については、「治験ではせきや発熱などの症状の改善を1日早める効果があるという結果だったが、インフルエンザの治療薬も同じ程度で十分な効果があると考えられ、ウイルス量も減ることで重症化を防ぐことも期待できる。重症者リスクが高い人が多い介護施設や病院などで感染者が出たときに使えば、症状の悪化や感染拡大を抑えられ、職場の機能不全も防げるのではないか」
そして今後の課題としては、「この薬は発症から3日以内に服用すると効果が大きくなるとされているので、より早く診断し、より早く薬を届ける体制を国や自治体が早急に整えることが重要だ。この薬が広く使われるようになったときに予期しないような重い副作用が出ないかや、耐性を持つウイルスが出ないか監視を続けることが必要だ。また、今後は重症化や死亡のリスクが結局どの程度抑えられるのか、データが提供されることがはっきりとデータで示されることも必要だ」
Q.承認までの道のりは?

「ゾコーバ」をめぐっては、塩野義製薬が2022年2月に厚生労働省に承認を申請してから専門家会議で2度の審査が行われましたが、いずれも有効性についての判断が見送られ、今回が3度目の審議となりました。
製薬会社が開発した治療薬やワクチンなどの使用を認める「薬事承認」の手続きでは、通常、申請から承認までおよそ1年ほどかけて審査が行われ、時間を要することからワクチンの承認が海外より遅れた要因のひとつと指摘されていました。
これを受けて2022年5月、感染症の流行時などの「緊急時」で「代わりの手段がないこと」を条件に国内外で開発されたワクチンや治療薬などを迅速に承認するための「緊急承認」の制度が新たに設けられました。
「ゾコーバ」も「緊急承認」の枠組みで審査されることとなり、6月に専門家会議で最初の審議が行われましたが、有効性などについて慎重に議論を重ねる必要があるとして判断が見送られました。
1か月後の7月に開かれた2回目の会議でも「有効性が推定されるという判断はできない」などとして再び判断が見送られ、継続審議となっていました。
こうした中、医療機関がひっ迫した”第7波”を踏まえ、9月に日本感染症学会などが重症化リスクが低い患者も服用できる飲み薬が必要だとして早期の承認を求める提言を厚生労働省に提出していました。
Q.緊急承認制度の運用 専門家は
今回の審査について、薬事制度に詳しい東京大学の小野俊介准教授は「緊急承認制度のもと、有効性や安全性のどこまで示されればよいのかが委員や審査当局の間で共有されず、議論が混乱していたような印象を受けた。その結果、委員からの意見が保守的で細かくなり、ほぼ通常と同じような審査の形になっていた」と述べ、制度の運用にあたって「承認を迅速に行うこと」と「薬の有効性や安全性の確認」の両立が改めて課題になったと指摘しました。
その上で次のように指摘しました。
「国は、臨床試験で有効性が最低限、どの程度示されれば承認できるのか、具体的なラインを示すなど、制度の透明化や負担を減らすことといった改善をはからないと、絵に描いた餅のような制度になってしまうのではないか」
塩野義製薬の新型コロナ飲み薬の使用を承認 厚労省(11/22)
2022年11月22日

塩野義製薬が開発した新型コロナウイルスの飲み薬について、厚生労働省の専門家会議が使用を認めることを了承し、承認されました。
重症化リスクの低い患者も軽症の段階から服用できるのが特長で、国内の製薬会社が開発した初めての飲み薬となります。
使用が承認されたのは塩野義製薬が開発した新型コロナウイルスの飲み薬「ゾコーバ」です。
この薬は、軽症の段階から服用できる新型コロナウイルスの飲み薬で、重症化するリスクが高い患者を対象にしていたこれまでの薬と違い、重症化リスクの低い患者でも服用できるのが特長です。
2022年2月に使用の承認が申請されたあと、緊急時に、開発された薬などを迅速に承認するための「緊急承認」の制度で6月と7月に審議されましたが、有効性についての判断が見送られて継続審議となり、塩野義製薬はその後、最終段階の治験の結果を新たに、厚生労働省などに提出していました。

11月22日開かれた厚生労働省の専門家会議では、発熱などの症状を改善する効果が認められたことなどから、「有効性が推定される」評価して使用を認めることを了承し、厚生労働省が承認しました。
国内の製薬会社が開発した初めての飲み薬となります。
厚生労働省は承認後に塩野義製薬から100万人分を購入する契約を結んでいて、今後、医療機関などへの供給が始まる見通しです。
加藤厚労相「安定供給の観点からも大きな意義」
加藤厚生労働大臣は、11月22日夜、記者会見を開き「新たな治療の選択肢の1つとして、新型コロナ対策に寄与することを期待するし、国内企業が製造販売するので、安定供給の観点からも大きな意義がある。流通システムができしだい、12月の初頭には医療現場で使用できるよう供給を開始する予定で、処方が可能な医療機関は、都道府県のウェブサイトで公開することになる」と述べました。
塩野義製薬 ”新しい治療選択肢を提供”
新型コロナウイルスの飲み薬ゾコーバが「緊急承認」の制度で国から承認されたことについて、塩野義製薬は11月22日夜、コメントを発表しました。
この中では「この新しい治療選択肢をまず日本の皆様に、そしてこの薬を必要とする多くの国々に提供できるよう、引き続き取り組んでまいります」としています。
そのうえで「23日より医薬品卸への出庫を開始し、ゾコーバの処方・調剤が可能な登録医療機関・薬局からの発注を順次、受け付ける予定です。緊急承認医薬品として安全性情報の迅速かつ確実な収集と医療機関に対するタイムリーな提供に取り組みます」としています。
そして、会社では、今後、正式承認の取得を目指す考えを示しました。
新型コロナ 国内承認の治療薬 最新状況まとめました(11/22)
2022年11月22日

新型コロナの第8波が始まったのではないか?
感染者は増加し、新たな変異ウイルスも出てきています。
そんな中11月22日、重症化リスクが低い患者も軽症の段階で服用できる飲み薬として、塩野義製薬の「ゾコーバ」が承認されました。
いま国内で承認されている治療薬にはどんな薬があり、どういった効果があるのか、最新の状況をまとめました。(2022年11月22日現在)
国内で承認されている新型コロナウイルスの治療薬は、2022年11月現在9種類あります。
【軽症段階で使える飲み薬】
新型コロナに感染してから間もない段階で効果がある飲み薬があれば、重症者や死亡者を減らせるとして、世界各国で開発が進められてきました。
現在承認されている軽症の段階から使える飲み薬は、アメリカの製薬大手「メルク」が開発した「ラゲブリオ」と、アメリカの製薬大手「ファイザー」が開発した「パキロビッドパック」の2種類です。
「ラゲブリオ」

国内で初めて2021年12月24日に特例承認されたのが「ラゲブリオ」、一般名「モルヌピラビル」です。
ウイルスが細胞に侵入した後、ウイルスの設計図となる「RNA」をコピーする際に必要な酵素の働きを抑え、増殖を防ぎます。
薬の添付文書などによりますと、投与の対象となるのは、18歳以上の軽症から中等症1の患者のうち、高齢者や肥満、糖尿病などの重症化リスクがある人で、発症から5日以内に1日2回、5日間服用するとしています。
また、胎児に影響が出るおそれがあるとして、妊婦や妊娠している可能性がある女性は服用しないこととしています。
重症化リスクがある患者の入院や死亡のリスクをおよそ30%低下させる効果があるとされ、薬の服用後に有害事象が出た割合は、薬を服用したグループと偽の薬を服用したグループで変わらなかったとしています。

厚生労働省によりますと、これまでに160万人分を確保し、2022年9月15日の時点でおよそ61万9600人に投与されているということです。
2022年9月16日からは薬の生産体制が整ったとして、一般の医薬品と同様に卸会社を通じた流通が行われています。
「パキロビッドパック」
ラゲブリオに続いて2022年2月10日に特例承認されたのが、アメリカの製薬大手「ファイザー」が開発した「パキロビッドパック」です。
新型コロナ向けに開発した抗ウイルス薬の「ニルマトレルビル」と、エイズの治療に使う既存の薬で抗ウイルス薬の効果を増強させる役割を担う「リトナビル」を組み合わせた薬です。
「ラゲブリオ」と同様、細胞内に侵入したウイルスの増殖を抑えるタイプの薬ですが、作用のメカニズムが異なり、ウイルスが自身のRNAをコピーして増える準備段階で働く酵素を機能しなくすることで増殖を抑えます。
会社が2021年12月に公表した臨床研究の最終的な分析結果によりますと、重症化リスクのある患者に対して発症から3日以内に投与を始めた場合には、入院や死亡のリスクが89%低下し、発症から5日以内に投与を始めた場合でも88%低下したとしています。
また、薬の服用後に有害事象が出た割合は、薬を投与した人たちと偽の薬を投与した人たちで頻度は変わらず、ほとんどが軽かったとしています。
薬の添付文書などによりますと、投与の対象は12歳以上の重症化のリスクが高い軽症から中等症1の患者で、1日2回、5日間服用するとしています。

パキロビッドパックは、一緒に飲むことが禁じられている薬がおよそ40種類あることや、腎臓の機能が低下している患者に対しても用量の調整が必要であることなどから、使用するケースが比較的少ない状態が続いています。
厚生労働省によりますと、200万人分が確保されていますが、投与されたのは2022年10月31日の時点でおよそ5万人にとどまっています。
「ラゲブリオ」と「パキロビッドパック」いずれも、ウイルスが細胞に感染する際の足がかりとなる「スパイクたんぱく質」が変異しても影響は少なく、効果は保たれると考えられています。

新型コロナの治療に詳しい愛知医科大学の森島恒雄 客員教授は「『パキロビッドパック』は一緒に飲めない薬が多いが、お薬手帳で情報を伝えてもらったり、かかりつけの医療機関で処方したりする仕組みが整えば、もっと処方できるのではないか」と話しています。
【軽症に使える抗体医薬】
新型コロナ用に開発された「抗体医薬」で、点滴や注射で投与する薬にも、軽症者に使えるものが2種類あります。
「抗体医薬」は人工的に作った抗体を投与するタイプの薬で、抗体が新型コロナウイルスの表面にある突起の部分「スパイクたんぱく質」に結合することで、ウイルスが細胞に侵入するのを阻止します。
抗体カクテル療法「ロナプリーブ」

軽症患者向けに使える初めての薬として2021年7月に特例承認されたのが、2種類の抗体を投与する抗体カクテル療法の薬「ロナプリーブ」です。
点滴や注射で投与します。
「ソトロビマブ」

また、2021年9月には1種類の抗体を投与する「ソトロビマブ」、販売名「ゼビュディ」が特例承認されました。
点滴で投与します。
いずれも、高齢者や基礎疾患のある人など重症化するリスクがある軽症から中等症1までの患者が投与の対象で、薬の添付文書などによりますと「ロナプリーブ」は発症から7日以内に「ソトロビマブ」は発症から5日以内に1回投与します。
「ロナプリーブ」は臨床試験で、投与していない人に比べて入院や死亡のリスクがおよそ70%下げられたということです。
また、免疫力が低下し重症化するリスクがある濃厚接触者に対しては、発症予防を目的に投与することも承認されています。
厚生労働省によりますと、投与された人数は2022年10月31日の時点でおよそ4万3000人にのぼるということです。
また「ソトロビマブ」は臨床試験で、投与していない人に比べて入院や死亡のリスクがおよそ85%下げられたということです。
厚生労働省によりますと、投与された人数は2022年10月31日の時点で18万人余りにのぼるということです。
ただ、これらの抗体医薬はウイルスが変異することで「スパイクたんぱく質」の形が変わってしまうと結合しにくくなり、効果が下がってしまうという弱点があります。
特にオミクロン株に対しては、従来株と比べて効果が著しく低下したという報告が相次ぎ、厚生労働省の新型コロナの「診療の手引き」では、オミクロン株に対して「有効性が下がるおそれがあることから、ほかの治療薬が使用できない場合に使用を検討する」としています。
【発症抑制に使える薬も】
抗体医薬の中には、感染する前に投与して発症を抑える目的で使えるものがあります。
「エバシェルド」

イギリスの製薬大手「アストラゼネカ」が開発した抗体医薬「エバシェルド」は、免疫の働きが低下していてワクチンを打っても効果が出ない人たちの発症抑制に使えるとして、2022年8月に特例承認されました。
この薬は、2種類の抗体を注射で投与します。
添付文書などによりますと、ワクチンの効果が不十分と考えられる人などおよそ5200人を対象に行った治験で、感染する前に投与すると発症リスクが77%抑えられ、効果は半年間続いたとしています。
また、感染した軽症から中等症のハイリスクの患者に投与することで、重症化や死亡のリスクを50%減らす効果がみられたとしています。
この薬は安定供給が難しいことから、厚生労働省は発症予防の目的で使う場合のみ、無償で配分しています。
一方で、オミクロン株に対しては「有効性が下がるおそれがあることから、ほかの治療薬が使用できない場合に使用を検討する」としています。
【別の病気で開発の治療薬で軽症対象も】
「レムデシビル」

別の病気の治療薬として開発され、新型コロナへの効果もあるとして使われている薬もあり、その中には軽症の段階から使えるようになったものもあります。
もともとエボラ出血熱の治療薬として開発されていた点滴の抗ウイルス薬「レムデシビル」は、2020年5月、新型コロナの治療薬として初めて特例承認されました。
新型コロナの中等症1から重症の入院患者に使用されてきましたが、厚生労働省は2022年3月、重症化リスクのある軽症や中等症の患者に対しても適応を拡大しました。
【中等症以上の患者用の薬】
肺炎を起こして酸素投与が必要になった中等症2や、さらに症状が重くなった重症の患者には、体のさまざまな部位の炎症を抑える目的で免疫の過剰な働きを抑えるタイプの薬が使われます。
「デキサメタゾン」

免疫の過剰な働きを抑えるステロイド剤の「デキサメタゾン」は、2020年7月に厚生労働省が新型コロナの治療薬として推奨しました。
もともと重度の肺炎やリウマチなどの治療に使われてきた薬で、錠剤の飲み薬と点滴薬、それに注射薬があり、中等症2や重症の患者に投与されます。
「バリシチニブ」

2021年4月に承認された「バリシチニブ」も免疫の過剰な働きを抑える薬で、中等症2以上の患者に投与されます。
もともとは、関節リウマチなどの患者に使われてきた錠剤の飲み薬で、国内ではレムデシビルと併用する場合に限られています。
「アクテムラ」
日本の製薬会社「中外製薬」などが開発した、関節リウマチの薬「アクテムラ」、一般名「トシリズマブ」も2022年1月に新型コロナの治療薬として承認されました。
点滴で過剰な免疫の働きを抑える薬で、酸素投与が必要になった中等症2以上の患者に対しステロイド剤と併用して投与するとしています。
コロナ治療薬「アビガン」開発中止 重症化抑える効果得られず(10/14)
2022年10月14日

新型コロナウイルスの治療薬として承認申請が行われている「アビガン」について、富士フイルムは治験の結果、重症化を抑える効果が確認できなかったとして、コロナの治療薬としての開発を中止し、承認申請を取り下げると発表しました。
「アビガン」は、富士フイルム富山化学が開発した新型インフルエンザの治療薬で、新型コロナにも効果が見込めるとして承認申請しましたが、厚生労働省の審議会は「有効性を明確に判断するのは困難だ」として、継続審議となっていました。
会社側は、2021年4月から重症化リスクがある20歳以上の軽症のコロナ患者を対象に、新たな枠組みで治験を進めていましたが、集まった84人のデータを解析した結果、重症化を抑えるとする有意な結果は得られなかったということです。
この結果を受けて、会社側は新型コロナの治療薬としての開発を中止し、承認申請を取り下げると発表しました。
アビガンは、新型コロナの感染拡大が始まった当初、政府は、治療薬としての早期承認を目指すとしていたほか、新型コロナ用に備蓄も進めていました。
富士フイルムは「感染拡大の当初は新型コロナの治療薬の候補がなく、既存の薬を転用する形で開発が進んだが、病態の解明も進み役割を終えたと考えている。治験にご協力いただいた患者や医療従事者の皆様に感謝を申し上げます」とコメントしています。
塩野義製薬 新型コロナ飲み薬 “治験で症状改善の効果を確認”(9/28)
2022年9月28日

重症化リスクのない人も服用できるよう開発を進めている、新型コロナの飲み薬について、塩野義製薬は最終段階の治験で、発熱などの症状を改善する効果が確認されたと発表しました。この薬は承認をめぐって厚生労働省の審議会で継続審議となっていますが、会社は良好な結果が得られたとして、改めてデータを提出するとしています。
塩野義製薬は9月28日、開発を進めている新型コロナの飲み薬「ゾコーバ」について、最終段階の治験の結果を速報として発表しました。
それによりますと、治験は重症化リスクがない人やワクチンを接種した人を含めた、12歳から60代までの、軽症から中等症のコロナ患者1800人余りを対象に、ことし2月から7月中旬まで行われました。
この中で、1日1回、5日間「ゾコーバ」を服用するグループと、偽の薬を服用するグループに分けて、患者も医師もどちらが投与されているか分からない方法で比較した結果、「ゾコーバ」を服用したグループではせきや喉の痛み、鼻水・鼻づまり、けん怠感、発熱・熱っぽさの5つの症状すべてが7日前後でなくなり、およそ24時間短縮されたとしています。
また、投与を始めて4日目の段階で、ウイルスの量が大きく減少したほか、重篤な副作用はなかったとしています。
この薬について塩野義製薬は、重症化リスクのない人も服用できる初めての飲み薬として、緊急承認の制度を使って厚生労働省に承認申請しましたが、ことし7月の審議会では「有効性を推定できるデータが不十分だ」として、継続審議となっていました。
会社は治験の結果、良好な結果が得られたとして、改めて厚生労働省などにデータを提出するとしています。
“塩野義製薬のコロナ飲み薬 早期の承認を” 学会が提言(9/2)
2022年9月2日

新型コロナウイルスによる医療のひっ迫を防ぐために、重症化リスクが低い患者も服用できる飲み薬が必要だとして、日本感染症学会などは、塩野義製薬が開発した新型コロナの飲み薬の早期の承認を求める提言を厚生労働省に提出しました。
提言は9月2日、日本感染症学会と日本化学療法学会が厚生労働省に提出しました。
軽症の段階で使える新型コロナの飲み薬は、重症化リスクが高い患者用のものが承認されていますが、リスクの低い患者が使えるものはなく、提言では医療のひっ迫を改善するには高齢者などと同居している軽症の患者にも速やかに薬を投与し、感染拡大を抑えることが大切だとしています。
そのうえで、リスクの低い患者にも使うことを目指して塩野義製薬が開発した飲み薬「ゾコーバ」について、「治験では呼吸器症状の改善が示され、ウイルス量の減少も示されている」として、国は迅速に承認を検討すべきだとしています。
「ゾコーバ」は、新たに創設された緊急承認の制度を使って申請されましたが、厚生労働省の審議会では2022年7月に「有効性を推定できるデータが不十分だ」として、承認が見送られ、9月にも示される新たな治験の結果を踏まえて改めて審査が行われる見通しとなっています。
記者会見した日本化学療法学会の松本哲哉理事長は「新たなデータが出れば、一日も早く審議を開始し、早期に承認してほしい」と話していました。
新型コロナ 飲み薬「ラゲブリオ」一般流通開始へ(8/19)
2022年8月19日

政府が分配している新型コロナウイルスの飲み薬「ラゲブリオ」について、製造会社の日本法人は薬の生産体制が整ったとして、一般の医薬品と同様に卸会社を通じた流通を始めると発表しました。必要な患者に速やかに処方されることが期待されるとしています。

アメリカの製薬大手メルクが開発した新型コロナの治療薬「ラゲブリオ」は、軽症患者用の初の飲み薬として2021年12月に承認され、国内では重症化するリスクのある患者を対象に、政府が分配してこれまでに38万人以上に投与されています。
この飲み薬について会社の日本法人の「MSD」は8月18日、薬の生産体制が整い、安定供給できる見通しがたったとして、近く、一般の医薬品と同様の形での流通を始めると発表しました。
これまでは流通量が限られていたため、政府が買い上げて薬局や医療機関は「登録センター」に登録して受け取る方式でしたが、今後は卸会社を通じて医療現場などに流通するようになるということです。
これに伴って用法用量として定められた1日2回、5日間服用する際の薬価がおよそ9万4000円に定められましたが、新型コロナに関する医療は全額、公費負担で引き続き、患者の負担はないということです。
MSDは「薬局や医療機関が必要な量の薬を確保しやすくなり、患者さんにできるだけ早いタイミングで処方することができる。準備ができ次第、できるだけ速やかに一般流通を開始する」と話しています。
新型コロナ 国内で承認されている治療薬 最新状況まとめました(8/4)
2022年8月4日

新型コロナウイルスの感染拡大により自宅で療養する人が急増するなか、重症化などを防ぐ治療薬を必要とする患者も増えています。
国内では、現在、軽症の段階で投与できる薬はいずれも重症化リスクがある人が対象となっていますが、いま国内で承認されている治療薬にはどんな薬があり、どういった効果があるのか、最新の状況をまとめました。

【どんな薬があるの?】
新型コロナに感染してから間もない段階で効果がある飲み薬があれば重症者や死亡者を減らせるとして、世界各国で開発が進められてきました。
新型コロナ用として開発された薬は4種類あり、現在国内で承認されている、軽症の段階から使える飲み薬は、
▽アメリカの製薬大手「メルク」が開発した「ラゲブリオ」と、
▽アメリカの製薬大手「ファイザー」が開発した「パキロビッドパック」の2種類です。
「ラゲブリオ」(一般名「モルヌピラビル」)
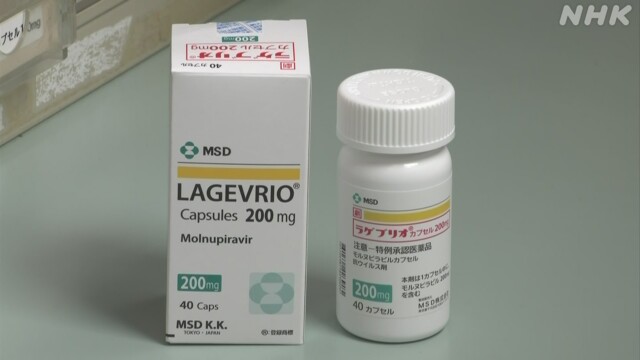
国内で初めて2021年12月24日に特例承認されたのが「ラゲブリオ」、一般名「モルヌピラビル」です。
ウイルスが細胞に侵入したあと、ウイルスの設計図となる「RNA」をコピーする際に必要な酵素の働きを抑え、増殖を防ぎます。
薬の添付文書などによりますと、投与の対象となるのは、18歳以上の軽症から中等症1の患者のうち、高齢者や肥満、糖尿病などの重症化リスクがある人で、発症から5日以内に一日2回、5日間服用するとしています。
また、胎児に影響が出るおそれがあるとして、妊婦や妊娠している可能性がある女性は服用しないこととしています。
重症化リスクがある患者の入院や死亡のリスクをおよそ30%低下させる効果があるとされ、薬の服用後に有害事象が出た割合は、薬を服用したグループと、偽の薬を服用したグループで変わらなかったとしています。
厚生労働省によりますと、これまでに160万人分を確保し、2022年7月26日の時点で、およそ27万5100人に投与されているということです。
「パキロビッドパック」
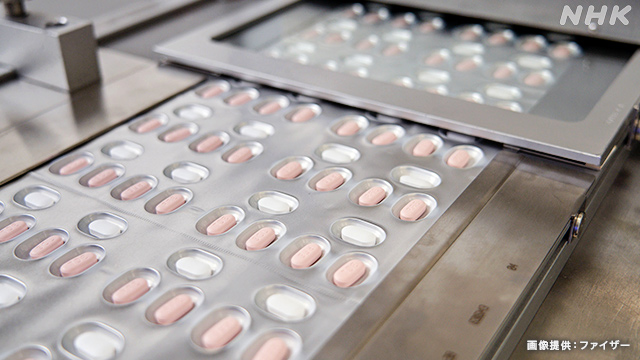
ラゲブリオに続いて、2022年2月10日に特例承認されたのが、アメリカの製薬大手「ファイザー」が開発した「パキロビッドパック」です。
新型コロナ向けに開発した抗ウイルス薬の「ニルマトレルビル」と、エイズの治療に使う既存の薬で抗ウイルス薬の効果を増強させる役割を担う「リトナビル」を組み合わせた薬です。
「ラゲブリオ」と同様、細胞内に侵入したウイルスの増殖を抑えるタイプの薬ですが、作用のメカニズムが異なり、ウイルスが自身のRNAをコピーして増える準備段階で働く酵素を機能しなくすることで増殖を抑えます。
会社が2021年12月に公表した臨床研究の最終的な分析結果によりますと、重症化リスクのある患者に対して、発症から3日以内に投与を始めた場合には入院や死亡のリスクが89%低下し、発症から5日以内に投与を始めた場合でも88%低下したとしています。
また、薬の服用後に有害事象が出た割合は、薬を投与した人たちと偽の薬を投与した人たちで頻度は変わらず、ほとんどが軽かったとしています。
薬の添付文書などによりますと、投与の対象は、12歳以上の、重症化のリスクが高い軽症から中等症1の患者で、一日2回、5日間服用するとしています。
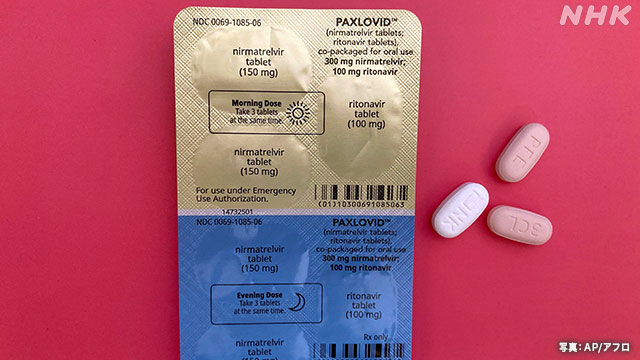
パキロビッドパックは、一緒に飲むことが禁じられている薬がおよそ40種類あることや、腎臓の機能が低下している患者に対しても用量の調整が必要であることなどから、使用するケースが比較的少ない状態が続いています。
厚生労働省によりますと、200万人分が確保されていますが、投与されたのは2022年7月26日の時点でおよそ1万7600人で、「ラゲブリオ」の15分の1以下にとどまっています。
「ラゲブリオ」と「パキロビッドパック」いずれも、ウイルスが細胞に感染する際の足がかりとなる「スパイクたんぱく質」が変異しても影響は少なく、効果は保たれると考えられています。
新型コロナの治療に詳しい愛知医科大学の森島恒雄客員教授は「経口薬は素早く服用しないと十分な効果が出ないが、今大勢の人が発熱外来に訪れていて、薬が必要とされる患者にすぐに処方するのが難しい状況になっている。『パキロビッドパック』は一緒に飲めない薬が多いが、お薬手帳で情報を伝えてもらったり、かかりつけの医療機関で処方したりする仕組みが整えば、もっと処方できるのではないか」と話しています。
【誰でも服用できる飲み薬は?】
重症者リスクがない人なども服用でき、効果が高い薬が登場すれば、感染拡大が抑えられ、インフルエンザのような対応に変えられる可能性があると考えられています。
「ゾコーバ」

日本の製薬会社「塩野義製薬」は、重症化リスクがない人でも軽症の段階で服用できる新型コロナの治療薬として、抗ウイルス薬「ゾコーバ」の承認を申請しています。
この薬は、ウイルスが細胞内に侵入したあと、RNAをコピーする準備段階で働く酵素が機能しないようにします。
「パキロビッドパック」と同様の仕組みでウイルスの増殖を抑えます。
会社は2022年4月、感染症に関する国際学会で治験の結果を示しました。
それによりますと、2022年1月から2月までに、12歳から70歳未満の軽症から中等症の新型コロナ患者428人を対象に調べたところ、薬の投与を一日1回、3回受けたあとでは、せきやのどの痛み、鼻水・鼻づまり、息切れ、熱っぽさがあることの5つの症状が偽の薬を服用したグループと比べ改善したとしています。
また、感染性のあるウイルスが検出された人の割合は、偽の薬を服用したグループと比べて90%減少し、ウイルスが陰性になるまでの時間は1日から2日、短くなったとしています。
一方で、当初の評価項目としていた下痢や吐き気などを加えた12の症状を合わせて比較すると、偽の薬を服用したグループと比べて明確な差は出なかったとしています。
また、7月14日には、実験ではオミクロン株の「BA.4」や「BA.5」に対しても「高い抗ウイルス活性を有することを確認した」と発表しました。
この薬の有効性や安全性について、6月と7月の2回、厚労省の審議会で審査が行われました。
委員からは「ウイルス量を減少させ、重症化予防の効果は推定できる」という意見が出た一方で、「胎児に影響が出るおそれがあり、妊娠の可能性のある女性や慢性疾患のある高齢者は服用できない」といった意見や「オミクロン株の症状に本当に効果があるのか」などと効果を疑問視する指摘が相次ぎました。
審議会では「有効性が推定されるという判断はできない」として、承認するかどうか判断せず、継続審議となりました。
塩野義製薬は、9月までに最終段階の臨床試験の結果を速報すると発表していて、秋頃に改めて審査が行われる見通しです。
専門家“効果はっきりすればインフルエンザのような対応も”

愛知医科大学の森島客員教授は「塩野義の薬は重症化リスクが低い人にも使えるのが利点で、症状を改善させる効果がはっきりすれば幅広く使える薬となり、薬を飲んで数日たつと職場に復帰できるインフルエンザのような対応が可能になるかもしれない。日本では感染した人が人口の1割ほどで、今後も感染の波が来ることは避けられないので、治療薬の登場が望まれる」と話しています。
【軽症者用 点滴や注射で投与する「抗体医薬」】
新型コロナ用に開発された「抗体医薬」にも軽症者用に使える薬が2種類あります。
人工的に作った抗体を投与するタイプの薬で、抗体が新型コロナウイルスの表面にある突起の部分「スパイクたんぱく質」に結合することで、ウイルスが細胞に侵入するのを阻止します。
抗体カクテル療法「ロナプリーブ」

このうち初めて、軽症患者向けに使える薬として、2021年7月に特例承認されたのが、2種類の抗体を投与する抗体カクテル療法の薬「ロナプリーブ」です。
点滴や注射で投与します。
「ソトロビマブ」

また、2021年9月には1種類の抗体を投与する「ソトロビマブ」、販売名「ゼビュディ」が特例承認されました。
点滴で投与します。
高齢者や基礎疾患のある人など、重症化するリスクがある軽症から肺炎の症状がある中等症1までの患者が投与の対象で、発症から7日以内に1回投与されます。
また、免疫力が低下し重症化するリスクがある濃厚接触者に対しても、発症予防を目的に投与することも承認されています。
「ロナプリーブ」は臨床試験で、投与していない人に比べて入院や死亡のリスクがおよそ70%下げられたということです。
厚生労働省によりますと、投与された人数は、2022年7月26日の時点でおよそ4万人に上るということです。
また、「ソトロビマブ」は臨床試験で、投与していない人に比べて入院や死亡のリスクがおよそ85%下げられたということです。
厚生労働省によりますと、投与された人数は、2022年7月26日の時点で15万人余りに上るということです。
ただ、これらの抗体医薬はウイルスが変異することで、「スパイクたんぱく質」の形が変わってしまうと結合しにくくなり、効果が下がってしまうという弱点があります。
特にオミクロン株に対しては、従来株と比べて効果が著しく低下したという報告が相次ぎ、厚生労働省の新型コロナの「診療の手引き」では、オミクロン株に対して、有効性が下がるおそれがあることから、ほかの治療薬が使用できない場合に使用を検討するとしています。
【別の病気で開発の治療薬で軽症者にも】
「レムデシビル」

別の病気の治療薬として開発され、新型コロナへの効果もあるとして使われている薬もあり、その中には軽症の段階から使えるようになったものもあります。
もともと、エボラ出血熱の治療薬として開発されていた点滴の抗ウイルス薬「レムデシビル」は、2020年5月に新型コロナの治療薬として初めて特例承認されました。
新型コロナの中等症1から重症の入院患者に使用されてきましたが、厚生労働省は2022年3月、重症化リスクのある軽症や中等症の患者に対しても適応を拡大しました。
中等症2以上の患者用の薬
肺炎を起こして酸素投与が必要になった中等症2や、さらに症状が重くなった重症の患者には、体のさまざまな部位の炎症を抑える目的で免疫の過剰な働きを抑えるタイプの薬が使われます。
「デキサメタゾン」

免疫の過剰な働きを抑えるステロイド剤の「デキサメタゾン」は、2020年7月に厚生労働省が新型コロナの治療薬として推奨しました。
もともと重度の肺炎やリウマチなどの治療に使われてきた薬で、錠剤の飲み薬と点滴薬、それに注射薬があり、中等症2や重症の患者に投与されます。
「バリシチニブ」

2021年4月に承認された「バリシチニブ」も免疫の過剰な働きを抑える薬で、中等症2以上の患者に投与されます。
もともとは、関節リウマチなどの患者に使われてきた錠剤の飲み薬で、国内ではレムデシビルと併用する場合に限られています。
「アクテムラ」

日本の製薬会社「中外製薬」などが開発した、関節リウマチの薬「アクテムラ」、一般名「トシリズマブ」も2022年1月に新型コロナの治療薬として承認されました。
点滴で過剰な免疫の働きを抑える薬で、酸素投与が必要になった中等症2以上の患者に対し、ステロイド剤と併用して投与するとしています。
“コロナ 供給可能な飲み薬などで対応に万全期す” 官房長官(7/21)
2022年7月21日
国内の製薬会社が開発した初めての新型コロナの飲み薬について、厚生労働省の審議会が、7月20日、現時点で承認の判断を行わず、継続審議とすることを決めました。これに関連して、松野官房長官は供給可能な海外の飲み薬などを活用することで、対応に万全を期す考えを示しました。
塩野義製薬が開発した新型コロナの飲み薬「ゾコーバ」について、厚生労働省の審議会は7月20日、「有効性が推定されるという判断はできない」などとして、現時点で承認の判断を行わず、継続審議とすることを決めました。
これに関連して、松野官房長官は午前の記者会見で「新規感染者数の急速な増加の継続も懸念される中、すでに2種類の飲み薬300万人分以上が医療現場に供給可能となっているほか、点滴薬が市場に流通している」と述べました。
そのうえで「こうした複数の選択肢の中から適切かつ早期に薬を投与できる体制を構築し、強化することで万全を期していく」と説明しました。
国内初のコロナ飲み薬 承認判断行わず継続審議に 厚労省審議会(7/20)
2022年7月20日

国内の製薬会社が開発した初めての新型コロナウイルスの飲み薬について、7月20日夜、厚生労働省の審議会が開かれ「有効性が推定されるという判断はできない」などとして、現時点で承認の判断を行わず、継続審議とすることを決めました。
継続審議となったのは大阪に本社がある塩野義製薬が開発した新型コロナの飲み薬「ゾコーバ」です。
ことし5月に創設された緊急承認の制度を使って申請が行われ、厚生労働省の審議会は7月20日夜、有効性や安全性について審査しました。
委員からは「ウイルス量を減少させ、重症化予防の効果は推定できる」という意見が出た一方で「胎児に影響が出るおそれがあり妊娠の可能性のある女性や慢性疾患のある高齢者は服用できない」といった意見や「オミクロン株の症状に本当に効果があるのか」などと効果を疑問視する指摘が相次ぎました。
この結果、「有効性が推定されるという判断はできない」などとして、現時点で承認するかどうか判断せず、継続審議とすることが決まりました。
新型コロナの飲み薬は海外の2つの薬がすでに使用されていますが、この薬が承認されれば国内の製薬会社が開発した薬としては初めてとなります。
会社によりますとこの薬は軽症の段階で服用でき、偽の薬を服用したグループと比較する治験を行った結果、ウイルスが検出された人の割合が90%減少したということです。
この飲み薬は2022年11月以降に示される新たな治験の結果などを踏まえて改めて審査が行われる見通しで、承認の判断は次回以降の審議会に持ち越されることになりました。
新型コロナウイルスの薬「ゾコーバ」とは
「塩野義製薬」の新型コロナウイルスの薬「ゾコーバ」は、国内の製薬会社が開発した軽症の段階で使える初めての飲み薬です。
新型コロナウイルスは感染すると細胞内に侵入し、ウイルスそのもののRNAをコピーして増えていきますが、新たな薬ではコピーの準備段階で働く酵素を機能しなくすることでウイルスの増殖を抑えます。
アメリカの製薬大手、ファイザーが開発した飲み薬「パキロビッドパック」と同様の仕組みで、塩野義製薬はことし2月、この薬の承認を厚生労働省に申請しました。
2022年4月に感染症の国際学会で発表された治験の結果によりますと、オミクロン株の感染が拡大した2022年1月から2月までに、12歳から70歳未満の軽症から中等症の新型コロナ患者428人を対象に調べたところ、薬の投与を1日1回、3回受けたあとでは、せきや喉の痛み鼻水・鼻づまり息切れ、熱っぽさがあることの5つの症状が、偽の薬を服用したグループと比べ改善したとしています。
一方で、当初の評価項目としていた下痢や吐き気などを加えた12の症状を合わせて比較すると、偽の薬グループと比べて明確な差は出なかったとしています。
感染性のあるウイルスが検出された人の割合は、偽の薬を服用したグループと比べて90%減少し、ウイルスが陰性になるまでの時間は1日から2日、短くなったということです。
塩野義製薬によりますと、安全性について重大な有害事象はなかったとしていて、最終段階の治験も並行して進めているということです。
また、7月14日には、実験ではオミクロン株の一種でより感染力が強いとされる「BA.4」や「BA.5」に対しても、「高い抗ウイルス活性を有することを確認した」としています。
【詳しく解説】新型コロナ飲み薬 なぜ多くの人がまだ飲めない?(7/8)
2022年7月8日
新型コロナウイルスの感染者が再び増加してきました。コロナ禍の前の日常に戻れる日は来るのか、戻れるとしたらいつなのか。その大きな鍵の一つが飲み薬です。ただ現状では必ずしも多くの人が飲み薬を飲むことが出来ません。なぜそうなっているのか、背景や詳しい状況、さらに今後の見通しについて、医療取材30年の中村幸司解説委員が説明します。【解説動画:9分45秒】
厚労相“塩野義製薬のコロナ飲み薬 承認前提に100万人分購入”(3/25)
2022年3月25日

大阪に本社がある「塩野義製薬」が開発する新型コロナの飲み薬について、後藤厚生労働大臣は記者会見で、薬事承認が行われることを前提に、100万人分を購入することで基本合意したと発表しました。
塩野義製薬は、新型コロナウイルスの軽症者用の飲み薬の開発を進めていて、2月、国内の製薬会社が開発する初めての飲み薬として厚生労働省に薬事承認を申請しました。
この飲み薬について、後藤厚生労働大臣は閣議のあとの記者会見で、薬事承認が行われることを前提に、速やかに100万人分を購入し、それ以降も一定数量を購入することで、3月25日、基本合意したと発表しました。
また、薬事承認については「海外で承認がされているものではないことから『特例承認』と比べ慎重な審査が必要だ。早期実用化に向けて優先かつ迅速に審査を進め、安全性や有効性が確認された場合には速やかに承認し、必要量を供給したい」と述べました。
そのうえで、後藤大臣は「このような合意を結ぶのは、国内企業が開発する経口治療薬については初めてだ。今後の承認が前提となるが、実用化されれば軽症者に対する治療の選択肢がさらに広がる。最終的な合意に向けて、流通などの詳細をさらに詰めていきたい。できるかぎりの国産治療薬の応援をしていきたい」と述べました。
新型コロナ 軽症者用飲み薬 塩野義製薬が承認申請(2/25)
2022年2月25日

大阪に本社がある「塩野義製薬」は新型コロナウイルスの飲み薬の承認を厚生労働省に申請しました。承認されれば、国内の製薬会社が開発した初めての、軽症の段階で使える新型コロナの飲み薬となります。
塩野義製薬は、新型コロナの軽症者用の飲み薬について2月25日、厚生労働省に承認を申請したと発表しました。
それによりますと、会社ではオミクロン株の感染が拡大した時期を中心に、12歳以上の軽症から中等症の新型コロナ患者428人に対し、感染確認から5日以内に、一日に1回、5日間投与した治験のデータを分析しました。
その結果、薬の投与を3回受けた後では感染性のあるウイルスが検出された人の割合が10%未満となり、偽の薬を服用したグループよりも低くなったということです。
新型コロナに感染したときに現れる疲労感や体の痛み、熱っぽさやせきなど、12の症状を合わせて偽の薬を服用したグループと比較すると投与から6日目までに有意な差は出なかったものの、鼻水や鼻づまり、喉の痛み、せき、息切れといった呼吸器の症状について、改善を確認したとしているほか、副作用も軽度だったということです。
会社では2000人程度を対象にした最終段階の治験も進めていますが、中間の段階で高い有効性が認められたため、世界に先駆けて日本国内で承認申請を行ったとしています。
軽症の段階で使える新型コロナの飲み薬は、海外の製薬会社が開発した「ラゲブリオ」と「パキロビッドパック」が国内でも承認されていますが、塩野義の飲み薬が承認されれば国内の製薬会社としては初めてで3種類目となります。
会社によりますと3月末までに100万人分、4月以降は年間で1000万人分以上を生産する予定だということです。
塩野義製薬「社会の安心安全の回復へ治療薬開発に注力」
新型コロナウイルスの飲み薬の承認を申請した塩野義製薬は、2月25日の午後、コメントを発表しました。
この中では、「一日も早く治療薬を提供できるよう、今回の臨床試験の追加解析データを速やかに審査機関に提出する。また、現在進めている軽症や中等症などの患者を対象にした臨床試験での評価を加速し、結果が得られ次第、国の審査機関に速やかに提出する」としています。
そのうえで、「新型コロナウイルス感染症が世界的な脅威として人々の生活に大きな影響を与える中、パンデミックの早期終息による社会の安心・安全の回復に貢献するために、治療薬の開発に引き続き注力して参ります」としています。
開発までの経緯
塩野義製薬が、新型コロナウイルスの飲み薬の開発に乗り出すと表明したのは、感染が拡大し始めた2020年の3月でした。
当時、別の病気を治すための薬などを転用する動きが出る中、会社では、インフルエンザなど感染症の治療薬での実績があったことなどから、新型コロナウイルス向けの治療薬を目指すことを決めました。
2021年7月には、健康な成人男性、75人を対象に安全性を確認するため初期段階の臨床試験を開始。
さらに2か月後の2021年9月には、次の段階として、軽症の患者か、無症状の人を対象に一日1回、5日間にわたって薬を投与し、有効性や安全性を確かめる臨床試験に移りました。
当初は、昨年末までに厚生労働省に治療薬の承認申請を行うことを目標にしていますが、2021年秋ごろから国内で患者数が減少し、臨床試験の対象者を確保するのが難航したことで、申請には至りませんでした。
ただ、年明け以降は感染の急拡大に伴って臨床試験への参加者が増え、申請に必要なデータを集めることができたといういうことです。
会社では、国から承認を受けたあとすぐに供給できるよう、すでに飲み薬の生産を始めていて、3月末までに100万人分の製造を目指すとしています。
塩野義製薬は、飲み薬と並行してワクチンの開発も進めていて、新型コロナの関連業務に研究員の8割を集中させるなど力を注いできました。
このほか国内の製薬会社では、大阪に本社がある「田辺三菱製薬」のカナダにある子会社が開発したワクチンが2月24日に現地で承認されるなど、欧米の製薬大手に遅れは取ったものの、治療薬やワクチンの実用化に向けた動きが進んでいます。
承認申請した飲み薬ってどんな薬?
「塩野義製薬」が承認申請した飲み薬は、新型コロナウイルス向けに新たに開発した抗ウイルス薬で、細胞内に侵入したウイルスの増殖を抑える仕組みです。
アメリカの製薬大手、ファイザーが開発した飲み薬「パキロビッドパック」と同様に、ウイルスが自身のRNAをコピーして増える準備段階で働く酵素を機能しなくすることでウイルスの増殖を抑えます。
会社が、2月7日に発表した12歳から60代までの新型コロナに感染した軽症や中等症、それに無症状の患者、69人を対象にした治験のデータでは、薬の投与を一日1回、3回受けたあとでは、感染性のあるウイルスが検出された人の割合が、薬の用量が多い場合には80%、用量が少ない場合は63%減少したとしています。
また、薬を服用したグループでは、ウイルスが陰性になるまでの時間が2日間短く、入院が必要になった人はおらず、副作用も軽度だったとしています。
2月25日に発表された軽症から中等症の428人の患者を対象にした治験の分析でも同様の結果が示されていますが、感染したときに現れる疲労感や体の痛み、熱っぽさやせきなど、12の症状を合わせてどの程度改善されたか、偽の薬を服用したグループと比較すると、投与から6日目までに有意な差は出なかったとしています。
一方で、鼻水や鼻づまり、喉の痛み、せき、息切れといった呼吸器の症状については改善を確認したとしています。
またオミクロン株に対する有効性については、実験で「高い抗ウイルス活性を確認している」としているほか、今回発表された治験の分析結果では、「オミクロン株流行後の感染者を中心に評価がなされた」としています。
新型コロナウイルスの治療に詳しい愛知医科大学の森島恒雄客員教授は、「12歳以上や重症化リスクがない人など、投与の対象が幅広いのが特徴で実用化されれば、薬を飲んで数日たつと職場に復帰できるインフルエンザのようになっていくかもしれない」と話しています。
塩野義製薬 「条件付き早期承認制度」の適用を希望
一方、今回、塩野義製薬は、新型コロナの飲み薬の承認申請に際して、「条件付き早期承認制度の適用を希望する」としています。
「条件付き早期承認制度」は、患者数が少なく、大規模な治験が難しい病気の薬を想定して作られた仕組みで、治験の途中でも一定の有効性や安全性が確認できれば申請できるようになっています。
これまでに、がんや難病などの医薬品がこの制度のもとに承認されていますが、新型コロナの治療薬で適用されれば初めてになります。
これについて森島客員教授は、「海外でのコロナの治療薬の開発でも、治験の途中の段階で効果がはっきりすれば、承認申請するということは、普通に行われてきた。ただ、症例数の少なさを補強するため、薬が広く使われた後に、副作用や効果を追跡する調査が必要になる」と指摘しています。
ファイザーの新型コロナ飲み薬を承認 国内で2種類目 厚労相(2/10)
2022年2月10日

アメリカの製薬大手、ファイザーが開発した新型コロナウイルスの飲み薬について後藤厚生労働大臣は2月10日夜、記者団に対し、正式に承認したことを明らかにしました。
国内では2種類目の新型コロナの飲み薬で、早ければ来週2月14日にも医療現場に届けられるということです。
厚生労働省の専門家部会は2月10日夕方に開いた会合で、アメリカの製薬大手ファイザーが開発した新型コロナの飲み薬「パキロビッドパック」を国内で使用することを了承しました。
このあと後藤厚生労働大臣は記者団に対し、この薬を正式に承認したことを明らかにしました。
「パキロビッドパック」はアメリカの製薬大手メルクが開発した「ラゲブリオ」に続いて、国内では2種類目の新型コロナの飲み薬となります。
政府は2022年中にこの薬を200万人分購入することでファイザーと最終合意していて、すでに国内に納入されている4万人分については早ければ来週2月14日にも医療現場に届けられるということです。
2月27日まではおよそ2000の主要な医療機関での院内処方と、これらの医療機関と連携可能な地域の薬局で試験的な取り組みを行ったうえで2月28日以降、全国の医療機関で処方できるようにするということです。
後藤大臣は「高血圧や高脂血症、不眠症などの治療に使われる薬で一緒に服用できない薬が多数あることから、審議会でも専門家から慎重な投与が必要との意見をいただいた。このため日本医師会や日本薬剤師会とも連携し段階的に医療現場への提供を進めていく」と述べました。
服用の方法 注意点
対象となるのは新型コロナウイルスに感染した人のうち12歳以上で、かつ重症化リスクのある患者です。2種類の薬を1日2回、5日間服用します。
発症後は速やかに少なくとも5日以内には服用を開始することとされています。
一方、添付文書では
▽HIV=ヒト免疫不全ウイルスに感染している人や
▽腎機能や肝機能に障害のある人
▽妊婦
▽授乳中の女性などは
服用に注意するか、服用しないよう求めています。
併用できない薬などは
厚生労働省によりますと、高血圧や高脂血症、不眠症などの治療に使われる合わせて39種類の薬や食品を使用している人はパキロビッドパックの服用が認められません。具体的には以下のとおりです。
▽関節リウマチなどの治療薬の
1. アンピロキシカム
2. ピロキシカム
▽片頭痛の治療薬の
3. エレトリプタン臭化水素酸塩
▽高血圧症などの治療薬の
4. アゼルニジピン
5. オルメサルタン メドキソミル・アゼルニジピン
▽不整脈や狭心症などの治療薬の
6. アミオダロン塩酸塩
7. ベプリジル塩酸塩水和物
8. フレカイニド酢酸塩
9. プロパフェノン塩酸塩
10. キニジン硫酸塩水和物
▽脳卒中などの治療薬の
11. リバーロキサバン
▽結核症の治療薬の
12. リファブチン
▽統合失調症の治療薬の
13. ブロナンセリン
14. ルラシドン塩酸塩
15. ピモジド
▽片頭痛などの治療薬の
16.
エルゴタミン酒石酸塩・無水カフェイン・イソプロピルアンチピリン
17. ジヒドロエルゴタミンメシル酸塩
▽子宮収縮の促進や子宮出血の予防などに使う
18. エルゴメトリンマレイン酸塩
19. メチルエルゴメトリンマレイン酸塩
▽性機能改善薬の
20. シルデナフィルクエン酸塩
21. タダラフィル
22. バルデナフィル塩酸塩水和物
▽高脂血症の治療薬の
23. ロミタピドメシル酸塩
▽白血病の治療薬の
24. ベネトクラクス
▽神経症の治療薬の
25. ジアゼパム
26. クロラゼプ酸二カリウム
▽不眠症の治療薬の
27. エスタゾラム
28. フルラゼパム塩酸塩
29. トリアゾラム
▽麻酔の前に投与する
30. ミダゾラム
▽肺高血圧症の治療薬の
31. リオシグアト
▽真菌症の治療薬の
32. ボリコナゾール
▽前立腺ガンの治療薬の
33. アパルタミド
▽てんかんの治療薬の
34. カルバマゼピン
35. フェノバルビタール
36. フェニトイン
37. ホスフェニトインナトリウム水和物
▽肺結核やそのほかの結核症の治療に使う
38. リファンピシン
39. セイヨウオトギリソウ
新型コロナ 開発進む飲み薬 効果や特徴は(2/9)
2022年2月9日
アメリカの製薬大手ファイザーが開発した新型コロナウイルスの飲み薬について、厚生労働省は2月10日、承認に向けた審議を行います。
感染から間もない段階で効果がある飲み薬があれば、重症者や死亡者を減らし、医療への負荷も減らせるため、世界各国で開発が進められてきました。
初承認はメルクの「ラゲブリオ」
このタイプの飲み薬として2021年12月24日に初めて承認されたのが、
アメリカの製薬大手メルクが開発した「ラゲブリオ」=一般名モルヌピラビルです。
ウイルスが細胞に侵入したあと、設計図となる「RNA」をコピーして増殖する際に必要な酵素の働きを抑えることで増殖を防ぎます。
薬の添付文書などによりますと、
投与の対象となるのは18歳以上の軽症から中等症の患者のうち、
▽高齢者や肥満や糖尿病など重症化リスクがある人で、
▽発症から5日以内に1日2回、5日間服用するとしています。
また、胎児に影響が出るおそれがあるとして、妊婦や妊娠している可能性がある女性は服用しないこととしています。
重症化リスクがある患者の入院や死亡のリスクをおよそ30%低下させる効果があるとされ、薬の服用後に有害事象が出た割合は、薬を服用したグループと、偽の薬を服用したグループで変わらなかったとしています。
会社側は、実験室内での分析で、オミクロン株に対しても「活性が示された」と発表しています。
この薬は、
▽2021年11月に、世界で初めてイギリスで承認され、
▽アメリカでも12月23日に緊急使用の許可が出された一方で、
▽フランスは臨床試験で当初、期待していたほどの効果がなかったとして発注をキャンセルしました。
厚生労働省は160万人分の供給を受けることで合意し、2月10日までに合計でおよそ34万人分が納入される予定ですが、安定的な供給が課題になっています。
ファイザーの飲み薬は
「ラゲブリオ」に続いて承認申請が行われたのが、アメリカの製薬大手「ファイザー」が開発した飲み薬です。
新型コロナウイルス向けに開発した抗ウイルス薬の「ニルマトレルビル」とエイズの治療に使う既存の薬で抗ウイルス薬の効果を増強させる役割の「リトナビル」を組み合わせた薬で、アメリカでは「パクスロビド」という商品名で販売されています。
日本では「パキロビッドパック」という商品名で、細胞内に侵入したウイルスの増殖を抑えるタイプの薬です。
メルクの「ラゲブリオ」とは作用のメカニズムが異なり、ウイルスが自身のRNAをコピーして増える準備段階で働く酵素を機能しなくすることで増殖を抑えます。
会社が2021年12月に公表した治験の最終的な分析結果によりますと、重症化リスクのある患者に対して
▽発症から3日以内に投与を始めた場合には入院や死亡のリスクが89%低下し、
▽発症から5日以内に投与を始めた場合でも、88%低下したとしています。
副作用について、薬の服用後に有害事象が出た割合は、薬を投与した人たちと偽の薬を投与した人たちで頻度は変わらず、ほとんどが軽かったとしています。
また、実験室での分析でオミクロン株に対しても「強い抗ウイルス活性を維持する可能性が示唆される」としています。
アメリカでは、2021年12月22日にFDA=食品医薬品局が「緊急使用許可」を出していて、
投与の対象は
▽12歳以上の軽症から中等症の患者で、
▽重症化のリスクが高い人とされ、
▽感染が確認されたらなるべく早く、症状が出た場合は5日以内に
▽1日に2回、5日間服用するとしています。
政府は、ことし中に200万人分を購入することで合意したと発表していて、承認され次第、2月中旬にも4万人分が供給されるという見通しを示しています。
塩野義製薬も開発進める
日本の製薬会社でも、大阪の「塩野義製薬」が軽症者用の飲み薬の開発を進めています。
作用の仕組みはファイザーの飲み薬と同様、ウイルスが自身のRNAをコピーして増える準備段階で働く酵素を機能しなくすることでウイルスの増殖を抑えるとしています。
会社によりますと、
12歳から60代までの新型コロナに感染した軽症や中等症、
それに無症状の患者69人について、
薬の投与を1日1回、
3回受けたあとでは、
感染性のあるウイルスがある人の割合が
▽薬の用量が多い場合には80%、
▽用量が少ない場合は63%減少したとしています。
また、入院が必要になった人はおらず、副作用も軽度だったとしています。
会社は2月7日、東京都内で記者会見を開き、400人の患者の分析結果が、近く、新たにまとまる見通しだとして、高い有効性が認められれば、最終結果を待たず、最短で2月中旬の週にも国に承認申請する考えを示しました。
承認申請されれば、国内の製薬会社の新型コロナの飲み薬としては初めてとなります。
一方、会社では、2022年3月末までに100万人分の生産を完了させ、4月以降は年間で1000万人分以上を生産する予定だとしています。
専門家「新薬の登場 非常に意義ある」

ファイザーが開発した飲み薬について、新型コロナウイルスの治療に詳しい愛知医科大学の森島恒雄客員教授は「先に承認されている飲み薬、ラゲブリオの供給が限られる中、新たな薬が登場することは非常に意義がある。また、オミクロン株に対しても試験管内で効果が確認されていて、作用の仕組みを考えても、ワクチンや一部の抗体医薬のように効果が落ちることはなく、有効だと考えられる」と話しています。
そのうえで「こうした飲み薬が幅広く使われるためには、診療所などでできるだけ早く検査・診断し、処方する仕組みがなにより重要だが、感染が急拡大する中、多くの人がなかなか診断を受けられていない。今の検査体制を一層拡大することが必要だ」と話しています。
またファイザーの飲み薬は、2種類の薬を組み合わせて飲むことになっていますが、このうち、抗ウイルス薬の効果を増強させる作用がある「リトナビル」について森島客員教授は、「薬の血中濃度を上げる仕組みがあり、基礎疾患があって別の薬を飲んでいる人は要注意だ。処方してもらう場合には、医師にお薬手帳を見せるなどして、確認することが重要だ」と指摘しました。
一方、国内の製薬会社で、塩野義製薬が開発している飲み薬について「12歳以上や重症化リスクがない人など、投与の対象が幅広いのが特徴で実用化されれば、薬を飲んで数日たつと職場に復帰できるインフルエンザのようになっていくかもしれない」と述べました。
会社が最終段階の治験の結果を待たず、承認申請する可能性を明らかにしたことについては、「海外でのコロナの治療薬の開発でも、治験の途中の段階で効果がはっきりすれば、承認申請するということは、普通に行われてきた。ただ、症例数の少なさを補強するため、薬が広く使われた後に副作用や効果を追跡する調査が必要になる」と指摘しました。
ファイザー コロナ飲み薬 2月10日承認見込み 使用条件を慎重審議(2/9)
2022年2月9日

アメリカの製薬大手ファイザーが開発した新型コロナウイルスの飲み薬について、厚生労働省は2月10日、専門家による部会を開いて承認に向けた審議を行います。
部会では承認が了承される見込みですが、この薬は飲み合わせに注意が必要な薬が複数あり、使用の条件を慎重に審議することにしています。
ファイザーの申請を受けて2月10日承認に向けた審議が行われるのは新型コロナウイルスの軽症から中等症の患者を対象にした「パキロビッドパック」(一般名「ニルマトレルビル/リトナビル」)という飲み薬です。
2021年12月にファイザーが公表した臨床試験の分析では、重症化リスクのある患者に対して発症から3日以内に投与を始めた場合、入院や死亡のリスクが89%低下したとされています。
また、オミクロン株に対する効果についても、実験室で確認したところ増殖を抑える効果がみられたとしています。
日本政府は、ファイザーから200万人分の供給を受けることで2月10日の厚生労働省の専門家部会では承認が了承される見込みです。
承認されれば、新型コロナの飲み薬としてはアメリカの製薬大手メルクの「ラゲブリオ」(一般名「モルヌピラビル」)に続いて2種類目となります。
ただ、この薬は一部の薬と一緒に使うと必要以上に強い効果が出て、健康に悪影響を及ぼすおそれがあり、飲み合わせに注意が必要で、厚生労働省は使用の条件を慎重に審議することにしています。
併用禁忌の薬が複数
ファイザーの飲み薬「パキロビッドパック」(一般名「ニルマトレルビル/リトナビル」)は、新型コロナウイルスの増殖を抑制する薬と、エイズの治療で使われる薬を同時に服用します。
このうち、エイズの治療で使われる薬は、一緒に服用する薬の効果を高める作用がありますが、種類によっては必要以上に強い効果が出てしまい、健康や生活に悪影響を及ぼすおそれがあるとされています。
日本では高血圧や不整脈、うつ病の薬など32種類との併用を認めていません。
この中には、片頭痛の薬や解熱鎮痛剤など薬局などで一般に購入できるものもあります。
アメリカFDA=食品医薬品局は2021年12月、「パキロビッドパック」アメリカでの販売名「パクスロビド」の緊急使用許可を出していますが、ファイザーは28種類の薬と併用しないよう求めています。
承認に向けた審議にあたって厚生労働省は、外国人と日本人では薬に対する反応が異なることも踏まえ、どの薬を併用できないとするか専門家とともに検討することにしています。
薬局 服薬状況をより丁寧に確認を

新型コロナウイルスの新たな飲み薬は、飲み合わせに注意が必要だと指摘されていることから、薬局では、患者がふだん使用している薬の状況を、より丁寧に確認する必要があるとしています。
東京 中央区の薬局では、新型コロナの飲み薬を扱っていて、医療機関から処方箋を受け取って、薬剤師が患者に電話やオンラインで服用方法などを指導したあと自宅に直接、届けています。
新たな飲み薬は、一部の薬と併用すると健康に悪影響を及ぼすおそれがあることから、承認されて扱うことになった場合は、より注意が必要になると考えています。
患者がふだん使用している薬は通常は、薬局を訪れた際のアンケートで把握できますが、新型コロナの患者は対面で会えない中で薬を渡すケースがほとんどです。
また、睡眠をうながす薬や血圧を下げる薬など、比較的よく処方される薬も飲み合わせに注意が必要だとされる可能性があります。
こうしたことから服薬の状況をより丁寧に確認しなくてはならないといいます。
これまで新型コロナの飲み薬を提供した人の中には、自宅療養中に一時、症状が悪化した人もいたということで、新たな薬についても慎重なフォローアップが欠かせないとしています。

越前堀薬局の薬剤師の犬伏洋夫さんは、「お薬手帳を持たない患者に聞いて自分が使っている薬の名前を言える人は1割もいないかと思います。実際に会えないことを考えると、より丁寧に電話で確認しなければならないし、薬の飲み合わせは、実は危ないという注意喚起をきちんとしなければいけない」と話しています。
専門家「影響あるか正確な情報 患者側に伝える必要」

この薬に詳しい国立国際医療研究センターエイズ治療・研究開発センターの岡慎一センター長は、「患者がふだん飲んでいる薬と一緒に使うと影響があるかどうかというのは、医療側がきっちり調べて、正確な情報を患者側に伝える必要がある。効果が高い薬とみられるので、まずはコロナの治療を優先して、その期間だけ服用を中断したり、ほかの薬に替えられたりできないか、患者からも医師や薬剤師に忘れずに相談してほしい」と話しています。
塩野義製薬 新型コロナの飲み薬 来週にも国に承認申請か(2/7)
2022年2月7日

大阪に本社がある「塩野義製薬」は、開発中の新型コロナウイルスの飲み薬について、これまでの治験で高い有効性が見られているなどとして、来週にも国に承認申請する可能性があると明らかにしました。承認申請すれば、国内の製薬会社の新型コロナの飲み薬としては初めてとなります。
これは塩野義製薬が2月7日、東京都内で開いた記者会見で明らかにしました。
塩野義製薬は、新型コロナに感染した軽症や中等症、それに無症状の患者向けの飲み薬の治験を行っています。

治験では12歳から60代の患者69人を対象に、1日1回、5日間薬を服用するグループと偽の薬を服用するグループで比較していて、薬の投与を3回受けたあとでは、感染性のあるウイルスがある人の割合が、薬の用量が多い場合には80%、用量が少ない場合は63%減少したということです。
また、薬を服用したグループではウイルスが陰性になるまでの時間が2日間短く、入院が必要になった人はいなかったということです。
さらに副作用も軽度だったということで、会社では現在進めているおよそ400人が対象の治験のデータを分析し、高い有効性が認められれば、最終段階の治験の結果を待たずに、来週から再来週にも国に承認申請する可能性があるとしています。
承認申請すれば、国内の製薬会社の新型コロナの飲み薬としては初めてとなります。
手代木功社長は「非常によい手応えを感じている。今回のデータを次の段階で再現できれば、非常にいい薬剤になる可能性が高い」と話しています。
ファイザーのコロナ飲み薬“200万人分購入で最終合意” 厚労相(2/1)
2022年2月1日

アメリカの製薬大手、ファイザーが開発した新型コロナウイルスの飲み薬について、後藤厚生労働大臣は、2022年中に200万人分を購入することで最終合意したと発表し、2月中旬にも薬事承認されしだい、4万人分が供給されるという見通しを示しました。
ファイザーが開発した新型コロナウイルスの重症化を防ぐための飲み薬「パクスロビド」について、政府は、2021年12月、200万人分を確保することで基本合意し、ファイザーは1月、厚生労働省に薬事承認を申請しました。
この飲み薬について、後藤厚生労働大臣は記者会見で1月31日、2022年中に200万人分を購入することで最終合意したと発表しました。
そのうえで「薬事承認が行われれば、速やかに4万人分が納入される見込みだ。今月中旬にはなんとか承認を下ろすような形で作業を進めていきたい」と述べ、2月中旬にも薬事承認がされしだい、4万人分が供給されるという見通しを示しました。
後藤大臣は「この治療薬はオミクロン株に効果があることが示唆されており、これにより重症化リスクがある軽症者に対する治療の選択肢が広がるものと考えている。引き続き、治療薬を必要な方に確実に届けられるように取り組んでいきたい」と述べました。
ファイザー 新型コロナ飲み薬の承認を厚労省に申請(1/14)
2022年1月14日
アメリカの製薬大手ファイザーは、新型コロナウイルスの飲み薬の承認を厚生労働省に申請しました。承認されれば飲み薬としては国内で2種類目です。
承認申請が行われたのは、ファイザーが開発した新型コロナウイルスの重症化を防ぐための飲み薬「パクスロビド」です。
ファイザーは、日本国内での使用に向けて1月14日、厚生労働省に承認を申請しました。
2021年12月、ファイザーが公表した臨床試験の最終的な分析では、重症化リスクのある患者に発症から3日以内に投与を始めた場合、入院や死亡のリスクが89%低下したとされています。
また、オミクロン株に対する効果についても、実験室で確認したところ増殖を抑える効果がみられたとしています。
日本政府はファイザーから200万人分の供給を受けることで基本合意していて、今後、有効性や安全性を審査したうえで2月中の早い時期の実用化を目指すとしています。
承認されれば、新型コロナウイルスの飲み薬では2021年12月下旬に承認されたアメリカの製薬大手メルクの「ラゲブリオ」=一般名「モルヌピラビル」に続いて2種類目です。
パクスロビドは、2021年12月、EMA=ヨーロッパ医薬品庁が正式な承認はしていないものの、緊急時などに重症化リスクの高い成人に使用できるとする見解を発表したほか、アメリカFDA=食品医薬品局が正式な承認の前に薬を使用できるようにする「緊急使用の許可」を出しています。
飲み薬「パクスロビド」とは
「ファイザー」が厚生労働省に承認申請した新型コロナウイルスの飲み薬「パクスロビド」は、新型コロナウイルス向けに開発した抗ウイルス薬と既存の抗エイズウイルス薬を組み合わせたものです。
先に承認されたアメリカの製薬大手メルクの「ラゲブリオ」=一般名、モルヌピラビルと同様、細胞内に侵入したウイルスの増殖を抑えるタイプの薬ですが、作用のメカニズムが異なり、ウイルスが自身のRNAをコピーして増える準備段階で働く酵素を機能しなくすることで増殖を抑えます。
アメリカでは、2021年12月22日にFDA=食品医薬品局が「緊急使用許可」を出していて、投与の対象となるのは、軽症から中等症の患者で、12歳以上の重症化のリスクが高い人とされ、感染が確認されたらなるべく早く、症状が出た場合は5日以内に、1日に2回、5日間、服用するとしています。
会社が12月14日に公表した治験の最終的な分析結果によりますと、重症化リスクのある患者に対して発症から3日以内に投与を始めた場合には入院や死亡のリスクが89%低下し、発症から5日以内に投与を始めた場合でも、88%低下したとしています。
副作用について、薬の服用後に有害事象が出た割合は、薬を服用した人たちと偽の薬を服用した人たちで頻度は変わらず、ほとんどが軽かったとしています。
また、実験室での分析の結果、オミクロン株に対しても「強い抗ウイルス活性を維持する可能性が示唆される」としています。
新型コロナウイルスの治療に詳しい愛知医科大学の森島恒雄客員教授は「治療の選択肢を増やせる点で意義は大きい。今後、薬に耐性があるウイルスが出る可能性もあり、作用のメカニズムが異なる複数の薬が実用化されることは重要だ」と話しています。
コロナ飲み薬 薬局で提供始まる 感染急拡大で自宅療養者増え(1/13)
2022年1月13日

新型コロナウイルスの感染の急拡大によって自宅療養者が増えていることから、街の薬局ではクリニックの処方を受け、飲み薬を自宅に届けるなどして提供を始めています。
アメリカの製薬大手メルクが開発した新型コロナウイルスの飲み薬は、2021年の年末に国内での使用が承認され、1月9日時点で全国のおよそ8000の医療機関と薬局におよそ2万4000人分が配送されています。
感染の急拡大によって自宅療養者が増えていることから、クリニックでの処方も始まっていて、神奈川県綾瀬市の薬局では1月6日以降、3人の患者に提供しました。
患者は自宅やホテルで療養していた20代から80代の男女で、薬剤師が電話で本人や家族に服薬指導を行ったうえで、直接自宅に出向いて薬を届けたということです。
その直後に別の患者の依頼が来ましたが、当初3箱しか注文できず薬が足りなくなったため、他の薬局を紹介して対応してもらったこともあったということです。
注文数限られる 薬剤師「在庫が心配」
飲み薬は足りなくなると専用のサイトを通じて追加で注文できる仕組みになっていますが、一度に注文できるのは数箱程度に限られているということです。
管理薬剤師の植田綾さんは「飲み薬は発注数が限られているので、患者が増えてくると在庫が心配です。薬を提供した人でも入院したと聞いたので、1人暮らしの人などはフォローアップも重要です。飲み薬に対応する薬局もまだ少なく、広域の患者をどうフォローできるのかが不安です」と話していました。
コロナ飲み薬の配布状況などは
アメリカの製薬大手メルクが開発した新型コロナウイルスの飲み薬「ラゲブリオ」=一般名、モルヌピラビルは、2021年12月24日に国内での使用が承認されました。
厚生労働省は、メルク側と合わせて160万人分の供給を受けることで合意していて、1月9日の時点で全国の医療機関や薬局およそ8000か所に対し、合わせておよそ2万3700人分を配布したとしています。
また、発症から5日以内に服用することが推奨されているため、厚生労働省は、薬局などから患者の自宅に速やかに配送する仕組みの整備を進めています。
このため、薬局などには夜間や休日も配送の依頼に対応するよう求めていて、難しい場合はほかの薬局などと輪番制で対応することも認めています。
後藤厚労相 自宅療養者の健康観察 飲み薬の供給体制など整う(1/12)
2022年1月12日

オミクロン株の感染拡大に備え、都道府県が実施した医療提供体制の点検結果がまとまり、後藤厚生労働大臣は、自宅療養中の患者の健康観察や、飲み薬の速やかな供給などを行える体制が全国で整ったことを明らかにしました。
オミクロン株の感染拡大に備え、政府は2021年12月、すべての都道府県に対し、自宅療養中の患者の健康観察や、飲み薬の速やかな供給などを行うための医療提供体制を自己点検したうえで、報告するよう求めました。
これについて、後藤厚生労働大臣は、記者団に対し、点検結果がまとまり、検査で感染が確認された患者には、翌日までに連絡を取り、健康観察を始めるほか、医師による診断の翌日までに飲み薬の投与が可能な体制が全国で整ったことを明らかにしました。
また、自宅療養を始めた場合には、翌日までにパルスオキシメーターを配布する体制も整い、自宅療養中の患者への健康観察などを行う医療機関の数は、2021年11月末時点から4000増えて、およそ1万6000確保できたということです。
後藤大臣は「厚生労働省としても看護師の不足に対応するなど、バックアップできることは、しっかりバックアップしていきたい」と述べました。
初の新型コロナ飲み薬 全国の医療機関や薬局に配送始まる(12/27)
2021年12月27日

先週、承認された、新型コロナウイルスの重症化を防ぐ初めての飲み薬が、12月27日から全国の医療機関や薬局に配送されています。
アメリカの製薬大手メルクが開発した「モルヌピラビル」は、新型コロナウイルスの重症化を防ぐ初めての飲み薬で、12月24日に国内での使用が承認されました。

厚生労働省は12月27日から全国の医療機関や薬局に順次、配送していて、このうち東京 西東京市の薬局には、12月27日正午ごろに薬3箱が届きました。
この飲み薬は、発症から5日以内の軽症から中等症の患者のうち、18歳以上で重症化リスクがある人が対象で、1回4錠を1日2回、5日間服用します。
1箱に40錠入っていて1箱で1人分にあたるということです。
自宅や療養施設で薬を受け取ることも可能で、医療機関が患者の最寄りの薬局にファックスなどで処方箋を送り、薬局の薬剤師が電話やオンラインで患者に服用方法などを指導したあと、届けることになっています。
「エコ薬局」の宮川昌和薬局長は「地域の方々が安心できる薬が一つ増えたと思います。承認されたばかりの薬なので、事前に予想されている副作用以外の症状が出ることも考えられます。飲む前よりも状態が悪化したり、吐き気や発疹などがあったりした場合は、医療機関と連携して迅速に対応したい」と話していました。
「モルヌピラビル」 新型コロナの飲み薬として正式に承認(12/24)
2021年12月24日

アメリカの製薬大手メルクが開発した新型コロナウイルスの飲み薬を、厚生労働省が12月24日夜承認しました。重症化を防ぐ初めての飲み薬で、来週から患者が服用できるよう全国の医療機関などに配送することにしています。
メルクが開発した新型コロナの飲み薬「モルヌピラビル」について、厚生労働省は12月24日、国内での使用を承認しました。
対象は、発症から5日以内の軽症から中等症の患者のうち、18歳以上で、重症化リスクがある人で、1日2回、5日間服用するとしています。
胎児に影響が出るおそれがあるとして、妊娠中の女性は服用しないこととしています。
新型コロナウイルス患者の重症化を防ぐ飲み薬は初めてで、自宅で服用できるうえ、病院での管理もしやすいことから患者や医療機関の負担の軽減につながるとされています。
メルクが行った臨床試験では、入院や死亡のリスクをおよそ30%低下させる効果が確認されたとしています。
承認に先立って開かれた専門家部会では、新たな変異ウイルス「オミクロン株」に対する効果について、厚生労働省は「会社側は、ほかの変異ウイルスへの効果と同じ程度と説明している」としましたが、一部の委員からは、臨床試験で効果が確認されていないとして、疑問視する声があったということです。
また、委員からは、有効性や安全性に関するデータが限られているという指摘もあり、医療機関には、患者が服用したあとの容体を一定期間確認するよう求めるとしています。
厚生労働省は、メルク側と年内に20万人分、合わせて160万人分の供給を受けることで合意していて、契約金額はおよそ1370億円だということです。
厚生労働省は、来週から患者が服用できるよう都道府県が指定した全国の医療機関や薬局などに配送することにしています。
医療機関などには国から無料で提供するため、患者の自己負担はないということです。
厚労省 薬は自宅で受け取るようにする方針
重症化を防ぐ飲み薬「モルヌピラビル」は、症状が出てから5日以内に服用することが推奨されています。
厚生労働省は、陽性となった人と周囲との接触をできるだけ避けるため、患者が薬局に出向くのではなく、自宅で受け取るようにする方針です。
医療機関が患者の最寄りの薬局にファックスなどで処方箋を送り、薬局の薬剤師が電話やオンラインで患者に服用方法などを指導したあと運送業者を通じて薬が配送される仕組みです。
厚生労働省は、都道府県を通じて対応できる薬局をすでにリスト化しています。
日本薬剤師会の田尻泰典副会長は、「いかに効率よく必要な人に、必要なタイミングで届けられるかが、私たちの命題だ。夏の第5波のときにも自宅療養者への対応を行ってきたので、処方箋が出てから患者に薬が届くまでに丸一日以上かかることはないと思う。夜中に薬が必要になっても届けられるように、リスト化された薬局には24時間対応をお願いしている」と話しています。
メルク開発の新型コロナ飲み薬 米FDAが「緊急使用の許可」(12/24)
2021年12月24日

製薬大手メルクが開発し、日本でも厚生労働省が承認に向けた手続きを進めている新型コロナウイルスの重症化を抑える飲み薬について、アメリカFDA=食品医薬品局は12月23日、「緊急使用の許可」を出しました。
FDAは12月23日、メルクの抗ウイルス薬「モルヌピラビル」について、新型コロナウイルスの感染症の重症化を防ぐ効果があるとして、正式な承認の前に使用を可能にする「緊急使用の許可」を出しました。
対象となるのは重症化のリスクが高い18歳以上の人で、感染が確認されてからすぐに処方を受け、5日以内に投与を開始すべきだとしています。
「モルヌピラビル」はウイルスの増殖を抑えて重症化を防ぐ薬で、臨床試験では重症化のリスクが高い大人に対して発症から5日以内に投与を始めたところ、入院するリスクが30%低下したと発表されています。
一方でFDAは、使用にあたってはほかの治療薬が手に入らなかったり、健康上の理由から使えない場合に限るとしているほか、妊娠中の女性については投薬の効果がリスクを上回ると医師などが判断した場合に限るとしています。
「モルヌピラビル」をめぐっては、アメリカ政府が310万回分購入することでメルクと合意しているほか、すでに承認したイギリスは感染者の急増に対応するため追加の契約を決めていますが、フランスは臨床試験で当初期待していたほどの効果がなかったとして発注をキャンセルするなど対応が分かれています。
日本では厚生労働省が12月24日に専門家部会を開き、その後、国内初の新型コロナの飲み薬として正式に承認する見通しです。
メルクのコロナ飲み薬 欧州で対応分かれる 厚労省12月24日承認審査(12/23)
2021年12月23日

厚生労働省が12月24日に承認審査を行う、アメリカの製薬大手メルクが開発した新型コロナウイルスの飲み薬について、イギリスは感染者の急増に対応するため追加の契約を決めた一方、フランスは臨床試験で当初期待していたほどの効果はなかったとして発注をキャンセルするなど、対応が分かれています。
アメリカの製薬大手メルクによりますと、飲み薬「モルヌピラビル」をめぐって、臨床試験では入院や死亡のリスクをおよそ30%低下させる効果がみられ、これまで30以上の国と契約を結んだということです。
一日の新たな感染者が10万人を超えるなど感染が急拡大するイギリスは、12月22日、ファイザーが開発した飲み薬に加え、メルクの「モルヌピラビル」も追加で175万回分購入する契約を結んだことを明らかにしました。
一方、フランスは、12月22日、メルクの臨床試験の結果が当初期待していたほどではなかったとして発注をキャンセルし、代わりにファイザーの飲み薬を調達する方針を明らかにするなど、ヨーロッパでは対応が分かれています。
EUの医薬品規制当局、EMA=ヨーロッパ医薬品庁は11月、緊急時などには使用できると発表しましたが、承認に向けては現在、審査を進めています。
米FDA ファイザー開発の新型コロナ飲み薬に「緊急使用の許可」(12/23)
2021年12月23日
アメリカFDA=食品医薬品局は12月22日、製薬大手ファイザーが開発した新型コロナウイルスの重症化を防ぐ飲み薬について「緊急使用の許可」を出しました。
FDAは12月22日ファイザーが開発した飲み薬「パクスロビド」について、新型コロナウイルスの感染症の重症化を防ぐ効果があるとして、正式な承認の前に薬を使用できるようにする「緊急使用の許可」を出しました。
対象となるのは12歳以上で重症化のリスクが高い人で、FDAは感染が確認されてからすぐに医師の処方を受け、5日以内に投与を開始すべきだとしています。
「パクスロビド」は5日間にわたって1日2回投与することでウイルスの増殖を抑えるもので、ファイザーは重症化のリスクが高い人に対し発症から5日以内に投与した場合、入院したり死亡したりするリスクが88%低下したとする臨床試験の結果を公表しています。
また、実験では変異ウイルスのオミクロン株でも増殖を抑える効果が見られたとしています。
FDAは「アメリカで飲むタイプの新型コロナウイルス治療薬が使えるようになるのは初めてで、変異ウイルスが広がる中、たたかうための新たな手段となる」とコメントしています。
アメリカは1000万回分購入することで会社側と合意しているほか、イギリスも275万回分を購入すると発表するなど、各国で確保の動きが進んでいます。
ファイザーは来年末までに1億2000万回分生産できる見込みだとしています。
中外製薬 新型コロナ軽症患者用飲み薬の開発終了 承認申請断念(12/17)
2021年12月17日

新型コロナウイルスに感染した軽症の患者用に開発を進めてきた飲み薬について、製薬大手の中外製薬は開発を終了し、厚生労働省への承認申請を断念したことを発表しました。
この薬は、C型肝炎の治療薬としてアメリカの製薬会社が開発を進めてきた「AT-527」と呼ばれる抗ウイルス薬で、スイスの製薬大手「ロシュ」などが新型コロナウイルスに感染した軽症患者の重症化を防ぐ飲み薬としての開発を進めていました。
中外製薬は、日本国内での治験を担当していましたが、2021年10月、海外で行われてきた治験の中間結果で、軽症や中等症の患者でウイルス量の明らかな減少が示されなかったことなどから、この薬の開発を終了し、厚生労働省への承認申請も断念したということです。
これに伴って、厚生労働省は中外製薬に対して、この薬の開発にかかる補助金4億5800万円の一部について返還を求めることにしています。
中外製薬は「新型コロナウイルスに対する治療の選択肢の拡充を目指して開発を進めてきましたが、当社による開発を終了することとなりました。開発にお力添えくださった患者さん、医療関係者をはじめとする皆様に感謝申し上げます」とするコメントを出しました。
ファイザー 開発中のコロナ飲み薬“入院や死亡リスク89%減”(12/15)
2021年12月15日

アメリカの製薬大手ファイザーは12月14日、開発中の新型コロナウイルスの増殖を抑えるための飲み薬について、臨床試験の最終的な分析の結果、入院や死亡のリスクを89%低下させる効果がみられたと発表しました。
ファイザーは12月14日、新型コロナウイルス感染症の重症化を防ぐ飲み薬について、臨床試験の最終的な分析結果を発表しました。
臨床試験では、新型コロナウイルスに感染し重症化リスクのある患者を、飲み薬を投与するグループと、プラセボと呼ばれる偽の薬を投与するグループに分けて症状の経過を比較しました。
その結果、発症から3日以内に投与を始めた場合では、入院したり死亡したりした人は、
▽プラセボを投与したグループで682人中44人だったのに対し、
▽薬を投与したグループでは697人中5人となり、
入院や死亡のリスクが89%低下したということです。
また、発症から5日以内に投与を開始した場合でも、入院や死亡のリスクは88%低下したとしています。
さらに新たな変異ウイルス、オミクロン株に対する効果についても、実験室で確認したところ、増殖を抑える効果がみられたということです。
新型コロナウイルスの重症化を防ぐための飲み薬は、アメリカの製薬大手メルクの「モルヌピラビル」がイギリスで使用されているほか、アメリカのFDA=食品医薬品局が、最終的に緊急使用の許可を出すかどうか審査を進めています。
飲み薬「モルヌピラビル」12月24日にも国内初承認に向け審議へ(12/15)
2021年12月15日

アメリカの製薬大手メルクが開発した新型コロナウイルスの飲み薬について、厚生労働省は12月24日にも承認に向けた審議を行うことが関係者への取材で分かりました。
承認されれば、国内で初めての新型コロナの飲み薬となり、年内にも患者が服用できるようになる見通しです。
承認が審議されるのは、新型コロナの飲み薬「モルヌピラビル」です。
メルクが12月3日に承認を申請していましたが、12月24日にも厚生労働省が専門家部会を開くことが関係者への取材で分かりました。
部会では承認が了承される見込みで、その後数日以内に厚生労働省が国内初の新型コロナの飲み薬として正式に承認する見通しです。
メルクによりますと、臨床試験では、発症から5日以内の軽症から中等症の患者のうち、重症化リスクがある人に対して、入院や死亡のリスクを30%低下させる効果が確認されています。
妊娠中の患者への使用は推奨されていません。
自宅で服用できるうえ、病院での管理もしやすいことから、患者や医療機関の負担の軽減につながると見られています。
厚生労働省は、すでにメルク側と年内に20万人分、合わせて160万人分の供給を受けることで合意していて、承認した場合は年内にも患者が服用できるよう、すみやかに都道府県が指定した薬局などに配送することにしています。
オミクロン株に治療薬は効くのか? 専門家の見方は?(12/6)
2021年12月6日
12月6日、日本国内で3例目となる新型コロナの新たな変異ウイルス、オミクロン株の感染者が確認されました。
NHKが12月6日午後4時時点でまとめたところ、オミクロン株の感染は日本を含め世界の44の国と地域で確認されています。
瞬く間に世界に広がる新たな変異ウイルスに治療薬は果たして効くのか。
これまでに使われている治療薬や開発中の治療薬など、さまざまな治療薬のオミクロン株への効果について専門家に聞きました。
「点滴薬」と「飲み薬」効果は?

話を聞いたのは新型コロナウイルスの治療に詳しい愛知医科大学の森島恒雄 客員教授です。
オミクロン株に対する治療薬の効果について、森島客員教授は新型コロナウイルスの表面にある突起「スパイクたんぱく質」を標的にしている点滴薬は、変異がある場所によっては効果に影響が出るおそれがある一方、ウイルスの増殖を防ぐ軽症者用の飲み薬については、効果は変わらないのではないかと指摘しています。

新型コロナウイルスの治療薬は、
▽ウイルスが細胞に侵入するのを防ぐ薬、
▽細胞に侵入したウイルスが増殖するのを抑える薬、
▽増殖したウイルスに反応する過剰な免疫の働きを抑える薬
の3つのタイプがあります。
細胞に侵入するのを防ぐ薬 “効果に影響出るおそれ”
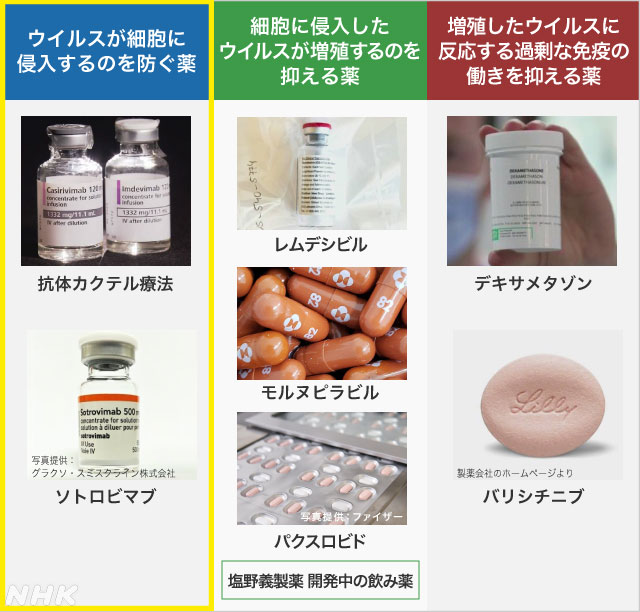
国内で承認されている薬のうち「抗体カクテル療法」の薬と「ソトロビマブ」は抗体医薬と呼ばれ、ウイルスが細胞に侵入する際の足がかりとなる、表面にある突起の「スパイクたんぱく質」を標的にして攻撃することで細胞への侵入を防ぎます。
これらの薬は、患者が軽症のうちに重症化を防ぐために点滴で投与されます。
海外で行われた臨床試験では、新型コロナウイルスに感染した人の入院や死亡のリスクが「抗体カクテル療法」ではおよそ70%、「ソトロビマブ」ではおよそ79%低下したとしています。
これらの薬のオミクロン株に対する効果について、専門家からはオミクロン株では「スパイクたんぱく質」におよそ30もの変異があることから、標的としているスパイクたんぱく質の部分に変異があれば、細胞へのウイルスの侵入を防ぐ効果に影響が出るおそれがあるとする指摘が出ています。
愛知医科大学の森島恒雄 客員教授は「抗体医薬はスパイクたんぱく質そのものを標的にしているので、今回の変異による影響は大きいと思う。ただ、標的のスパイクたんぱく質がウイルスが変異した部分と重なっていなければ、治療効果が保たれる見込みがあると思われる」と指摘しています。

ソトロビマブについて、開発したイギリスの製薬大手「グラクソ・スミスクライン」はオミクロン株に似せたウイルスを使った実験の結果、オミクロン株に対しても効果があることが示されているとしています。
細胞内での増殖を防ぐ薬 “オミクロン株でも効果変わらないか”

一方、細胞に侵入したウイルスが増殖するのを抑えるタイプの薬は細胞内でウイルスが増殖するのに必要な酵素が作られるのを防ぎます。
国内で承認され、中等症や重症の患者に使われている点滴薬「レムデシビル」もこのタイプです。
また、現在、感染した人が自宅などで療養する際にも使えるよう、主に軽症者用の飲み薬としての開発が進められていて、
▽アメリカの製薬大手、メルクが開発し、厚生労働省に承認申請した飲み薬「モルヌピラビル」や、
▽ファイザーが開発し、アメリカで緊急使用の許可を申請した飲み薬「パクスロビド」、
▽塩野義製薬が開発中の飲み薬も同じタイプです。
会社側によりますと、臨床試験では「モルヌピラビル」は入院や死亡のリスクを低下させる効果がおよそ30%で「パクスロビド」はおよそ89%だったとしています。
森島客員教授によりますと、このタイプの薬は細胞内に入ったウイルスに作用する働きがあり、オミクロン株に見られる変異には大きく影響されないと考えられるため、これまでの新型コロナウイルスに対してと効果は変わらないのではないかとしています。
過剰な免疫抑える薬 “治療効果は期待できる”
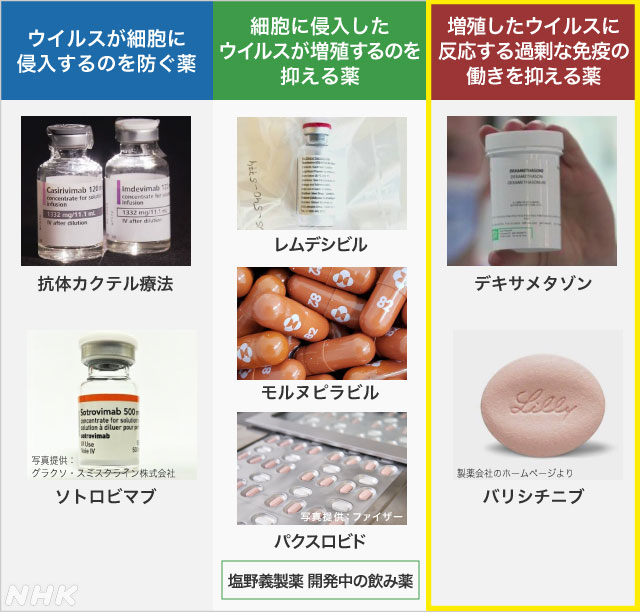
さらに、増殖したウイルスに反応する過剰な免疫の働きを抑える「デキサメタゾン」や「バリシチニブ」などの薬については、免疫の反応を抑えるため変異とは関わりなく、効果は変わらないとみられるということです。
森島客員教授は「抗体医薬の治療効果がいきなりゼロになることはなく、どの程度、下がるのかは、実際の治療の現場を見ないと分からない。開発が進む飲み薬については、実際に細胞の中に入ったウイルスが増殖するのを防ぐ仕組みで、治療効果はそのまま期待できると思う。オミクロン株で影響を受けるとしても今後承認された場合には飲み薬、そして抗体医薬を早めに投与し、重症化を防ぐといった治療戦略は変わらない」と話しています。
デンマークでの確認183件 イギリスは246人に

海外では連日、オミクロン株の感染が相次いで確認されています。
デンマークの保健当局は、12月5日までに国内で確認された感染例の数が183件となり、2日前までの18件から大幅に増加したと公表しました。
デンマーク保健当局の担当者は「デンマークでは旅行者やその関係者以外でオミクロン株の感染が確認されている」と懸念を示しています。
イギリスでは12月5日、1日で新たに86人の感染が確認され、これまでの累計では246人となっています。
イギリス政府は、すでに3回目接種については、2回目からの間隔を6か月から3か月に大幅に短縮するなど警戒を強めています。
また保健当局は、オミクロン株では感染した人がほかの人に感染を広げるようになるまでの期間が、短くなっている可能性があるという分析を明らかにし、12月7日からは入国の規制についてワクチン接種済みかどうかにかかわらず、すべての人を対象に入国前の検査を義務づけると発表しました。
オミクロン株 日本を含め44の国と地域で確認(12月6日16:00時点)

NHKが12月6日午後4時時点でまとめたところ、新たな変異ウイルス、オミクロン株の感染は、日本を含め世界の44の国と地域で確認されています。
【アジア】
日本、香港、韓国、インド、シンガポール、マレーシア、スリランカ、タイ、モルディブ
【オセアニア】
オーストラリア
【北米】
アメリカ、カナダ
【中南米】
メキシコ、ブラジル、チリ
【ヨーロッパ】
イギリス、ドイツ、フランス、イタリア、オランダ、ベルギー、デンマーク、チェコ、オーストリア、スウェーデン、フィンランド、ノルウェー、スペイン、ポルトガル、スイス、アイルランド、ギリシャ、アイスランド、ルーマニア
【中東】
イスラエル、サウジアラビア、UAE=アラブ首長国連邦
【アフリカ】
南アフリカ、ボツワナ、ナイジェリア、ガーナ、ジンバブエ、チュニジア、ザンビア
松野官房長官 3回目接種「一定程度の国民に前倒し可能」

また感染の第6波に備えて、12月1日から始まった新型コロナのワクチンの3回目接種。
松野官房長官は午後の記者会見で、3回目のワクチン接種で2回目との間隔を短縮する対象などについて「オミクロン株に対するワクチンの効果や、オミクロン株の特徴については、専門家や製薬企業で検証が進められており、できるだけ早期にこれらを見極めたうえで前倒しの範囲や方法をお示ししたい」と述べました。
そして「ファイザーとモデルナのワクチンを用いるが、合わせて1億7000万回分の供給を受ける契約を締結済みであり、総量として必要なワクチンは確保できる見込みだ。モデルナのワクチンを、ファイザーのワクチンを接種した方にも活用することにより、優先度に応じ一定程度の国民に前倒しが可能だと報告を受けている」と述べました。

承認申請中の新型コロナ飲み薬 発症5日以内の服用推奨で課題も(12/4)
2021年12月4日

アメリカの製薬大手メルクが12月3日、新型コロナウイルスの飲み薬の承認を日本国内で初めて申請しましたが、発症から5日以内の服用が推奨されているため、早期に患者に届けられるかどうかが課題となります。
メルクは12月3日、軽症と中等症の患者向けに開発した新型コロナウイルスの飲み薬「モルヌピラビル」の承認を日本法人を通じて厚生労働省に申請しました。
日本国内で飲み薬の承認申請が行われたのは初めてで、自宅でも服用できるため、患者や医療機関の負担の軽減にもつながると期待されています。
臨床試験では、発症から5日以内の重症化リスクがある患者で入院や死亡のリスクが30%低下したとされ、厚生労働省は年内にも承認の可否を判断する方針です。
一方、課題となるのが服用までの時間です。
モルヌピラビルは、症状が出てから5日以内に服用することが推奨されています。
処方を受けるには、医療機関などで検査を受けることが条件となる見通しですが、感染が急拡大した場合は業務がひっ迫してすぐに検査が受けられず、結果が出るのにも時間がかかるおそれがあります。
さらに、検査結果が出たあと、薬を入手するまでに通常より時間がかかるケースも出てくると見られています。
陽性となった場合、厚生労働省は周囲との接触をできるだけ避けてもらうため、患者が薬局に出向くのではなく、自宅で受け取るようにする方法を検討しています。
受診した医療機関が、患者の最寄りの薬局にFAXなどで処方箋を送り、薬局の薬剤師が電話やオンラインで患者に服用方法などを指導したあと運送業者を通じて薬が配送される仕組みです。
しかし、当面は供給量が限られるため、自治体が指定した薬局に配分される予定で、人口の少ない地域や離島などに住む患者で指定された薬局が身近にない場合配送に日数がかかるおそれがあります。
薬局「経過観察が大切」
医療機関や薬局では飲み薬承認への期待が高まる一方、自宅で服用する際の経過観察が大切だという声や処方の基準を明確にしてほしいという声が聞かれました。
JR千葉駅の構内にある薬局では医師から処方箋を受け取って患者の自宅に薬を配送する仕組みを2020年3月から取り入れています。
処方箋が届くと薬剤師が患者に電話で連絡をして薬の飲み方などを説明する「服薬指導」を行ったうえで、宅配業者を通じて配送します。
新型コロナの患者や、感染が心配で通院を控えている高齢者など、これまでに1000件ほど利用があったということです。
飲み薬が実用化された場合、隣にあるクリニックと連携すれば陽性と判明したその日のうちか翌日には届けることができると見込んでいます。
薬剤師の白鳥香さんは「飲み薬という選択肢が増えることは安心材料になると感じます。薬を届けたあとに状況を確認することが大切になってくると思うし、副作用の情報もしっかり把握していきたい」と話していました。
医療機関「処方の基準を明確にしてほしい」
また、薬局の隣のクリニックではPCR検査やオンライン診療を行っていますが2021年夏の第5波の際には1日に200人ほどが検査に訪れ検査結果が出るまでに2、3日かかることもあったということです。
発症後5日以内に服用を始めるためにはできるだけ早い受診を呼びかける必要があると考えています。
クリニックの柳本蔵人医師は「これまで点滴の薬は出ていたがわれわれのようなクリニックで使うのは難しかった。飲み薬になれば早めに投与して重症化を防げるようになるのではないか。ただ、第5波のときも最初は軽症だった患者が急に状態が悪化することがあり自宅で服用する際のフォローアップは大切になると思う。また、薬の量は限られているので重症化する人に行き届かない事態にならないように、どういった人に処方するのか国には基準を明確にしてもらいたい」と話していました。
米製薬大手メルク 新型コロナの飲み薬 日本での使用 承認申請(12/3)
2021年12月3日

アメリカの製薬大手メルクが、新型コロナウイルスの飲み薬の日本国内での使用を認めるよう厚生労働省に承認を申請しました。
承認が申請されたのはメルクが新型コロナウイルスの軽症と中等症の患者向けに開発した飲み薬「モルヌピラビル」です。
国内で新型コロナウイルスの飲み薬の承認申請が行われたのは初めてです。
承認されれば自宅でも服用できるようになるほか、これまでの治療薬に比べて病院での管理が簡単になり、患者や医療機関の負担の軽減につながると期待されています。
メルクの発表によりますと「モルヌピラビル」は臨床試験では、発症から5日以内で重症化リスクがある患者に対し、入院や死亡のリスクを30%低下させる効果が確認されたということです。
安全性については大きな懸念は確認されなかったとする一方、胎児の成長に深刻な影響が出る可能性が否定できないなどとして妊娠中の患者への使用は推奨していません。
厚生労働省はすでにメルク側と160万人分の供給を受けることで合意していますが、当面は流通量が限られるため、特定の医療機関や薬局に供給することなどが検討されています。
厚生労働省は有効性や安全性を審査したうえで年内にも専門家部会を開いて承認の可否を判断する方針です。
「モルヌピラビル」は、2021年11月、世界で初めてイギリスで承認され、アメリカでも近く緊急使用の許可を出すか判断される見通しです。
初めての飲み薬「モルヌピラビル」
「モルヌピラビル」は、アメリカの製薬大手「メルク」が開発した重症化を防ぐ効果があり、感染から間もない患者に使える初めての飲み薬です。
ウイルスが細胞に侵入したあと、設計図となる「RNA」をコピーして、ウイルスが増殖するのに必要な酵素の働きを抑え、増殖を防ぎます。
感染が確認されたらなるべく早く、症状が出た場合は5日以内に服用することが推奨され、新型コロナウイルスの軽症から中等症の患者で、肥満や糖尿病など、感染した場合に重症化するリスクが少なくとも1つはある人が対象です。
メルクは、重症化リスクがある患者の入院や死亡のリスクを低下させる効果は、2021年10月には治験の初期段階での解析の結果、およそ50%としていましたが、11月には追加の解析を行った結果、およそ30%だったと発表しました。
2021年10月の発表では、発症から5日以内の患者で、重症化リスクのある760人余りを薬を投与するグループと、プラセボと呼ばれる偽の薬を投与するグループに分けて、経過を比較したところ、
▽プラセボを投与したグループでは、入院した人や死亡した人の割合が14.1%だったのが、
▽薬を投与したグループでは7.3%で、入院や死亡のリスクがおよそ50%低下したとしていました。
一方で、11月に発表した、追加のデータを加えた治験の解析結果では、1400人余りを薬を投与するグループと、プラセボを投与するグループに分けて、経過を比較したところ、
▽プラセボを投与したグループでは、入院した人や死亡した人の割合が9.7%だったのが、
▽薬を投与したグループでは6.8%で、入院や死亡のリスクがおよそ30%低下したとしています。
また、副作用について、薬を服用したあとで有害事象が出た割合は、薬を服用したグループと、プラセボを服用したグループで変わらなかったとしています。
「モルヌピラビル」は、2021年11月にイギリスの規制当局が承認しているほか、アメリカでもFDA=食品医薬品局の専門家委員会が緊急使用の許可を出すことを支持する結論を賛成13人、反対10人の賛成多数で可決していて、これを受けて近く、FDAが最終的に判断する見通しです。
松野官房長官「年内の承認目指し迅速に審査」
松野官房長官は午後の記者会見で「きょう特例承認を求める申請があったと聞いている。今後、年内の承認を目指し、まずはPMDA=医薬品医療機器総合機構で優先的かつ迅速に審査を行っていくものと承知している」と述べました。
ファイザー 開発中“コロナ飲み薬” FDAに緊急使用許可を申請(11/17)
2021年11月17日

アメリカの製薬大手ファイザーは開発中の新型コロナウイルスの増殖を抑えるための飲み薬について、FDA=食品医薬品局に緊急使用の許可を申請したと発表しました。
ファイザーが開発中の飲み薬はエイズの発症を抑える薬として使われている抗ウイルス薬とともに投与され、新型コロナウイルスの発症初期の患者が重症化するのを防ぐ効果が期待されています。
ファイザーは11月16日この薬について軽症から中程度の症状があり、重症化のリスクがある大人の患者に対して緊急使用を許可するようFDAに申請したと発表しました。
会社が11月5日に発表した臨床試験の暫定的な分析結果ではこの薬を投与したグループではそうでないグループと比べて入院や死亡のリスクがおよそ89%低下したとされています。
新型コロナウイルスの重症化を防ぐための飲み薬としてはアメリカの製薬大手メルクの「モルヌピラビル」が11月4日、イギリスの医薬品規制当局から承認を受けていてFDAにも緊急使用の許可が申請されています。
コロナ軽症患者向け飲み薬 160万回分確保で合意 後藤厚労相(11/11)
2021年11月11日
新型コロナウイルス対策をめぐり後藤厚生労働大臣は、軽症患者向けの飲み薬を開発する製薬大手「メルク」の日本法人との間で、薬事承認が行われることを前提に国内向けに160万回分の飲み薬を確保することで合意したと発表しました。
後藤厚生労働大臣は、11月10日夜、厚生労働省で記者団の取材に応じ、新型コロナウイルスの増殖を抑える軽症患者向けの飲み薬「モルヌピラビル」を開発しているアメリカの製薬大手「メルク」の日本法人「MSD」との間で160万回分の飲み薬を確保することで合意したと発表しました。
具体的には日本国内での薬事承認が行われることを前提に国内向けに年内に20万回分、2022年2月と3月にそれぞれ20万回分の供給を受けるとともに、それ以外に100万回分を確保したということです。
後藤大臣は「国民の健康を守り、命を守っていくことに対し、大変大きな効果と大きな意味があることだ。国内産の経口治療薬も含め、今後とも必要な対応を進めていきたい」と述べました。
コロナ第6波に備える “飲み薬” 治療薬の開発はどこまで(11/8)
2021年11月8日
新型コロナウイルスの感染はいまは収まってきていますが、いつ来るか分からない感染拡大の第6波に備える動きも進んでいます。感染する前に接種するワクチンについては、アメリカで5歳から11歳の小学生の年代のワクチン接種も始まり、日本国内でも3回目の接種の議論が…続きを読む
ファイザー コロナ飲み薬 入院や死亡のリスク 89%低下と発表(11/5)
2021年11月5日
アメリカの製薬大手ファイザーは11月5日、開発中の新型コロナウイルスの増殖を抑えるための飲み薬について、最終段階の臨床試験で入院や死亡のリスクを89%低下させる効果がみられたと発表しました。
ファイザーが開発中の新型コロナウイルスの増殖を抑えるための飲み薬は、現在、最終段階の臨床試験が行われていて、会社は11月5日にその暫定的な分析結果を発表しました。
臨床試験では、新型コロナの発症から3日以内で、重症化リスクのある患者770人余りを薬を投与するグループと、プラセボと呼ばれる「偽の薬」を投与するグループに分けて症状の経過を比較しました。

その結果、入院または死亡した人はプラセボを投与したグループでは385人中27人でしたが、薬を投与したグループでは389人中3人で、入院や死亡のリスクが89%低下したとしています。
ファイザーは、今後速やかにアメリカFDA=食品医薬品局に緊急使用の許可を申請する手続きを進めるとしています。
ブーラCEOは「パンデミックを終わらせるうえでの『ゲームチェンジャー』となる結果だ。規制当局に認められれば、多くの命を救える可能性がある」とコメントしています。
新型コロナウイルスの増殖を抑えるための薬をめぐっては、アメリカの製薬大手メルクが開発した飲み薬が、11月4日にイギリスの医薬品規制当局から承認を受けたばかりです。
飲み薬「モルヌピラビル」イギリスが世界で初承認(11/4)
2021年11月4日

イギリスの医薬品規制当局は、新型コロナウイルスの増殖を抑えるための飲み薬「モルヌピラビル」を承認したと発表しました。新型コロナウイルスに対する飲むタイプの抗ウイルス薬を承認したのは、世界で初めてだとしています。

イギリスの医薬品規制当局の11月4日の発表によりますと、アメリカの製薬大手メルクが開発を進める、新型コロナウイルスの増殖を抑えるための飲み薬「モルヌピラビル」について、安全性や有効性などを検証した結果、承認したということです。
新型コロナウイルスに対する飲むタイプの抗ウイルス薬を承認したのは、世界で初めてだとしています。
発表では、臨床試験の結果として「モルヌピラビル」は感染の初期段階で効果があり、感染が確認されたらなるべく早く、症状が出た場合は5日以内に、服用することを推奨しています。
また、対象となるのは軽症から中等症の患者で、肥満や糖尿病などの重症化するリスクが少なくとも1つはある人だとしています。
イギリスのジャビド保健相は「イギリスは、家庭で服用できる新型コロナの抗ウイルス薬を承認した最初の国となった」とコメントしています。
「モルヌピラビル」についてメルクは10月、アメリカのFDA=食品医薬品局に緊急使用の許可を申請するとともに、臨床試験の結果として、薬を投与したグループでは投与していないグループと比べ、入院や死亡のリスクが50%低下したと発表していました。

メルク 年内に1000万回分を生産
開発したアメリカの製薬大手メルクは「新型コロナウイルスのパンデミックと闘うためのワクチンや薬の中に、飲み薬という重要な手段が加わった」とする声明を発表しました。
メルクは「モルヌピラビル」を年内に1000万回分生産するとしています。
また、アメリカFDAや、EUの医薬品規制当局のEMA=ヨーロッパ医薬品庁に使用の許可の申請を行っているほか、各国の規制当局に対しても使用許可の申請の手続きを進めているとしています。
新型コロナ 軽症者向け飲み薬 塩野義製薬が海外でも臨床試験へ(11/1)
2021年11月1日
大阪に本社がある製薬会社「塩野義製薬」は、国内で新型コロナウイルスの新たな感染者が大きく減少していることを受けて、飲み薬の臨床試験をシンガポールなど海外でも行う方針を明らかにしました。

新型コロナウイルスの軽症者向け飲み薬の開発を進めている塩野義製薬は、2021年9月から最終段階の臨床試験に入っていて、国内のおよそ2100人を対象に薬の有効性や安全性を確かめる方針でした。
これについて手代木功社長は11月1日の中間決算の会見で、国内で新たな感染者が大きく減少していることから、治験を受ける患者の確保が難しくなる可能性があることを明らかにしました。
こうした状況を踏まえ会社では、依然として新たな感染者の数が多いシンガポールや韓国、イギリスなど、海外でも臨床試験を行う方針を明らかにしました。
そのうえで、12月中旬までに薬の効果などに関するデータを集めたうえで、予定どおり、早ければ年内にも国への承認申請の準備に入るとしています。
手代木社長は「感染者の著しい減少で、日本国内だけで症例を集めるのは難しい。少しでも早く治療薬を提供するために、やれることをやっていく」と述べました。
また、手代木社長は、開発中の新型コロナウイルスの国産ワクチンについて、月内にも最終段階の大規模な臨床試験を始めたいという考えを示しました。
新型コロナ飲み薬 “年内の実用化を” 岸田首相が厚労相に指示(10/26)
2021年10月26日

新型コロナウイルス対策の切り札として期待されている飲み薬について、岸田総理大臣は、後藤厚生労働大臣に対し、年内の実用化を目指すとともに、必要な量の確保に向けた取り組みを加速するよう指示しました。
新型コロナウイルスの治療薬をめぐり、国内では、抗体カクテル療法などに使われる軽症患者向けの点滴薬などが承認されていますが、医師による管理が必要なため、自宅で服用できる飲み薬の開発が期待されています。
こうした中、岸田総理大臣は、閣議のあと後藤厚生労働大臣と協議し、新型コロナの飲み薬の年内の実用化を目指すとともに、必要な量の確保に向けた取り組みを加速するよう指示しました。
後藤大臣は、記者会見で「治験を支援するための補助などを行っているが、できるかぎり早く承認を進め、国民に具体的な確保状況や見通しなどを説明できるよう準備を進めたい。国民の安心を確保するための切り札と言えるので、全力を尽くしたい」と述べました。
軽症者向けの飲み薬 開発状況は
新型コロナウイルスへの効果が確認されている軽症者向けの飲み薬は現在のところありません。
症状が悪化しないうちに自宅などでも服用できる飲み薬があれば、感染しても重症化するのを防ぐことができ、亡くなる人を減らすことにつながると期待されるため、各国の製薬会社が開発を急いでいます。
開発が最も早く進んでいるのがアメリカの製薬大手「メルク」が開発している「モルヌピラビル」と呼ばれる抗ウイルス薬です。
会社の発表によりますと、治験の中で発症から5日以内の患者で、重症化リスクのある760人余りを薬を投与するグループと、プラセボと呼ばれる偽の薬を投与するグループに分けて、経過を比較したところ、
▽プラセボを投与したグループでは、入院した人や死亡した人の割合が14.1%だったのが、
▽薬を投与したグループでは7.3%だったということで、
入院や死亡のリスクがおよそ50%低下したとしています。
これを受けメルクは10月11日、モルヌピラビルについて、アメリカのFDA=食品医薬品局に緊急使用の許可を申請したと発表しました。
また、アメリカの製薬大手「ファイザー」は2種類の抗ウイルス薬を併用する治療法について、最終段階の治験を海外で進めています。
治験の暫定的な結果は、12月までに得られる見込みだとしていて、年内にもアメリカで緊急使用許可の申請を行う可能性があるとしています。
「メルク」と「ファイザー」は、それぞれ感染者と同居する人が予防的に服用することで、感染や発症を防ぐ効果があるか調べる治験も進めています。
スイスの製薬大手「ロシュ」は、「AT-527」と呼ばれるC型肝炎の治療薬として開発を進めてきた抗ウイルス薬が新型コロナウイルスにも効果があるかどうか、日本の患者を含めて最終段階の治験を進めています。
日本国内での開発などを行っている中外製薬によりますと、年内に結果がまとまる見込みで、来年にも、厚生労働省に承認申請をしたいとしています。
また、大阪に本社がある製薬会社「塩野義製薬」はことし7月から薬の安全性を確かめる第1段階の治験を進め、安全性に大きな問題はなかったとして、最終段階の治験を9月下旬から始めたと発表しました。
治験のデータは、早ければ年内にまとまる見込みだとしています。
このほか、日本の製薬会社の「富士フイルム富山化学」がインフルエンザの治療薬の「アビガン」について、同じく日本の製薬会社の「興和」が寄生虫による感染症の特効薬「イベルメクチン」ついて、それぞれ新型コロナに対する効果があるか、最終段階の治験を進めています。
飲み薬「モルヌピラビル」米で緊急使用の申請 許可なら世界初(10/11)
2021年10月11日
アメリカの製薬大手メルクは開発中の新型コロナウイルスの増殖を抑える薬「モルヌピラビル」について、アメリカFDA=食品医薬品局に緊急使用の許可を申請したと発表しました。
FDAが許可すれば、新型コロナウイルスに対する飲むタイプの抗ウイルス薬としては世界で初めて実用化されるものになります。
メルクが開発中の「モルヌピラビル」は、新型コロナウイルスの増殖を抑えるための飲み薬で、発症初期の患者が重症化するのを防ぐ効果が期待されています。
メルクは10月11日「モルヌピラビル」について軽症から中程度の症状があり重症化のリスクがある大人の患者に対して「緊急使用」を許可するようFDAに申請したことを明らかにしました。
メルクが10月1日に発表した臨床試験の暫定的な分析結果では、薬を投与したグループではそうでないグループと比べ入院や死亡のリスクがおよそ50%低下したということです。
FDAが審査の結果、緊急使用を許可すれば、新型コロナウイルスに対する飲むタイプの抗ウイルス薬としては世界で初めて実用化されるものになります。
新型コロナウイルスの感染症の重症化を防ぐため、軽症のうちに服用できる飲み薬については、メルクのほかにもアメリカの製薬大手ファイザーやスイスの製薬大手ロシュなども開発を進めています。
開発責任者「医療機関の負担 大幅軽減を期待」
「モルヌピラビル」の開発責任者を務めるメルクのダリア・ハズダ博士は、NHKのインタビューに対し「治療薬はワクチンの代わりになるものではなく、ワクチンの重要性は今後も変わらないが、パンデミックを終わらせるうえで、簡単に使える飲むタイプの治療薬はとても重要だ」と述べ、開発の意義を強調しました。
そのうえで「点滴薬と比べ迅速に投与できるため、新型コロナウイルスの治療方法を変えていく可能性がある。外来で診断された患者に対し使えるようになることで、医療機関の負担を大幅に軽減できると期待している」と述べています。
また安全性については、臨床試験で薬を投与したグループと投与しなかったグループで健康への影響に大きな差は見られなかったということですが、ハズダ博士は「今後FDAと薬による治療の効果とリスクのバランスについて議論したうえで、許可の判断が行われる。長期的な安全性を含めて引き続き検証を進めていく」としています。
新型コロナ飲み薬開発 岸田首相 “政府として後押し”(10/10)
2021年10月10日

新型コロナウイルス対策で、岸田総理大臣は横浜市内の宿泊療養施設を視察し、治験が行われている軽症者向けの飲み薬の早期開発に期待を示すとともに、政府として後押ししていく考えを示しました。
横浜市内の宿泊療養施設では、新型コロナウイルスの軽症者向けの飲み薬の安全性などを確かめる治験が行われていて、岸田総理大臣は「塩野義製薬」の手代木功社長から、年内の承認申請を目指していることなどについて説明を受けました。
このあと岸田総理大臣は記者団に対し「経口薬は、これからのコロナ対策における大きな決め手になる。年内の承認申請に向けて努力を続けるという話を聞かせていただいたので、ぜひ期待したい」と述べました。
そのうえで「世界のワクチンや治療薬の開発状況もしっかりみて、わが国の対応を考えていくことが重要だ。政治が何を考えなければいけないか、しっかり対応を考えたい」と述べ、政府として後押ししていく考えを示しました。
一方、岸田総理大臣は、東日本大震災からの復興に関連し「私の内閣でも『復興なくして日本の再生なし』という考えのもとに、しっかり取り組んでいきたい」と述べ、福島県など被災地を視察する方向で調整していると明らかにしました。
コロナ 軽症者向け「飲み薬」 各社の開発状況は(10/7)
2021年10月7日

新型コロナウイルスの患者の治療をめぐり世界中で開発が急がれている軽症者向けの「飲み薬」。症状が悪化しないうちに自宅などでも服用できれば、重症化を防ぐことができ、亡くなる人を減らすことにつながると期待されています。
この「飲み薬」について、最終段階の治験の結果を示す時期や、承認申請の時期のめどを示している会社の開発状況をまとめました。
メルク開発 モルヌピラビル“入院 死亡リスク約50%低下”

このうち、開発が最も早く進んでいるとみられるのが、アメリカの製薬大手「メルク」が開発している「モルヌピラビル」と呼ばれる抗ウイルス薬です。
会社の発表によりますと、治験の中で発症から5日以内の患者で重症化リスクのある760人余りを、この薬を投与するグループと、プラセボと呼ばれる偽の薬を投与するグループに分けて経過を比較したところ、プラセボを投与したグループでは入院した人や死亡した人の割合が14.1%だったのが、薬を投与したグループでは7.3%だったということで、入院や死亡のリスクがおよそ50%低下したとしています。
メルクは、できるだけ早くアメリカのFDA=食品医薬品局に緊急使用の許可を申請するとしています。
日本法人社長「承認得られれば速やかに供給できるよう調整」

メルクの日本法人「MSD」のカイル・タトル社長と白沢博満 上級副社長はNHKのインタビューに応じ、日本国内でも承認申請に向けて審査当局と協議を進めていることを明らかにしました。
タトル社長は「承認が得られれば国と契約を結び、必要な分量の薬を速やかに供給できるよう調整している」と述べ、承認申請を迅速に進め年内の供給を目指す考えを示しました。会社側では年内に「モルヌピラビル」を世界で1000万人分供給できるとしています。
2022年には製造体制を拡大し2000万人分を供給できる見通しだということで、白沢副社長は「まずはきたる第6波までに流通体制を整え、いずれはインフルエンザと同じように体調の悪さを自覚したら誰でも近くのクリニックで処方してもらえるよう供給体制を整備したい」と話しています。
ファイザー ロシュ 塩野義製薬も最終段階の治験

▽アメリカの製薬大手「ファイザー」は2種類の抗ウイルス薬を併用する治療法について、最終段階の治験を海外で進めています。治験の暫定的な結果は12月までに得られる見込みだとしていて、年内にもアメリカで緊急使用許可の申請を行う可能性があるとしています。
▽スイスの製薬大手「ロシュ」は「AT-527」と呼ばれるC型肝炎の治療薬として開発を進めてきた抗ウイルス薬が新型コロナウイルスにも効果があるかどうか、日本の患者を含めて最終段階の治験を進めています。
日本国内での開発などを行っている中外製薬によりますと、年内に結果がまとまる見込みで、2022年にも厚生労働省に承認申請したいとしています。
▽大阪に本社がある製薬会社「塩野義製薬」は2021年7月から薬の安全性を確かめる第1段階の治験を進め、安全性に大きな問題はなかったとして、最終段階の治験を9月下旬から始めたと発表しました。治験のデータは早ければ年内にまとまる見込みだとしています。
このほか日本の製薬会社の「富士フイルム富山化学」がインフルエンザの治療薬の「アビガン」について、同じく日本の製薬会社の「興和」が寄生虫による感染症の特効薬「イベルメクチン」ついて、それぞれ新型コロナに対する効果があるか最終段階の治験を進めています。
ワクチン接種と並び“コロナ対策の切り札”と期待

新型コロナウイルスの感染拡大の「第5波」では医療体制がひっ迫し、自宅療養者は最大で9月1日の時点で13万5000人余りに上りました。
自宅療養をしている軽症の患者が自宅で服用できる薬がなかったため、治療を受けられないまま、症状が悪化して重症化したり亡くなったりする人も相次ぎました。
2021年7月中旬には、人工的に作った抗体でウイルスの増殖を防ぐ「抗体カクテル療法」の薬が軽症患者用の治療薬として初めて承認されましたが、点滴での投与が必要で供給量が限定されているため、治療を受けられる人はおおむね50歳以上で、重症化リスクのある人など一部にとどまっています。
こうしたことから軽症患者が重症化するのを防ぐために、自宅で服用できる飲み薬が求められていて、ワクチン接種と並んで新型コロナ対策の切り札となると期待されています。
治験の実施計画によりますと、モルヌピラビルは発症から5日以内の軽症から中等症の患者が12時間おきに5日間、合わせて10回服用するとしていて、承認された場合、発症後の早い段階で使うことが想定されています。
専門家「検査体制 量・質ともに拡充する必要」

新型コロナウイルスの治療に詳しい愛知医科大学の森島恒雄 客員教授は、軽症患者用の飲み薬について「この夏の感染拡大の第5波では感染者が入院できず、自宅待機を余儀なくされる中で、重症化したり死亡したりするケースもまれではなかった。飲み薬があれば自宅待機しながら治療でき、重症患者の治療を行う医療現場などでの負担を大きく減らすことができる。ワクチン接種の拡大と合わせてこうした薬が普及して一般の診療所でも広く処方できるようになれば、インフルエンザ並みの対応に変えられるかもしれない」と話しています。
そのうえで「軽症患者用の飲み薬は、感染が分かった時点でなるべく早く投与することが望ましいので、検査体制を量・質ともに拡充していく必要がある。また、薬の供給が世界中で待ち望まれる中、日本に十分な量が供給されるか懸念がある。もし供給が限定的となる見通しならば、どのような患者に優先的に投与するか事前に考えておくことも重要だ」と指摘しました。
承認されたコロナ治療薬 3タイプに分類
いま承認されている新型コロナウイルスの治療薬は3つのタイプに分けられます。
▽ウイルスが細胞に侵入するのを防ぐ薬
▽細胞に侵入したウイルスの増殖を抑える薬
▽増殖したウイルスに反応する過剰な免疫の働きを抑える薬
ウイルスが細胞に侵入するのを防ぐ薬
新型コロナウイルスは、表面にある突起の「スパイクたんぱく質」が、人の細胞に結合することで侵入します。
現在、使われているmRNAワクチンは、人工的に作ったスパイクたんぱく質の遺伝子の一部を投与することで、体内で抗体が作られるようになりそれがウイルスのスパイクたんぱく質にくっつくことで、細胞への侵入を防ぎます。
承認されている治療薬のうち、抗体医薬と呼ばれるタイプで軽症患者に点滴で投与する「抗体カクテル療法」や「ソトロビマブ」は、ワクチンと同じような仕組みで、人工的に作った「抗体」がスパイクたんぱく質にくっつくことで、細胞に侵入するのをブロックします。
抗体がウイルスを狙い撃ちにするため、高い効果が期待される一方、供給量が限られるといった課題もあります。
細胞に侵入したウイルスの増殖を抑える薬

メルクが開発中の飲み薬「モルヌピラビル」は、ウイルスが細胞に侵入したあと設計図の「RNA」をコピーして、増殖するのに必要な酵素の働きを抑え増殖を防ぎます。
承認されている治療薬の中では、中等症から重症の患者に投与される点滴薬「レムデシビル」がこのタイプですが、医療機関で受ける必要があります。
ウイルスが細胞の中で増殖する仕組みは、ほかのウイルスでも共通しているため、別の病気の治療にも使われる薬を転用する形で開発が進められています。
増殖したウイルスに反応する過剰な免疫の働きを抑える薬
いま新型コロナの治療に使われている薬のうち、主に重症患者に使われるのが「デキサメタゾン」と「バリシチニブ」です。
ウイルスが体内で増殖し炎症を引き起こす物質が過剰に出ると、免疫の働きが暴走し、肺に傷がつくなど体に深刻なダメージを受けることがありますが、これらの薬は免疫の働きや炎症を抑える役割を果たします。
“コロナ飲み薬”開発の製薬大手幹部「日本でも年内供給を」(10/7)
2021年10月7日

新型コロナウイルスの軽症患者向けの飲み薬を開発している製薬大手「メルク」の日本法人の社長らが、NHKのインタビューに応じ、日本国内でも承認申請の準備を速やかに進め、年内の供給を目指す考えを示しました。
インタビューに応じたのは、アメリカの製薬大手メルクの日本法人「MSD」のカイル・タトル社長と白沢博満上級副社長です。
メルクは、10月1日、新型コロナウイルスの増殖を抑える軽症患者向けの飲み薬、「モルヌピラビル」について最終段階の治験で、患者の入院や死亡リスクを半減させる効果がみられたと発表していて、MSDのタトル社長らは日本国内でも承認申請に向けて審査当局と協議を進めていることを明らかにしました。

そのうえでタトル社長は「承認が得られれば、国と契約を結び、必要な分量の薬を速やかに供給できるよう調整している」と述べ、承認申請を迅速に進め、年内の供給を目指す考えを示しました。
これまで日本で承認された新型コロナの軽症患者用の治療薬はいずれも点滴薬で、医師による管理が必要なため、自宅で服用できる飲み薬の開発が期待されていて、会社側では年内に「モルヌピラビル」を世界で1000万人分供給できるとしています。

来年には製造体制を拡大し、2000万人分を供給できる見通しだということで、白沢副社長は「まずはきたる第6波までに流通体制を整え、いずれはインフルエンザと同じように、体調の悪さを自覚したら誰でも近くのクリニックで処方してもらえるよう供給体制を整備したい」と話していました。
米で開発中の飲み薬「モルヌピラビル」“リスク50%低下”(10/2)
2021年10月2日
アメリカの製薬大手メルクは10月1日、開発中の新型コロナウイルスの増殖を抑える薬について、最終段階の臨床試験で入院や死亡のリスクをおよそ50%低下させる効果がみられたと発表しました。
アメリカの製薬大手メルクが開発中の「モルヌピラビル」は、新型コロナウイルスの増殖を抑えるための飲み薬で、現在、発症初期の患者が重症化するのを防ぐ効果を確かめる最終段階の臨床試験が行われています。
10月1日、メルクは、この臨床試験の暫定的な分析結果を発表しました。
それによりますと、臨床試験では、発症から5日以内の患者で重症化リスクのある760人余りを、この薬を投与するグループと、プラセボと呼ばれる偽の薬を投与するグループに分けて症状の経過を比較しました。
その結果、▼プラセボを投与したグループでは、入院した人や死亡した人の割合が14.1%だったのに比べ、▼薬を投与したグループでは7.3%になったということで、入院や死亡のリスクがおよそ50%低下したとしています。
メルクは「良好な結果が得られた」として独立した委員会の推奨に基づいて臨床試験の参加者の募集を停止し、できるだけ早くアメリカFDA=食品医薬品局に緊急使用の許可を申請するとしています。
新型コロナウイルスの感染症の重症化を防ぐため、軽症のうちに服用できる飲み薬については、メルクのほかにもアメリカの製薬大手ファイザーやスイスの製薬大手ロシュなども開発を進めています。
飲み薬タイプのコロナ治療薬 臨床試験入りを発表 塩野義製薬(9/28)
2021年9月28日

大阪に本社がある製薬会社「塩野義製薬」は、開発を進めている新型コロナウイルスの飲み薬タイプの治療薬について、有効性や安全性を調べるための次の段階の臨床試験に入ったと発表しました。簡単に服用できる飲み薬タイプへの期待が高まる中、今後開発が順調に進むかが注目されます。
「塩野義製薬」は、飲み薬のタイプの新型コロナウイルスの治療薬の開発を進めています。
2021年7月からは薬の安全性を確かめる第1段階の臨床試験を進めてきましたが、9月28日、現時点では安全性に大きな問題はなかったことを明らかにしました。
これを踏まえて、会社は9月27日から次の段階の臨床試験に入ったということです。
次の段階では、軽症の患者か無症状の人を対象に、1日1回、5日間にわたって薬を投与し、有効性や安全性を確かめることにしています。
医療機関の入院患者だけではなく、宿泊療養者なども対象にするとしています。
塩野義製薬は、試験の規模や終了時期のめどを明らかにしていませんが、年内には100万人分を供給できる生産体制を整えたいとしています。
新型コロナの軽症患者に使用できる薬としては、国内では抗体カクテル療法に続いて、9月27日、イギリスの製薬大手、グラクソ・スミスクラインの「ソトロビマブ」が承認されましたが、いずれも飲み薬のタイプではありません。
このため、簡単に服用できる飲み薬への期待が高まっており、今後、開発が順調に進むかが注目されます。