新型コロナウイルスの治療薬として期待される薬品について、世界中の研究機関や製薬企業が臨床試験を実施。治療法の確立につながるか、注目されています。
治療薬開発 現状は
目次 ※ クリックすると各項目に移動 ※ タップすると各項目に移動
イベルメクチン コロナ治療薬の承認申請を断念 有効性見られず(9/26)
2022年9月26日

寄生虫が原因で失明などが引き起こされる感染症の特効薬「イベルメクチン」について、新型コロナ患者に投与しても、有効性が見られなかったとする治験の結果を名古屋市に本社がある製薬会社「興和」が発表しました。新型コロナの治療薬としての承認申請を断念するとしています。
興和は9月26日、東京都内で記者会見を開き、治験の結果を明らかにしました。
それによりますと、治験は2021年11月から8月まで12歳以上の軽症のコロナ患者1030人を対象に行われ、一日1回、3日間、イベルメクチンを服用するグループと偽の薬を服用するグループに分けて、患者も医師もどちらが投与されているか分からない方法で比較したということです。
その結果、いずれのグループでも投与から4日前後で発熱やのどの痛みなどの症状が治まり、薬によって改善したという有効性が見いだせなかったということで、会社は新型コロナの治療薬としての承認申請を断念すると発表しました。
イベルメクチンは、ノーベル生理学・医学賞を受賞した北里大学の大村智特別栄誉教授の研究を元に開発された、寄生虫によって失明やリンパ管の腫れが引き起こされる病気の特効薬で、新型コロナへの効果があるか各国で研究が進められましたが、2022年3月、ブラジルなどの研究グループが入院に至るリスクを下げるなどの効果はなかったとする臨床試験の結果を発表していました。
三輪芳弘社長は「全社挙げて治験に臨んできたが、この結果では承認申請を考えることはできない。結果を受け入れたい」と述べました。
アストラゼネカ注射薬 厚労省承認 事前投与で発症防ぐ効果期待(8/30)
2022年8月30日

新型コロナウイルスに感染した人の重症化予防に加え、事前に投与することで発症を防ぐ効果が期待される、イギリスの製薬大手、アストラゼネカの注射薬について、厚生労働省は使用を正式に承認しました。がんの治療などで免疫の働きが低下し、ワクチンの効果が十分に得られない人などに使用される予定です。
承認されたのは、新型コロナウイルスの働きを抑える抗体を注射で投与する「抗体医薬」「エバシェルド筋注セット」です。
アストラゼネカによりますと、2021年3月まで行われた感染していない人が対象の治験では、発症リスクが77%抑えられ、効果が半年間続いたほか、2021年7月まで行われた軽症から中等症の人が対象の治験では、発症から7日以内の投与で、重症化や死亡のリスクを50%減らす効果が確認されたということです。
欧米各国では感染前に使用できる薬として承認されていて、厚生労働省は8月30日、使用すること正式に承認しました。
国内では主に、がんの治療などで免疫の働きが低下し、ワクチンの効果が十分に得られない人を対象に、医師が必要だと判断した場合に使用される予定です。
厚生労働省は15万人分の在庫を確保しているということで、使用開始に向け速やかに手続きを進めたいとしています。
新型コロナBA.5 既存の抗ウイルス薬が高い効果 東大など発表(7/21)
2022年7月21日

世界的に拡大している新型コロナウイルスのオミクロン株の一種、「BA.5」に対する治療薬の効果について、東京大学などのグループが培養細胞の実験で調べたところ、現在使われている抗ウイルス薬が高い効果を示したとする結果を発表しました。
この研究は、東京大学医科学研究所の河岡義裕特任教授らのグループが、国際的な医学雑誌の「ニュー・イングランド・ジャーナル・オブ・メディシン」で発表しました。
グループは、オミクロン株の「BA.5」の実際のウイルスを培養細胞に感染させ、さまざまな治療薬を投与してウイルスの増殖がどの程度、抑えられるのかを調べました。
その結果、国内で承認されている「レムデシビル」、「ラゲブリオ」、それに「パキロビッド」の3種類の抗ウイルス薬の成分については、いずれも「BA.2」に対してよりもウイルスの増殖を抑える効果が高かったということです。
一方、抗体を使った治療薬については今回の実験では、当初のウイルスへの効果と比べると大幅に効果が下がっているものがあったということです。
河岡特任教授は「『BA.5』の病原性はまだ十分、分かっていないが、実験では日本で使える薬でも高い効果がみられたため、その点で安心ではないか」とコメントしています。
2種類のコロナ治療薬 “動物実験で耐性ウイルス出現リスク低”(6/19)
2022年6月19日
新型コロナウイルスの2種類の治療薬について東京大学などのグループは、ハムスターを使った実験の結果として、薬が効きにくくなる「耐性ウイルス」ができるリスクは低いとみられると発表しました。

この研究は東京大学医科学研究所の河岡義裕特任教授らのグループが行いました。
グループは、新型コロナで耐性ウイルスができるリスクを調べるため、免疫を働かなくした特殊なハムスターにオミクロン株のウイルスを感染させ、新型コロナの治療薬のうち、すでに使われている「ラゲブリオ」と塩野義製薬が現在、承認申請している薬の2種類をそれぞれ投与しました。
その結果、いずれの薬でも投与から2日目には肺でのウイルスの量が1万分の1になりましたが、免疫が働かないハムスターのためウイルスは完全にはなくなりませんでした。
そして9日目の時点で体内からウイルスを取り出し、再び薬が効くかどうかを調べたところ、いずれの薬も効果がみられ、耐性ウイルスは確認されなかったということです。

グループによりますと、耐性ウイルスができやすい薬の場合、数日で耐性ウイルスが確認されることもあるということで、河岡特任教授は「ヒトでも同じ結果かどうかは検証が必要だが、少なくとも動物実験の結果からは耐性ウイルスのリスクは低いとみられる」と話しています。
アストラゼネカ 事前投与のコロナ注射薬 厚生労働省に承認申請(6/9)
2022年6月9日

新型コロナウイルスに感染した人の重症化予防に加え、事前に投与することで発症を防ぐ効果が期待される注射薬について、イギリスの製薬大手、アストラゼネカが国に承認を求める申請を行ったと発表しました。
アストラゼネカは6月9日、新型コロナウイルスの働きを抑える抗体を投与する「抗体医薬」について、厚生労働省に承認を申請したと発表しました。
この薬は2種類の抗体を注射で投与することで、感染した人の重症化を防ぐとともに、感染前に投与することで発症を防ぐ効果が期待されるとしています。
承認されれば、がんの治療で免疫の働きが低下し、ワクチンの効果が十分に得られない人などの発症予防のために使えるとしています。
会社によりますと、2021年3月まで行われた感染していないおよそ5200人を対象にした治験では、発症リスクが77%抑えられ、効果が半年間続いたとしているほか、2021年7月まで行われた軽症から中等症の900人余りを対象にした治験では、発症から7日以内の投与で重症化や死亡のリスクを50%減らす効果が確認されたということです。
オミクロン株でも効果が見られたとしていて、欧米各国では感染前に使用できる薬として承認されています。
会社では今回、特例承認を希望するとしていて「薬を必要とする方々に一日も早くお届けできるよう、規制当局と緊密に連携し取り組んでまいります」としています。
イベルメクチン臨床試験 新型コロナの入院予防効果認められず(3/31)
2022年3月31日

寄生虫が原因で失明などが引き起こされる感染症の特効薬「イベルメクチン」について、新型コロナウイルスの患者に投与しても、入院に至るリスクを下げる効果はなかったとする臨床試験の結果を、ブラジルなどの研究グループが発表しました。

臨床試験の結果は、ブラジルの複数の大学などの研究グループが、国際的な医学雑誌「ニュー・イングランド・ジャーナル・オブ・メディシン」に発表しました。
研究グループは、2021年3月から8月にかけて、肥満や糖尿病、高血圧など、新型コロナの重症化リスクがある18歳以上の患者1358人について、発症から7日以内に「イベルメクチン」を一日に1回、3日間、服用するグループと偽の薬を服用するグループに分けて経過を調べました。
その結果、4週間以内に入院するか救急外来を受診した患者は「イベルメクチン」を服用したグループで14.7%、偽の薬のグループでは16.3%で、統計学的に有意な差は見られなかったということです。
また、発症から7日目での体内のウイルス量の減少や回復するまでの期間、それに死亡するリスクについても差は見られなかったとしています。
「イベルメクチン」はノーベル医学・生理学賞を受賞した北里大学の大村智特別栄誉教授の研究を元に開発された、寄生虫によって失明やリンパ管の腫れが引き起こされる病気の特効薬で、各国で新型コロナ患者に対する有効性や安全性についての研究が進められてきました。
今回の臨床試験は、患者も、投与する医師の側も「イベルメクチン」か偽の薬か分からない客観性が高い方法で行われていて、研究グループは「イベルメクチン」は新型コロナの発症後すぐに投与しても、症状が悪化して入院に至るリスクを下げる効果が認められなかったとしています。
WHO「血しょう治療」推奨せず 死亡率低下の証拠見つからず(12/7)
2021年12月7日
新型コロナウイルスに感染し、回復した人の血液の成分を患者に投与する「回復者血しょう」を使った治療について、WHO=世界保健機関は死亡率の低下などにつながる証拠が見つからなかったとして患者への投与は勧められないとする指針を公表しました。
WHOは新型コロナウイルスに感染し、回復した人の血しょうを患者に投与する「回復者血しょう治療」について世界各地の1万6236人に行った臨床試験を分析し、12月7日、治療に対する新たな指針を公表しました。
それによりますと、「回復者血しょう」の投与で▽死亡率が低下したり▽人工呼吸器を必要としなくなったりする証拠は見つからなかったとしています。
それにもかかわらず、この治療法は高額で設備の管理に時間がかかるとして、WHOは患者への投与を推奨しないとしています。
新型コロナの患者への「回復者血しょう治療」は去年から各国で研究が進められ、アメリカでは緊急の使用が許可されましたが、その後、死亡率の低下などにつながらないとする研究結果が相次いで発表されていました。
新型コロナの治療薬について、WHOは▽軽症患者などに対して2種類の薬を同時に投与する「抗体カクテル療法」、▽重症化した患者については「デキサメタゾン」のようなステロイド剤や、日本で開発された関節リウマチの治療薬「アクテムラ」などの投与を推奨しています。
抗体カクテル療法 予防目的の投与 条件付きで承認へ 厚労省(11/5)
2021年11月5日
新型コロナウイルスの軽症患者などを対象にした「抗体カクテル療法」について、厚生労働省は、発症を予防する目的での投与も条件付きで認めることになりました。
2種類の抗体を同時に点滴で投与する抗体カクテル療法は、軽症から中等症で、かつ重症化リスクがある患者を対象に2021年7月に承認されました。
日本での販売権を持つ中外製薬は、海外の治験で患者の家庭の濃厚接触者に投与した結果、感染して発症するリスクを81%減らす効果が確認できたなどとして、発症を予防する目的での投与も認めるよう追加で申請していました。
これについて11月4日夜開かれた厚生労働省の専門家部会は投与する人を、患者に濃厚接触した家族などか無症状の患者とし、かつ原則として重症化リスクがあることを条件に承認を了承しました。
ただし、感染症はワクチンで予防することが基本だとして、投与の対象はワクチンの効果が不十分と考えられる人などに限るということです。
また、点滴より短時間で済む皮下注射で投与することも了承されました。
厚生労働省は11月5日にも正式に承認することにしていて、発症を予防する目的で新型コロナウイルスの薬が承認されるのは国内で初めてです。
「抗体カクテル療法」予防目的の投与認めるか 11月4日判断へ(10/28)
2021年10月28日
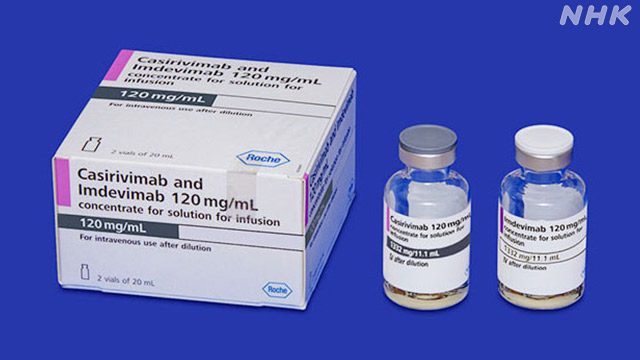
新型コロナウイルスの軽症患者などを対象にした「抗体カクテル療法」について、厚生労働省は、感染と発症を予防する目的で投与することなども認めるか、11月4日に判断することを決めました。
2種類の抗体を同時に点滴で投与する抗体カクテル療法は、軽症から中等症の患者で、かつ重症化リスクがある人が対象で、厚生労働省によりますと、10月20日までに全国で合わせておよそ3万6000人が投与を受けたと見られています。
日本での販売権を持つ中外製薬は▽感染と発症を予防するための投与や▽無症状の患者への投与も新たに認めるよう申請していて、厚生労働省は、11月4日に専門家部会を開いて承認するかどうか判断することを決めました。
中外製薬によりますと、海外の治験では▽家庭内の濃厚接触者に予防目的で投与したところ、感染して発症するリスクが81%減少し、▽無症状の患者でも発症するリスクを31%減らす効果が確認されたということです。
また、現在は点滴での投与に30分程度かかることなどから、より短時間で投与できる皮下注射も認めるよう申請しています。
予防目的での投与や無症状の患者への投与が認められれば、新型コロナウイルスの薬としては初めてで、専門家部会が承認を了承すれば、厚生労働省が数日以内に承認する見通しです。
「抗体カクテル療法」約3万5000人が投与か 厚労省(10/7)
2021年10月7日
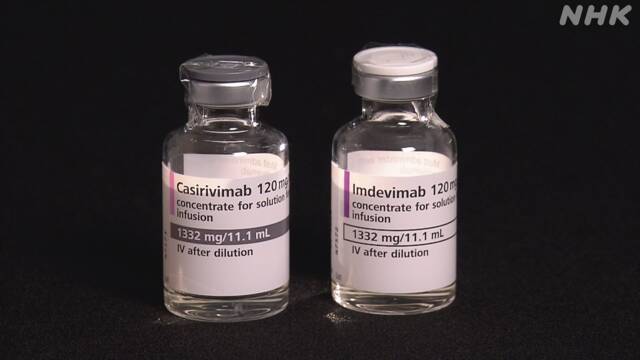
新型コロナウイルスの軽症患者などを対象にした「抗体カクテル療法」について、厚生労働省は5日までに全国でおよそ3万5000人が投与を受けたと見られると発表しました。2種類の抗体を同時に点滴で投与する「抗体カクテル療法」は、軽症患者にも使用できる初めての治療薬として、2021年7月に承認されました。
当初、対象は入院患者に限定されていましたが、現在は宿泊療養施設のほか、外来や往診での使用も条件付きで認められています。
厚生労働省は、6日開いた専門家会合で、10月5日までに全国のおよそ2100か所の医療機関に納品され、合わせておよそ3万5000人が投与を受けたと見られると報告しました。
また、同じく抗体を使った薬で、軽症患者に使用できる2種類目の治療薬として先月27日に承認された「ソトロビマブ」も、10月5日までにおよそ20か所の医療機関に納品され、およそ40人に投与されたと見られるということです。
ソトロビマブは、現在、投与の対象が入院患者に限定されていますが、厚生労働省はできるだけ速やかに対象を拡大していく予定だとしています。
軽症患者に使用できる2種類目の治療薬「ソトロビマブ」承認(9/28)
2021年9月28日

抗体を投与することで新型コロナウイルスの働きを抑える新たな治療薬が、9月27日夜、国内で承認されました。
軽症患者に使用できる薬としては抗体カクテル療法に続いて2種類目となります。

承認されたのは、イギリスの製薬大手グラクソ・スミスクラインが、厚生労働省に承認申請をしている「ソトロビマブ」です。
対象となるのは、重症化のリスクが高く、かつ酸素の投与が必要ない軽症または中等症の患者で、新型コロナウイルスの働きを抑える「中和抗体」を点滴で投与します。
海外で行われた治験では、入院や死亡のリスクを79%減らす効果が確認されたということで、アメリカでは2021年5月に緊急使用の許可が出ています。
厚生労働省の専門家部会で9月27日、承認の可否が審査され、有効性や安全性が認められるとして、国内での承認が了承されました。
これを受け、厚生労働省は、9月27日夜、正式に承認しました。
軽症患者にも使用できる薬としては抗体カクテル療法に続いて2種類目となり、より多くの患者の重症化の予防につながることが期待されます。
一方、アナフィラキシーや呼吸困難などの副作用が起きるおそれもあることから、厚生労働省はまずは対象を入院患者に限定したうえで、抗体カクテル療法と同様に外来や往診での投与を認めるか検討していくことにしています。
「ソトロビマブ」とは
ソトロビマブは、すでに承認されている抗体カクテル療法と同じ、「中和抗体薬」と呼ばれる治療薬です。
開発したグラクソ・スミスクラインによりますと、1057人を対象に海外で行われた治験では、入院や死亡のリスクを79%減らす効果が確認されました。
また、投与から24時間以内に、発熱や呼吸困難、悪寒、めまい、発疹などの症状が確認されたほか、1人がアナフィラキシーを起こしたということです。
グラクソ・スミスクラインは、臨床データが限られているため、今後、報告されていない重篤な症状があらわれる可能性もあるとしています。
新型コロナウイルスの治療薬の承認は、レムデシビルとデキサメタゾン、バリシチニブ、それに抗体カクテル療法のカシリビマブとイムデビマブに続いて5種類目となります。
厚生労働省は、供給量の見通しや金額を明らかにしておらず、医療機関から投与する患者の数などを報告してもらったうえで、必要な量を供給することにしています。
田村厚生労働相「新たな治療の選択肢 期待している」
田村厚生労働大臣は9月27日夜、厚生労働省で記者団に対し「新型コロナウイルスに対する新たな治療の選択肢なので期待している。適切に供給されるように、政府でしっかり確保し、必要な医療機関に配送したい」と述べました。
そのうえで、投与の対象について「特例承認をしたばかりなので、副反応が出ても対応できるかなど、しっかり見ていかなければならない。当面は、入院が前提になるが、早い時期に安全性が確認できれば、最終的には往診でも使えるようにしたい」と述べました。
専門家「複数の薬で安定供給できれば重症化予防に」
感染症対策に詳しい国際医療福祉大学の松本哲哉教授は、今回承認された治療薬は、抗体カクテル療法と期待される効果や使い方は同じだとしたうえで「薬の供給量には限界があり、今後もし、感染の急拡大で患者が増えた場合に1つの薬だけでは不足するおそれもある。複数の抗体薬が使えるようになることは医療現場にとって重要だ。複数の薬によって安定的な供給ができれば、必要な人に必要な治療が届き、より多くの人の重症化予防につながるだろう」と話しています。
WHO 軽症患者向け「抗体カクテル療法」を初めて推奨(9/24)
2021年9月16日
WHO=世界保健機関は、新型コロナウイルスの治療薬で軽症患者などに対して2種類の薬を同時に投与する「抗体カクテル療法」を初めて推奨しました。
WHOは9月24日、新型コロナウイルスの治療薬に関する手引きを更新しました。
それによりますと、抗体でできた2種類の薬「カシリビマブ」と「イムデビマブ」を投与する「抗体カクテル療法」という治療法について、臨床試験の結果、一般的な治療を行った場合に比べ重症化して入院するリスクや回復までにかかる期間が減少したとしています。
そのうえで、これらの薬を軽症患者などの治療に推奨するとしています。
WHOはこれまで重症患者に対して別の治療薬を推奨していますが、軽症患者など向けに推奨するのは今回が初めてです。
日本では同じ薬を使った「抗体カクテル療法」が2021年7月、軽症の患者に使用できるとしてすでに承認されています。
ただ、これらの薬は高額なうえ、供給量が限られているため、感染拡大が深刻な途上国にどう供給するかが課題になっていて、WHOは薬を製造している企業に対し寄付を求めるなどの交渉を進めているとしています。
「抗体カクテル療法」 往診での使用は慎重に検討 厚生労働省(9/16)
2021年9月16日
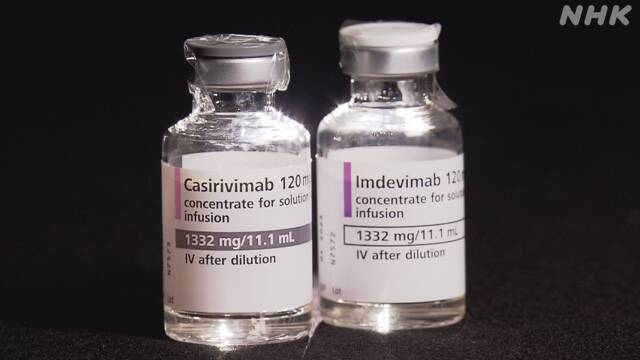
新型コロナウイルスの軽症患者などに使用できる「抗体カクテル療法」について、厚生労働省は菅総理大臣の指示を受けて往診での使用を認めるか検討を始めました。
一方、まれに副作用が疑われる重篤な症状も報告されていることから、一部の医療機関で試験的に導入し、安全性を確保できるか慎重に見極めた上で判断する方針です。
抗体でできた2種類の薬を同時に点滴で投与する「抗体カクテル療法」は、軽症患者にも使用できる初めての治療薬として、7月に承認されました。
当初は、入院患者だけが対象でしたが、8月以降、宿泊療養施設などに加え、外来での使用も条件付きで認められています。
菅総理大臣は、往診での使用も可能とするよう田村厚生労働大臣に検討を指示し、厚生労働省が具体的な検討に入りましたが、課題となるのが安全性の確保です。
厚生労働省などによりますと、8月21日までに推定で5800人余りが投与を受け、0.46%にあたる27人で▽発熱や▽酸素飽和度の低下、▽狭心症など副作用が疑われる重篤な症状が報告されています。
厚生労働省は、現在、投与から24時間は患者の容体が悪化しても把握できることなどを使用の条件にしていますが、医療関係者からは往診で使用した場合、特に1人暮らしの患者などは把握できないおそれがあると指摘されています。
このため一部の医療機関の往診で試験的に導入し、課題を検証した上で全国的に使用を認めるか判断する方針で、近く要件を示すことにしています。
厚生労働省は、「臨床データが限られていて、新しい症状が報告される可能性も否定できない。結論ありきで考えず、往診でも安全性を確保できるか慎重に見極めた上で使用の可否を判断したい」としています。
投与を受けた1.35%の79人で副作用が疑われる症状
厚生労働省や、関係企業とライセンス契約を結んでいる中外製薬によりますと、2021年7月22日から8月21日までのおよそ1か月間に投与を受けたと推定される5871人のうち、1.35%に当たる79人で副作用が疑われる症状が報告されました。
このうち重篤だったのは27人で、
▽発熱が5人、
▽酸素飽和度の低下が4人、
▽悪寒が2人、
▽狭心症やおう吐、血圧の低下や上昇などがそれぞれ1人となっています。
いずれの症状も投与との因果関係は分かっていないということで、厚生労働省などが引き続き情報収集を進めています。
複数の課題も
新型コロナウイルスに感染し自宅で療養する人の往診を行っている、東京 品川区の「心越クリニック」の岩間洋亮院長は、「抗体カクテル療法」を往診でも使用することについて「患者の重症化を防ぐ手段が増えるのは望ましいことだ」としたうえで、複数の課題があると指摘します。
患者がアレルギーを発症した場合に家族がすぐに気付けるかという懸念や、1人暮らしで見守る人がいないケースも考えられるとして、「訪問看護やヘルパーなどと連携し、経過を丁寧に見守る体制を構築する必要があるが、実現は簡単ではないだろう」としています。
また「抗体カクテル療法に使う薬は1つの瓶に2人分入っているものが主に流通していて、開封後は48時間以内に使い切らなければならない。薬は高価なので、廃棄せずにむだなく使えるよう医師の間で患者を調整するような体制も必要だ」と話していました。
医師「前向きに捉え 歓迎」
東京 大田区などで自宅療養者の往診を行ってきた「ひなた在宅クリニック山王」の田代和馬院長は「在宅でできる治療は限られていたので、効果的な選択肢が加わるという意味では前向きに捉え、歓迎している」と話しています。
そのうえで、「2つの抗体を混ぜるなど投与前の準備に時間がかかり、投与後も副作用が出ていないか経過観察をしなければならないことを考えると、1日に対応できる患者の数は限られる。病院の空き病床などを活用して複数の患者にスムーズに抗体カクテル療法を行える体制を充実させ、状況に応じて一部、在宅でも対応すれば重症化する人を減らせるのではないかと思う。今のうちから『第6波』に備えてあらゆる機関が連携して抜本的な対策を整えていく必要がある」と話していました。
医師「適正に使用するためのルールづくりも必要」
自宅療養者の往診を行っている医師のグループ「ファストドクター」の代表、菊池亮医師は「病院や宿泊療養施設といった十分な体制があるところで投与することが前提だ。ただ、入院調整に時間がかかり適切な時期に投与できないケースもあり、在宅でも対応できる体制作りは必要だと思う」と話しています。
そして、菊池医師は、往診の際に抗体カクテル療法が必要だと思った患者がいても、病床がひっ迫して入院できない状況では、治療の選択肢として患者に提案できなかったとしたうえで、「投与の選択肢がせばまってしまうことで、治療が受けられない患者が出てしまうことはよくないと感じていた」としています。
その上で「リスクの高い患者を重症化させないために有効性が高いが、使用経験の浅い薬なので、往診で使用する場合に副作用への対策をどう講じていくかなど、適正に使用するためのルールづくりも必要だ」と指摘しています。
酸素投与と抗体カクテル療法 同時に可能な施設を全国に 菅首相(9/16)
2021年9月16日

新型コロナウイルス対策で、菅総理大臣は、東京都が新たに設ける「酸素ステーション」を視察したあと記者団に対し、酸素の投与と「抗体カクテル療法」を同時に行える施設は画期的だとして、全国に設置できるよう支援していく考えを示しました。
菅総理大臣は、9月16日午前、東京都の小池知事とともに、都が中央区の築地市場の跡地に新たに設ける、自宅で療養している人を一時的に受け入れて酸素投与を行う「酸素ステーション」を視察しました。
このあと菅総理大臣は記者団に対し「この施設は酸素の投与と、重症化の防止に極めて高い効果のある『抗体カクテル療法』の2つのことができる。患者の皆さんにとって、これほど心強いものはなく画期的な施設だ」と述べました。
そのうえで「こうした施設を全国に増やしていきたい。政府は、しっかりと応援をさせていただいて、1人でも多くの命を救いたい」と述べ、全国に設置できるよう支援していく考えを示しました。
そして、菅総理大臣は、施設の廊下の壁に「皆様のご尽力に感謝」ということばと、みずからの名前をペンでしたため、施設をあとにしました。
小池知事「国と連携し難局を乗り越えていきたい」
東京都の小池知事は、築地市場の跡地に設ける酸素投与と抗体カクテル療法を行う施設を菅総理大臣と視察したあと、記者団に対して「新規の陽性者は若干、抑えられてはいるが、それでも1000人近い新規陽性者の数字が上がっている。このあいだまでオリンピック・パラリンピックの車両基地があったこの場で抗体カクテル療法を早めに受けることによって重症化が防げる。国と都が連携することで、コロナ対策をしっかり進めていき、この難局をともに乗り越えていきたい」と述べました。
「抗体カクテル療法」往診使用 “一部医療機関先行で“厚労相(9/16)
2021年9月16日

新型コロナウイルスの感染者への治療法で、入院や外来などに限られている「抗体カクテル療法」について、田村厚生労働大臣は自宅への往診でも使用できるよう、近く、一部の医療機関で先行して行ったうえで、全国展開したいという考えを示しました。
「抗体カクテル療法」は、入院や外来診療のほか、宿泊療養でも認められていますが、菅総理大臣は9月15日、往診でも可能とするよう、田村厚生労働大臣に検討を指示したことを明らかにしました。
田村大臣は、参議院厚生労働委員会の閉会中審査で「宿泊療養施設には24時間誰かがいるので、副作用があっても対応できるが、自宅となると、健康が悪化する可能性があるので、すぐに対応できる体制を組まなければならない」と指摘しました。
そのうえで「まずは早急に、モデル的にいくつかの医療機関で対応し、課題点や問題点を抽出したうえで、全国展開していきたい。近いうちにスタートしたい」と述べました。
一方、政府の分科会の尾身会長は、新型コロナへの対応をめぐり「日本の地域医療計画は、感染症に対してどうするかという発想がなかった。日本の医療体系そのものをもう一度見直す機会であり、この経験を生かして、根本的な見直しが必要だ」と述べました。
分科会 尾身会長「行動制限緩和は感染が落ち着いた後に」
また、尾身会長は、行動制限の緩和について「11月ごろになると、多くの希望者にワクチンが届くので、どういうことが可能になるか目安を示すことは国の役割だ。しかし、そのことと緊急事態宣言を発令している中で、実際に行動制限を緩めることは全く別だ。ヨーロッパの状況を見ると、ワクチン接種がかなり進んでも、行動制限を緩めると感染拡大することが分かっている」と述べました。
そのうえで「ワクチンには感染予防効果がかなりあるが、完璧ではなく、ワクチンが普及しても感染予防対策をしっかり続けないと、必ずリバウンドが起こる。行動制限を緩和するのは、感染が落ち着いた後に、じっくり徐々にすると、政府が、国民にメッセージを伝えてほしい」と述べました。
酸素濃縮装置 国が都道府県に貸し出しへ コロナ患者に酸素投与(9/16)
2021年9月16日
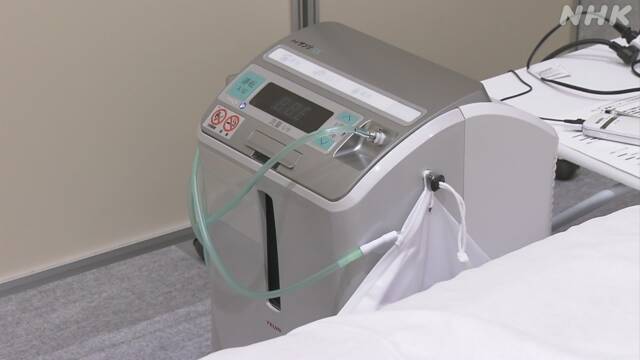
新型コロナウイルスの患者に酸素の投与を行うための「酸素濃縮装置」が不足する中、厚生労働省は毎月、最大500台を確保し、都道府県に貸し出すことになりました。
酸素濃縮装置は鼻や口からチューブで酸素を吸入するもので、自宅で療養中の人や一時的な受け入れ施設で入院を待っている患者に使われていますが、感染の拡大が続いたことから、全国的に不足しています。
こうした中、厚生労働省はメーカーと調整して9月から毎月、最大500台を確保し、都道府県に無料で貸し出すことになりました。
当面は、緊急事態宣言やまん延防止等重点措置の対象地域となっている都道府県が、患者を一時的に受け入れる入院待機ステーションや酸素投与を行う宿泊療養施設を新たに整備する場合に必要な台数を貸し出す方針です。
また、自宅で療養中の患者を医師が往診する際などに必要となる分については、10月以降、貸し出しを始めます。
厚生労働省は「今後の感染拡大に備えて酸素濃縮装置が必要な人や地域に行き渡るようにしたい。メーカーにも増産を要請している」としています。
「抗体カクテル療法」外来患者への日帰り投与始まる 長野 松本(9/14)
2021年9月14日
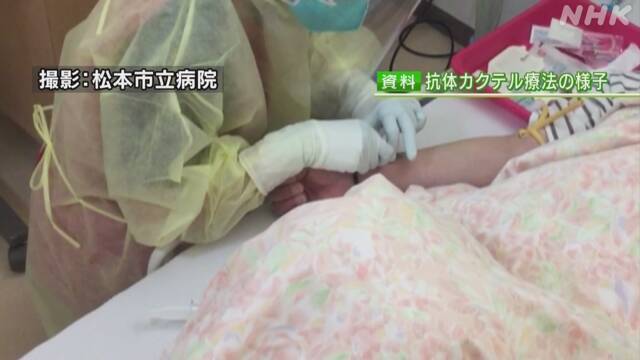
長野県の松本市立病院で新型コロナウイルスの軽症患者などの治療に使われる「抗体カクテル療法」の外来患者に対する日帰りでの投与が始まりました。
「抗体カクテル療法」は、新型コロナの軽症から中等症の患者を対象にした治療法で、2種類の抗体を混ぜ合わせて点滴で投与します。
松本市立病院では、当初は入院患者だけを対象に行っていましたが、9月13日からは宿泊施設などで療養する人に日帰りでの投与を始めました。
対象は、おおむね50歳以上の人や基礎疾患など重症化のリスクがある患者で、30分かけて点滴を行い、その後、経過観察のため2時間ほど待機してもらいます。
病院では、1日に最大6人まで対応できる体制を整えていて、日帰り投与の導入で、病床の不足を防ぐことができるほか、入院の負担がなくなるなど患者にもメリットがあるということです。
県によりますと、県内では30の医療機関が「抗体カクテル療法」に使う薬を備蓄し、入院患者を中心に投与していますが、外来患者への投与は県内では初めてとみられるということです。
松本市立病院の中村雅彦院長は「重症化リスクのある人を早めに『抗体カクテル療法』で治療することで、重症化を防いでいきたい」と話しています。
新型コロナ 抗体カクテル療法で患者の95%の症状改善 都が調査(9/9)
2021年9月9日
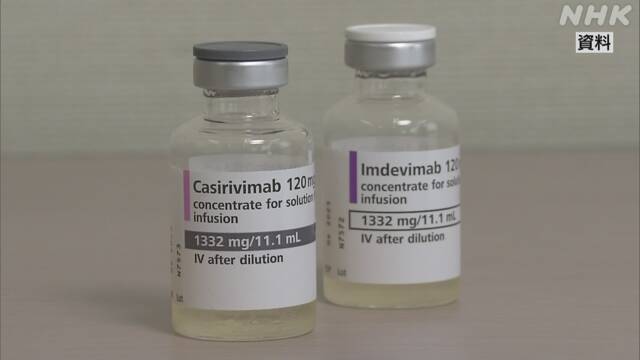
都内の医療機関で新型コロナウイルスの患者に行われている、抗体カクテル療法で、95%の患者の症状が改善したことが、都のモニタリング会議で報告されました。

東京都は116の医療機関で抗体カクテル療法を受けた420人を調査しました。
その結果、95%余りにあたる400人は症状が改善したということです。
一方、投与を受けた60代の基礎疾患のある男性はその後、亡くなりました。
また、投与のあとも症状が改善せず入院を続けている人は19人で、このうち18人は50代以上でした。
発症から投与までの期間をみると、改善した患者の56%余りは4日以内、改善しなかった患者の63%余りは5日以降で、専門家は早期の治療で効果が出る傾向があると説明しています。
「抗体カクテル」外来診療でも投与へ 期待と課題(8/26)
2021年8月26日
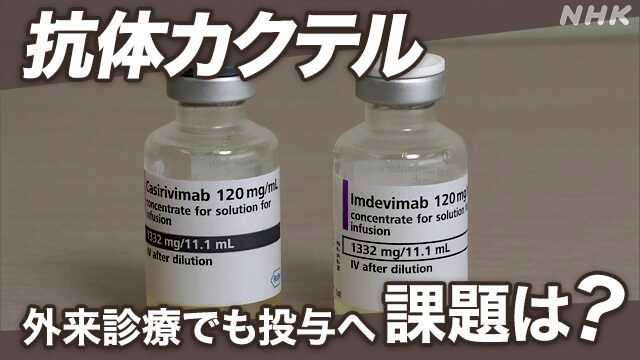
新型コロナウイルスの軽症患者などに使用できる「抗体カクテル療法」の治療薬について、薬を販売する「中外製薬」は8月26日、説明会を開き、政府が新たに容認した外来診療での投与に対応するためにも、必要な供給量を確保する考えを示しました。

「抗体カクテル療法」は、2種類の抗体を混ぜ合わせて点滴で投与し、新型コロナウイルスの働きを抑えるもので、7月、日本で承認され、軽症から中等症の患者を対象に医療機関や宿泊療養施設での投与が始まっています。
この治療薬を国内で販売している中外製薬が8月26日、報道機関などを対象にした説明会を電話会議形式で開きました。
この中で奥田修社長は、「デルタ株がまん延し、治療薬の需要が世界的に高まっているが、日本政府からの要請に応じて、必要な供給量を確保したい」と述べ、政府が新たに容認した外来診療での投与に対応するためにも必要な量を確保する考えを示しました。
説明会には、新型コロナウイルス対策にあたる政府の分科会のメンバーで、東邦大学の舘田一博教授も出席し、「軽症から、中等症、重症に向けての薬の選択肢が増えれば、大きな前進になるだろう」と述べました。
抗体カクテル療法 “軽症者の重症化を防ぐ”
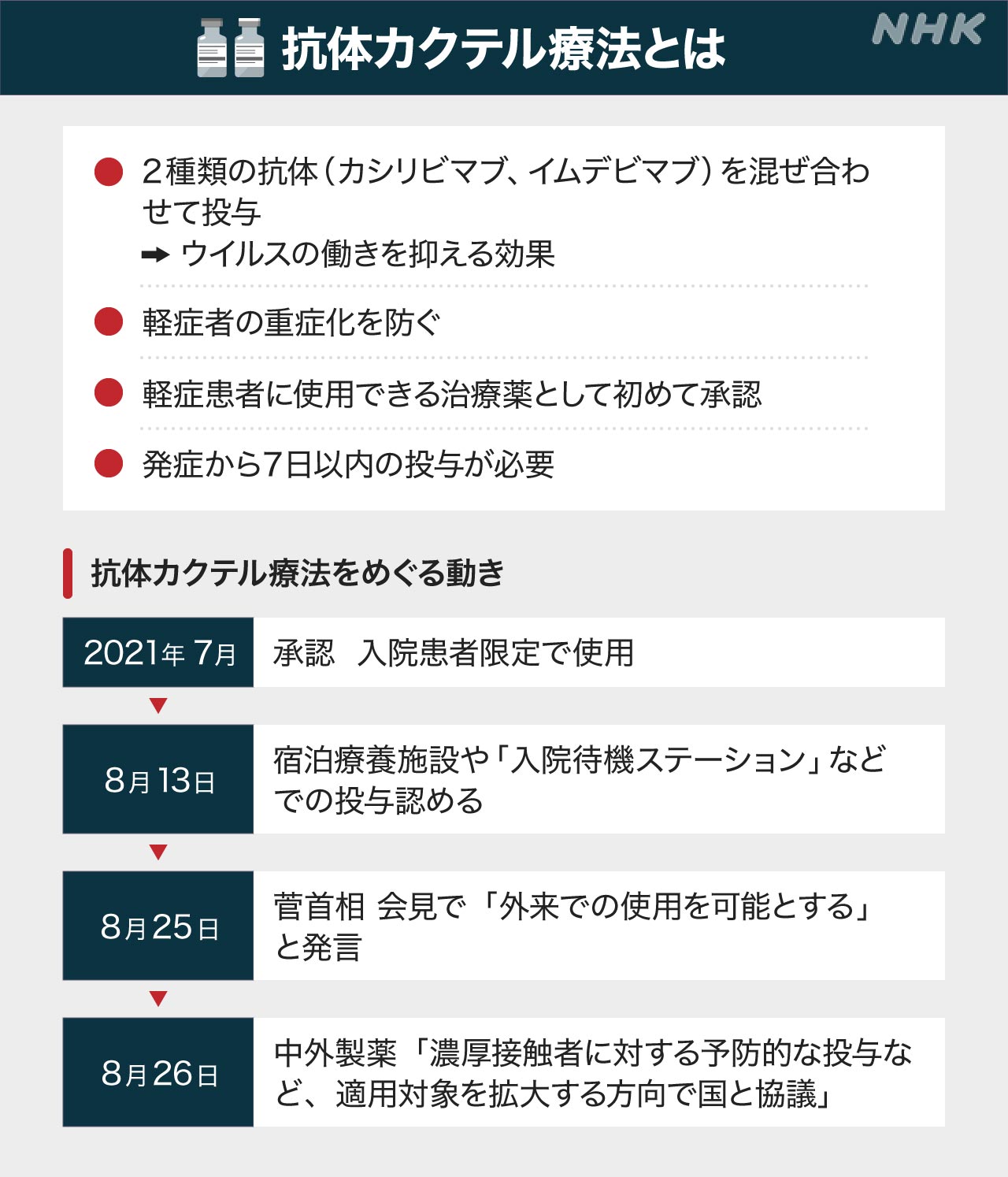
「抗体カクテル療法」は、2021年7月に承認されました。
「カシリビマブ」と「イムデビマブ」の2種類の抗体を混ぜ合わせて投与することで、新型コロナウイルスの働きを抑える効果があり、軽症の人の重症化を防ぐことを目的に、初めて軽症患者に使用できる治療薬として承認されました。
発症から8日目以降に投与を開始した場合の有効性を裏付けるデータがないことから7日以内の投与が必要ですが、海外で行われた臨床試験では、入院や死亡のリスクをおよそ70%減らす効果が確認されています。
アメリカのFDA=食品医薬品局が、2020年11月に症状が悪化するリスクの高い患者に一定の効果がみられるとして緊急の使用許可を出し、その前の2020年10月にアメリカのトランプ前大統領が新型コロナウイルスに感染して入院した際にも使われました。
対象を徐々に拡大 “十分に観察できる体制”が条件
厚生労働省は十分な観察が必要だとして、当初、入院患者に限って使用を認めていましたが、感染の急拡大で、入院できない患者が増えたことから、8月13日、十分に観察できる体制が整っていることを条件に、▽宿泊療養施設や、▽臨時の医療施設として設置された「入院待機ステーション」などで投与することを認めました。
さらに菅総理大臣は、8月25日の記者会見で外来診療でも投与を容認すると述べました。

(菅総理大臣)
「中和抗体薬は、すでに1400の医療機関で1万人に投与され『重症化を防ぐ極めて高い効果が出ている』という声が現場から寄せられている。これまで対象は入院患者のみとされてきたが、入院せずとも使うことが出来るよう、外来で使うことも可能とする。必要な数量はしっかりと確保している。今後とも50代以上の人や基礎疾患がある人を対象として集中的に使用し、重症化を防いでいく」
中外製薬 「適用対象の拡大」 申請する方向で国と協議

また、中外製薬の奥田社長は8月26日の記者会見で、濃厚接触者に対する予防的な投与など、適用対象の拡大についても今後、申請する方向で国と協議していることを明らかにしました。
コロナ治療薬 国内では4つが承認

日本国内では、これまでに新型コロナの治療薬として4つの薬が承認されています。
1. レムデシビル
新型コロナウイルスの治療薬として、最も早く2020年5月に特例承認されました。
もともとはエボラ出血熱の治療薬として開発が進められた薬で、点滴で投与されます。
当初、対象となる患者は、人工呼吸器や人工心肺装置=ECMOをつけている重症患者などに限定されていましたが、2021年1月からは肺炎になった中等症の患者にも投与が認められています。
2. デキサメタゾン
2020年7月に厚生労働省が治療薬として推奨しました。
もともとは、重度の肺炎やリウマチなどの治療に使われてきた炎症やアレルギーを抑える作用のあるステロイド剤「デキサメタゾン」で、イギリスで行われた臨床試験で、重症者の死亡を減らす効果が確認されました。
国内では、抗ウイルス薬のレムデシビルとデキサメタゾンを併用する治療が広く行われていて、2020年春の感染の第1波と比べて、その後の感染拡大で致死率が大きく下がった要因の1つになったと考えられています。
3. バリシチニブ
関節リウマチなどの薬で炎症を抑える効果がある薬で、2021年4月に承認されました。
この薬は錠剤で、酸素投与が必要な中等症以上の入院患者に対して、レムデシビルと併用して服用することが条件となっています。
国際的な臨床試験で「バリシチニブ」と「レムデシビル」を併用すると、「レムデシビル」を単独で投与する場合に比べて患者が平均で1日早く回復したということです。
4. 抗体カクテル療法
2021年7月に承認されました。
「カシリビマブ」と「イムデビマブ」2種類の抗体を混ぜ合わせて、点滴で投与することで、新型コロナウイルスの働きを抑える効果があり、初めて軽症患者に使用できる治療薬として承認されました。
課題は体制の確保
【重症化する前に投与を】
軽症者の重症化を防ぐことが目的の治療で、さらに発症から8日目以降に投与を開始した場合の有効性を裏付けるデータがないことから7日以内の投与が必要です。しかし、感染の拡大にともなって、現在、入院患者の多くが中等症か重症となっているなど、すでに投与の時期を過ぎているケースがあると指摘されています。このため、より症状が軽い人に投与できるよう対象を徐々に拡大してきました。
【投与には副作用に備えた体制が必要】
海外で行われた治験では、投与を受けた4206人のうちの10人に発熱や呼吸困難、酸素飽和度低下、悪寒、不整脈などの症状が見られたということです。
また、アナフィラキシーと呼ばれる重いアレルギー反応も報告されています。いずれも容体は回復したということですが、製薬会社は投与が終わってから少なくとも1時間は状態を観察するよう求めていて、厚生労働省は24時間は健康観察を十分にできる体制を確保するよう求めています。
また専門家は、日本人特有の副作用が出ないかどうかは慎重に見極めるべきだと指摘しています。
【体制の確保は】
“24時間の十分な健康観察”のためには夜間も含めた体制の確保が必要になります。重症患者数が過去最多を更新するなど医療体制がひっ迫する中、いかに体制を確保するかが課題となります。

「抗体カクテル療法」の外来診療での投与を認める方向で調整へ(8/25)
2021年8月25日
新型コロナウイルスに感染した入院患者などに行われている「抗体カクテル療法」をめぐり、厚生労働省は、自宅療養者への対応を進めるため、一定の条件を満たした医療機関では、外来診療による日帰りでの投与も認める方向で調整を進めることになりました。
「抗体カクテル療法」は、2つの薬を同時に点滴投与することで、抗体が作用してウイルスの働きを抑える治療法で、重症化リスクがある軽症から中等症の患者を対象に入院患者のほか、宿泊療養施設や臨時の医療施設での投与が認められています。
厚生労働省は、感染が急拡大し、自宅療養者が増加していることを踏まえ、投与後の患者の容体の変化に対応できる入院設備などが整った医療機関に限って、外来診療による日帰りでの投与も認める方向で調整を進めることになりました。
厚生労働省は、患者の移動手段の確保など、具体的な運用方法について検討を急ぎ、速やかに実施したい考えです。
ただ、医師が患者の自宅を訪れる「往診」での投与は、薬の副作用などの経過観察が難しいとして、引き続き、認めない方針です。
一方、立憲民主党は、できるだけ多くの患者が使えるよう自宅での投与も可能にすべきだとして、そのための条件や体制の検討を政府に求めることにしています。
効くのか?効かないのか? イベルメクチン コロナ治療に効果は…”(8/23)
2021年8月23日

寄生虫が原因で失明などが引き起こされる感染症の特効薬「イベルメクチン」。新型コロナウイルスの患者にも有効な可能性があるとする情報が東京都医師会の会長や一部の医師などから出されています。 しかし各国の保健当局やWHO=世界保健機関、メーカーなどは、これまでのところ臨床試験で有効性は明確に示されていないとしています。「イベルメクチン」をめぐる最新の情報をまとめました。
イベルメクチンとは?

イベルメクチンは、ノーベル医学・生理学賞を受賞した北里大学の大村智特別栄誉教授の研究をもとに開発された飲み薬で、寄生虫によって失明やリンパ管の腫れが引き起こされる病気の特効薬として、アフリカ諸国を中心に世界中で使われています。
日本国内では皮膚に激しいかゆみが出る「疥癬(かいせん)」などの治療薬として承認されていて、細胞を使った実験で2020年、新型コロナウイルスの増殖を抑える効果があるとする結果が出されたことから、患者に対する有効性や安全性について各国で研究が進められています。
日本 コロナ治療薬で承認されず 臨床試験で有効性など調査

イベルメクチンは、南米の一部の国などで新型コロナに対する治療薬として認めているところもありますが、日本国内では新型コロナの治療薬としては承認されておらず、北里大学の学校法人「北里研究所」が2020年9月から、北里大学病院などで血液中の酸素の値が95%以上の軽症から中等症の一部の患者を対象に医師主導の臨床試験を行って有効性や安全性を調べています。
当初の計画では2021年3月末までに240人を対象にした臨床試験を終えるとしていましたが、北里研究所によりますと、相次ぐ感染拡大で各病院では症状が重い患者の治療を優先せざるをえない状況が続き、2021年6月の時点で参加した患者は半数程度にとどまっているということです。
海外 有効性は十分証明されず研究続く
また、海外でもさまざまな研究結果が報告されてきましたが有効性は十分証明されておらず、研究が続いています。
米・NIH“コロナに有効か結論出せない”

アメリカのNIH=国立衛生研究所は2021年2月、イベルメクチンはウイルス性の感染症の治療薬としては承認されておらず、新型コロナの治療について報告された研究のほとんどは対象の患者の数が少なかったり、患者の重症度が明確ではなかったりするなど情報が不完全で、新型コロナに有効かどうか結論が出せないとしています。
米・製薬大手メルク「治療効果 十分な科学的根拠はない」

また、イベルメクチンを製造するアメリカの製薬大手「メルク」も2月「新型コロナウイルスへの治療効果について十分な科学的根拠はない」とする声明を出しています。
WHO 科学的根拠があるか「極めて不確実だ」

さらにWHOは3月、合わせて2407人が参加した16の臨床試験の結果を分析した結果、新型コロナ患者で死亡率の低下や回復を早める科学的根拠があるかどうかは「極めて不確実だ」と指摘していて、イベルメクチンの投与は臨床試験に限るよう推奨しています。
厚労省「有効性や安全性が確立していないことに留意」

そして、国内でも厚生労働省が2021年7月末に改訂した医療機関向けの「診療の手引き」では「軽症患者における全死亡や入院期間、ウイルス消失時間を改善させなかったと報告されている」として、新型コロナの治療として「有効性や安全性が確立していないことに留意する」とした薬剤の中に位置づけています。
一方、イベルメクチンについて製薬会社が添付している文書によりますと、副作用として肝機能障害などが報告されているほか、高齢者や妊娠中の女性への投与の安全性は確立していないとしています。
米・FDA 用量の多いイベルメクチンの服用「本気でやめて」

アメリカのFDA=食品医薬品局は3月、ウェブサイトで用量の多い動物用のイベルメクチンについて「自己判断で服用して入院した患者がいる」としたうえで「大量に摂取しても大丈夫と聞いたかもしれないが、間違いで非常に危険だ。吐き気や下痢、けいれんなど深刻な被害を引き起こす可能性があるだけでなく、死に至ることもある」と注意を呼びかけたほか、8月にもツイッターで「あなたは馬じゃない、牛でもない、本気で皆さんやめてください」と個人での服用をやめるよう呼びかけています。
コロナ治療薬 国内では4つが承認
日本国内では、これまでに新型コロナの治療薬として4つの薬が承認されています。
1. レムデシビル
このうち、新型コロナウイルスの治療薬として最も早く2020年5月に特例承認されたのが抗ウイルス薬の「レムデシビル」です。もともとはエボラ出血熱の治療薬として開発が進められた薬で、点滴で投与されます。
当初、対象となる患者は
▽人工呼吸器や
▽人工心肺装置=ECMOをつけている重症患者などに限定されていましたが
2021年1月からは肺炎になった中等症の患者にも投与が認められています。
2. デキサメタゾン
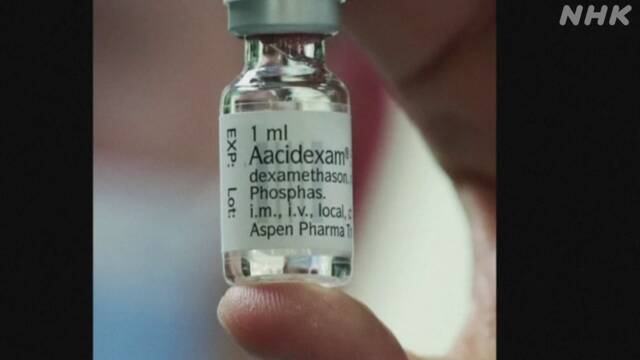
続いて、2020年7月に厚生労働省が治療薬として推奨したのが、もともとは重度の肺炎やリウマチなどの治療に使われてきた炎症やアレルギーを抑える作用のあるステロイド剤「デキサメタゾン」です。
この薬は、イギリスで行われた臨床試験で重症者の死亡を減らす効果が確認されました。
国内では抗ウイルス薬のレムデシビルとデキサメタゾンを併用する治療が広く行われていて、2020年春の感染の第1波と比べて、その後の感染拡大で致死率が大きく下がった要因の1つになったと考えられています。
3. バリシチニブ

2021年4月には、関節リウマチなどの薬で炎症を抑える効果がある薬「バリシチニブ」が治療薬として承認されました。
この薬は錠剤で、酸素投与が必要な中等症以上の入院患者に対してレムデシビルと併用して服用することが条件となっています。
国際的な臨床試験で「バリシチニブ」と「レムデシビル」を併用すると「レムデシビル」を単独で投与する場合に比べて患者が平均で1日早く回復したということです。
4. 抗体カクテル療法
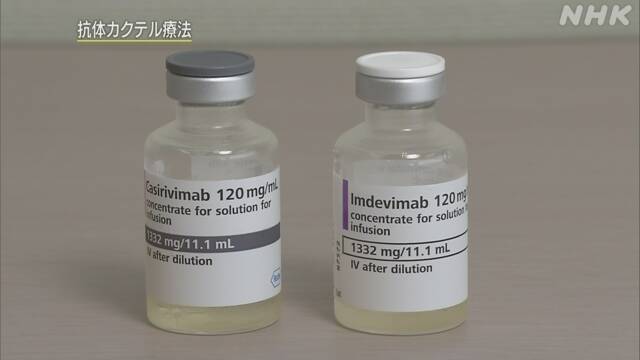
そして、2021年7月に承認されたのが「抗体カクテル療法」です。
「カシリビマブ」と「イムデビマブ」2種類の抗体を混ぜ合わせて点滴で投与することで新型コロナウイルスの働きを抑える効果があり、初めて軽症患者に使用できる治療薬として承認されました。
発症してから早期に投与する必要がありますが、海外で行われた臨床試験では入院や死亡のリスクをおよそ70%減らす効果が確認されています。

アメリカのFDA=食品医薬品局が2020年11月に症状が悪化するリスクの高い患者に一定の効果がみられるとして緊急の使用許可を出し、その前の2020年10月にアメリカのトランプ前大統領が新型コロナウイルスに感染して入院した際にも使われました。
厚生労働省は医師による観察が必要だとして当初、入院患者に限って使用を認めていましたが、感染の急拡大で入院できない患者が増えたことから8月13日、十分に観察できる体制が整っていることを条件に
▽宿泊療養施設や
▽臨時の医療施設として設置された「入院待機ステーション」などで
投与することを認めました。
この薬について、新型コロナウイルスの治療に詳しい愛知医科大学の森島恒雄客員教授は「投与後に医師による観察が必要なので自宅療養中の患者に投与するのは難しい。一度に大勢の患者が受けられるよう、休止している図書館や体育館などの施設も活用して、この非常事態を乗り切っていくことが必要だ」と話しています。
臨床試験や臨床研究中の薬
このほか、日本国内では
▽関節リウマチの薬「アクテムラ」や
▽新型インフルエンザの治療薬「アビガン」
▽ぜんそくの症状を抑える「オルベスコ」
▽急性膵炎や血栓ができる病気の治療薬「フサン」
それに
▽寄生虫が原因の感染症の薬「イベルメクチン」など
他の病気の治療に使われている薬などで新型コロナに対する効果を確かめる臨床試験や臨床研究が行われています。
専門家 イベルメクチン「闇雲に使われるのは避けるべき」

森島客員教授は「イベルメクチンも期待される治療薬の1つだが、広く使われるためには承認されたほかの治療薬と同様に効果を科学的に実証し、その結果は誰もが納得する主要な医学雑誌で発表する必要がある。イベルメクチンに関する論文ではデータが不正に操作されたものはあるが、感染力が強いデルタ株に効くか言及した論文はほぼないなど、はっきりしたことが分からない。医療体制が危機的な状況となる中、医療者と患者の双方が薬を求める気持ちはよく分かるが、もし副作用が出た時に誰が責任をとるのか、患者をどう守るのか、きちんと保証されずに使われるのは問題で闇雲に使われるのは避けるべきだ」と指摘しています。
イベルメクチン 個人の判断での服用やめるべき
「イベルメクチン」について、通販サイトなどでは「新型コロナウイルスへの治療効果が期待されている」などとして販売され、個人的に購入するという人も出てきていますが、臨床試験に詳しい専門家は現段階では有効性に関する科学的根拠は十分ではなく、個人の判断での服用はやめるべきだとしています。
国際的ウェブサイト「科学的根拠 現時点で見つからず」
各国の専門家が論文を検証して科学的な根拠があるか調べている国際的なウェブサイト「コクラン」は7月末、新型コロナに対するイベルメクチンの有効性について各国から出されている論文を調べたうえで「治療や予防のために使用することを支持する科学的な根拠は現時点では見つからなかった」とする結果を示しました。
専門家 “治療効果にレベルの高いエビデンスない”

薬や治療法の臨床試験に詳しい日本医科大学武蔵小杉病院の勝俣範之教授は、治療法が有効だとする科学的な根拠=「エビデンス」には信頼度が高いものから低いものまであり、現在のところ、イベルメクチンの新型コロナに対する治療効果にはレベルの高いエビデンスはないと指摘します。
国際的に最高レベルのエビデンスと位置づけられるのは「ランダム化比較試験」と呼ばれる臨床試験で、薬を投与する人とプラセボと呼ばれる偽の薬を投与する人に分け、誰に薬が投与されるか患者も医師も分からない状態で客観的に比較した結果です。
勝俣教授によりますと、エビデンスのレベルは主に5段階に分けられ
▽特にレベルが高い「レベル1」に位置づけられるのが「臨床試験に参加する患者が多いランダム化比較試験で証明された治療法」
続いて
▽「レベル2」が「患者数の少ないランダム化比較試験で証明された治療法」とされています。
そして
▽「レベル3」が「比較対照のない臨床試験で出された結果」
▽「レベル4」が「2例以上の観察研究や事例の報告」で
▽「患者の体験談や医師の治療経験、動物実験などの基礎研究」は最も低い「レベル5」に位置づけられます。
勝俣教授は、薬や治療法は医師が患者に投与して有効だと感じても臨床試験で有効性が証明されないケースも多いとしています。
「今の段階で有効性 明確に示されていない」
そのうえで、新型コロナに対するイベルメクチンの有効性について「ランダム化比較試験で検証されているデータも出てきているが、患者数が少ないものが多く今の段階では有効性は明確に示されていない。診療に当たる医師が経験から有効性について言及しているケースもあるが『投与したあとに症状がよくなった』という患者の経過を見ているだけだ。軽症患者の多くは自然に回復するので、薬に効果があったかどうかは診療現場で確かめることはできない。医師個人の経験に基づく話はどんな名医や権威のある医師であっても、科学的根拠の中では最も信頼度の低い『レベル5』の情報だと見なされる」と指摘しました。
そして「今後、有効性が示されることもあるかもしれないが、現段階では示されておらず個人の判断で服用するのはやめたほうがよい。コロナに限らず、不安な状態になると誤った情報や不確かな情報に惑わされやすくなる。 公的な機関から出される情報などをもとに、レベルの高い根拠に裏打ちされているか、しっかり見る必要がある」と話しています。
菅首相 “「抗体カクテル療法」治療薬投与施設 全国に整備を”(8/16)
2021年8月16日
新型コロナウイルス対策で、菅総理大臣は「抗体カクテル療法」として、新たに承認された治療薬の投与を行っている東京都内の宿泊療養施設を視察し、集中的に投与を行える施設を全国の拠点に整備することで、患者の重症化を防ぎたいという考えを強調しました。
菅総理大臣は8月16日午後、東京都の小池知事らとともに、新型コロナウイルスの患者のために都が、宿泊療養施設として確保しているホテルを視察しました。
この施設では、8月13日から、いわゆる「抗体カクテル療法」として、新たに承認された治療薬の投与を行っています。

視察のあと、菅総理大臣は、記者団に対し「抗体カクテル療法」について「『デルタ株』による急激な感染拡大の中にあって、軽症や中等症の方が重症化するのを70%防ぐと言われている。これからも極めて対策として大事だ」と述べました。
そして「全国のおよそ1000の病院で、まずは4000人に投与したところ、多くの方が回復し、かなり効果があるという報告も受けている。一刻も早く、この薬を多くの皆様に届けたい」と述べました。
そのうえで、政府として、治療薬の量は十分に確保しているとして、医療機関だけでなく、集中的に投与を行える施設を全国の拠点に整備することで、患者の重症化を防ぎたいという考えを強調しました。

また、菅総理大臣は、都内の感染対策について「東京の感染を抑えることは全国の感染拡大を抑えることにつながる。常日頃、都としっかり連携しながら対策を講じており、デパートの入場制限やテレワークなどに取り組んでいる」と述べました。
さらに、ワクチン接種について「これだけ感染が広がる中にあっても、間違いなくワクチンは大きな効果がある」と指摘したうえで、今月中に新たに350の会場で職域接種が開始されると明らかにしました。
小池都知事「抗体カクテルは大きな武器」

東京都の小池知事は、「抗体カクテル療法」と呼ばれる治療法を先週から行っている宿泊療養施設を視察したあと、記者団に対して、「宿泊療養施設でも『抗体カクテル』が活用でき、重症化を防ぐことができれば大きな武器になり得る。まさに災害級のレベルにも達してしまっている、デルタ株というコロナ対策に当てていく」と述べました。
また、国と連携した医療提供体制の確保について、「病院や宿泊療養施設、自宅でのサポートについていろいろな意味で協力、連携していくことが肝要だ。何が必要なのか、もっと強化するところはどこなのか、国と連携を図ることが都民の命、健康を守ることに直接つながってくる」と述べました。
抗体カクテル療法 期待と課題
視察に同行した東京都医師会の猪口正孝副会長によりますと、「抗体カクテル療法」を都の宿泊療養施設になっている「品川プリンスホテル」の「イーストタワー」で8月13日から始め、これまでに4人に薬を投与したということです。
「抗体カクテル療法」は、軽症の人の重症化を防ぐことが目的ですが、都内の入院患者の多くはほとんどが中等症か重症のため、軽症が多い宿泊療養施設での投与が有効だとしています。
一方、発症から8日以上たつと有効性があまり認められないことから7日以内の投与が必要ですが、患者の急増で対象者を見つけることが難しくなってきているということです。
投与できる患者を見つけ出し、すぐに対応できる体制づくりが課題です。
塩野義製薬 開発中のコロナ治療薬 初期段階の臨床試験開始(7/26)
2021年7月26日

大阪に本社がある製薬大手の「塩野義製薬」は、開発を進めてきた新型コロナウイルスの治療薬について、初期段階の臨床試験に入ったことを明らかにしました。会社では、試験を通して安全性などを確認することにしています。
「塩野義製薬」は7月26日、開発を進めてきた新型コロナウイルスの治療薬について、7月22日から初期段階の臨床試験に入ったことを明らかにしました。
この段階の臨床試験は、20歳から55歳までの健康な成人男性75人を対象に実施し、安全性などを確認することにしています。
会社では、早い段階でこの治療薬を使えばウイルスの増殖や重症化を防ぐ効果が期待できるとしています。
開発が進められている治療薬は飲み薬で、実用化されれば、点滴などに比べて簡単に使用できるメリットがあります。
塩野義製薬は「発症を予防するワクチンだけではなく、感染した場合に症状を抑えるための治療薬も求められている。社会や医療現場の求めに応えていきたい」とコメントしています。
新型コロナウイルスの重症化を防ぐための飲み薬をめぐっては、アメリカの製薬大手・メルクが最終段階の臨床試験を行うなど海外でも開発が進められています。
中外製薬 新型コロナ「抗体カクテル療法」7月19日承認可否判断へ(7/13)
2021年7月13日

中外製薬が承認申請した「抗体カクテル療法」と呼ばれる新型コロナウイルスの治療法について、厚生労働省は7月19日に承認の可否を判断することを決めました。
承認審査が行われるのは、6月末に新型コロナウイルスの治療薬として中外製薬が承認申請した「カシリビマブ」と「イムデビマブ」です。
同時に投与することで、2種類の抗体が作用してウイルスの働きを抑える「抗体カクテル療法」という治療法で、2020年11月にアメリカのFDA=食品医薬品局から緊急使用の許可を受けています。
アメリカのトランプ前大統領が入院した際にも投与され、中外製薬によりますと、海外で行われた治験では入院や死亡のリスクをおよそ70%減らす効果が確認されているということです。
中外製薬は、審査の手続きを大幅に簡略化する「特例承認」を求めていて、厚生労働省は7月19日に専門家部会を開いて承認の可否を判断することを決めました。
承認されれば、新型コロナウイルスの治療薬としては、レムデシビルとデキサメタゾン、それにバリシチニブに続いて4例目となります。
WHO 新たなコロナ治療薬推奨 日本で開発の「アクテムラ」など(7/7)
2021年7月7日

WHO=世界保健機関は、新型コロナウイルスの重症患者に対して、日本で開発された関節リウマチの治療薬「アクテムラ」などの投与を推奨するとする新たな手引きを公表しました。
WHOは7月6日、イギリスの大学などとともに合わせて1万人余りを対象に行った、新型コロナウイルスの治療薬に関する臨床試験の結果を公表しました。
それによりますと、重症患者に対して関節リウマチの治療薬「アクテムラ=一般名・トシリズマブ」や、同じ仕組みの「サリルマブ」のいずれかを「デキサメタゾン」のようなステロイド剤と合わせて投与した場合、一般的な治療を行った場合に比べ、死亡するリスクが減少したということです。
WHOは、これまで新型コロナウイルスの重症患者には「デキサメタゾン」などのステロイド剤が効果が見られるとしてきましたが、今回の結果を受けて「アクテムラ」や「サリルマブ」も推奨するとする、新たな手引きを公表しました。

「アクテムラ」は、大阪大学の岸本忠三特任教授らのグループと中外製薬が開発した関節リウマチの薬で、免疫の過剰な働きによる炎症を抑える効果があると期待されています。
中外製薬 新型コロナ治療薬 厚生労働省に承認申請(6/30)
2021年6月30日

中外製薬はアメリカで緊急使用許可が出ている開発中の新型コロナウイルスの治療薬について厚生労働省に承認を求める申請を行いました。
承認申請が行われたのは「カシリビマブ」と「イムデビマブ」と呼ばれる2種類の医薬品です。同時に投与することで新型コロナウイルスの働きを抑える中和抗体を作り出す「抗体カクテル療法」という治療法を採用しています。
中外製薬によりますと、海外の治験では入院や死亡のリスクをおよそ70%減らす効果が確認されたということです。
2020年11月には入院をしていない患者への治療薬としてアメリカのFDA=食品医薬品局から緊急使用の許可を取得し、6月29日、厚生労働省にも承認申請を行ったということです。
変異した新型コロナウイルスへの効果も期待できるとされ、承認されればことし国内に供給する分を日本政府が確保することで合意しているということです。
中外製薬は「変異ウイルスの感染拡大など流行が長期化して新たな治療の選択肢が必要とされている。1日も早く患者に届けられるよう規制当局と緊密に協働していく」などとコメントしています。
日本の関節リウマチ治療薬「アクテムラ」 米 コロナで緊急許可(6/25)
2021年6月25日

アメリカFDA=食品医薬品局は6月24日、日本で開発された関節リウマチの治療薬「アクテムラ」について、新型コロナウイルスで入院している患者の、死亡のリスクを下げるなどの効果がみられたとして、緊急使用を許可すると発表しました。
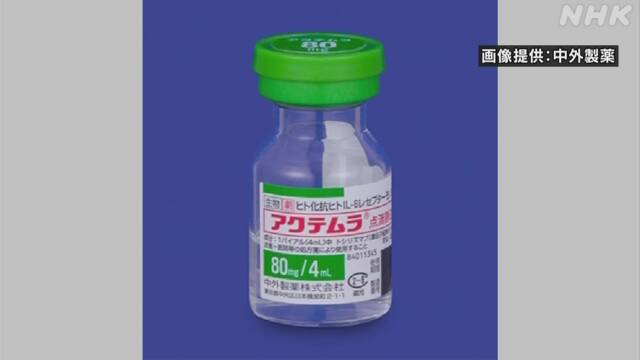
FDAは6月24日、関節リウマチの治療薬「アクテムラ=一般名・トシリズマブ」について、新型コロナウイルスに感染して入院している患者への緊急使用を許可すると発表しました。
対象となるのは酸素の吸入や人工呼吸器、ECMO=人工心肺装置による治療が必要で、かつ、ステロイド系の抗炎症薬を投与されている患者です。
FDAによりますと、4つの臨床試験の結果を分析したところ、アクテムラを投与された患者は、そうでない患者に比べて死亡するリスクが低下したり、入院期間が短くなったりするなどの効果がみられたということです。
「アクテムラ」は、大阪大学の岸本忠三特任教授らのグループと、中外製薬が開発した関節リウマチの薬で、免疫の過剰な働きによる炎症を抑える効果があると期待されています。
変異ウイルスの感染防ぐ中和抗体 富山大学などが作製に成功(6/16)
2021年6月16日

さまざまなタイプの変異した新型コロナウイルスが、細胞に結合するのを防ぎ、感染を防ぐことができるとする中和抗体を人工的に作ることに成功したと、富山大学などの研究グループが発表しました。製薬会社と連携し、治療薬としての開発を目指したいとしています。
これは富山大学の研究グループが6月16日、会見を開いて明らかにしました。
研究グループでは、新型コロナウイルスに感染して回復した患者の血液から、抗体を作り出す免疫細胞の「B細胞」を取り出しました。
そして、このB細胞の遺伝子を組み換えて抗体を作らせることで、特に感染を防ぐ力が強い中和抗体を、人工的に作り出すことに成功したとしています。
研究グループによりますと、この中和抗体は、体の中で新型コロナウイルスが細胞に結合するのを阻害する働きがあり、軽症や中等症の患者に投与すれば重症化を防ぐことが期待できるとしています。
さらに、現在確認されているほとんどの変異ウイルスの感染を防ぐことができるとしていて、研究グループはこの抗体を「スーパー中和抗体」と名付けました。
人工的に作り出した抗体を投与する新型コロナウイルスの薬は、「抗体医薬」と呼ばれ、海外では緊急使用されたものもありますが、変異ウイルスで効果が下がることが課題になっています。
富山大学では今後、製薬会社と連携し、治療薬としての開発を目指したいとしています。
関節リウマチなどの薬「バリシチニブ」新型コロナ治療薬承認へ(4/22)
2021年4月22日
関節リウマチなどの薬「バリシチニブ」が新型コロナウイルスの治療薬として国内で承認される見通しとなりました。治療薬として認められるのは3例目です。
「バリシチニブ」は、免疫の異常反応による炎症を抑える関節リウマチなどの薬で、アメリカでは新型コロナウイルスの患者にも別の治療薬レムデシビルと併用して使用することでより早く回復するとして、2020年11月から緊急的な使用が認められています。
日本国内でも、2020年12月、製薬会社の「日本イーライリリー」から新型コロナウイルスの治療薬として申請があり、厚生労働省は、21日専門家による審議会を開き、承認する方針を固めました。
対象となるのは、酸素吸入が必要な中等症から重症の成人の患者で、レムデシビルと併用して、1日1回錠剤を服用します。
バリシチニブだけを投与することはありません。
厚生労働省によりますと、海外の臨床試験では、バリシチニブをレムデシビルと併用した場合、レムデシビル単独で使用した患者と比べて、平均して1日早く回復したということです。
厚生労働省は、今後、速やかに承認の手続きを進めるとしています。
国内で新型コロナウイルスの治療薬として認められるのはレムデシビルとデキサメタゾンに続き、3例目です。
「アビガン」使用 国が計画する備蓄量の約0.5%にとどまる(3/18)
2021年3月18日
新型コロナウイルスの治療薬として承認審査が続いている「アビガン」について、2月下旬までの1年間に患者に投与されたのは1万人分余りと、国が計画する備蓄量のおよそ0.5%にとどまったことが分かりました。感染症の治療に詳しい専門家は、背景に、有効性が証明されず、臨床研究が続いていることを挙げたうえで、計画どおりに備蓄するか改めて検討する必要があると指摘しています。
「アビガン」は新型インフルエンザの治療薬として開発され、2020年4月、政府は、当時治療薬が限られていた新型コロナウイルスへの効果も期待できるとして、今年度中に200万人分を備蓄する計画をまとめました。
厚生労働省は、すでに備蓄しているおよそ70万人分に加えて、ことし1月に富士フイルム富山化学から55万人分を購入し3月19日、さらに79万人分を購入する方針です。費用は合わせておよそ139億円を見込んでいます。
一方、アビガンの観察研究を続けている藤田医科大学によりますと、2020年2月から2月24日までのおよそ1年間に患者に使用されたのは全国で合わせて1万800人分で、国が計画する備蓄量の0.54%でした。
アビガンをめぐっては、2020年12月、厚生労働省の専門家部会が「現時点のデータでは新型コロナウイルスへの有効性を明確に判断するのが困難だ」として承認の可否の判断を見送り、承認される時期のめどは立っていません。
日本感染症学会の理事長で、東邦大学の舘田一博教授は、「2020年4月は手探りのなかで少しでも効果があるならと備蓄が決められたが、まだ臨床研究が続いていて、効果が証明されていない」としたうえで、「計画どおりに備蓄するのか、一度立ち止まるのかを考えていかなければならない。これまでに得た情報をもとに、ほかの治療薬を活用することも含めて改めて検討すべきだ」と指摘しています。
厚生労働省は、「すでに危機管理の観点などから200万人分を備蓄すると決めている。使用期限は10年間あるので、承認されれば治療薬として使いたい」などとコメントしています。
「アビガン」これまでの経緯
アビガンについて、政府は、当初、2020年5月中の承認を目指し、富士フイルム富山化学が治験を進めていました。しかし、データが思うように集まらず、2020年7月には藤田医科大学などのグループが「初日から投与すると熱が下がりやすい傾向などが見られたものの、統計的に明確な有効性は確認できなかった」などと発表しました。
2020年9月になって富士フイルム富山化学が、「アビガンか偽薬かを患者に伝えずに投与する方法で治験を行った結果、PCR検査で陰性になるまでの期間を2.8日短縮する効果が確認された」などと発表し、10月に厚生労働省に承認申請を行いました。
これに対し、2020年12月に開かれた厚生労働省の専門家部会では、「投与した医師の先入観が影響している可能性を否定できない」などと慎重な判断を求める意見が委員から相次ぎ、厚生労働省が海外の治験のデータなどを踏まえて改めて審査を行う方針を示しています。
治療担当する医師「今はほとんど使っていない」
首都圏の病院で新型コロナウイルスの入院患者の治療を担当している医師は、アビガンを使用する対象を酸素を投与する必要がない比較的軽度の肺炎の患者としたうえで、「感染が始まった初期は使うこともあったが、今はほとんど使っていない」と説明しています。
そのうえで、「今もアビガンの使用を検討していないわけではないが承認されていないうえに胎児への副作用の可能性も指摘されているため、患者の同意を得る手続きが煩雑なこともあって必ずしも投与する必要はないと考えている。そもそも軽症の患者には治療薬が必要ないことも多く、酸素の投与が必要な患者には、すでに承認されているレムデシビルなどを投与して対応している」と話しています。
専門家「通常の調達であれば考えられない」
会計検査院のOBで、現役時代に旧厚生省の検査を担当し、現在は日本大学の客員教授を務める有川博さんは「国民の生命や安全に関わることとは言え、安全性や有効性が確立していない段階で備蓄するのは通常の調達であれば考えられない。緊急に備蓄する必要があって、ほかの薬で代替できないことを国民に説明できるなら調達が認められる可能性はあるが、それができないなら速やかに調達を止め、適切な購入の時期や方法を検討し直すべきだ」などと指摘しています。
「診療の手引き」には ほかの治療薬も
厚生労働省は、医療機関向けの「診療の手引き」で、アビガン以外にも複数の新型コロナウイルスの治療薬を紹介しています。
代表的な薬の1つが、2020年5月に新型コロナウイルスの治療薬として国内で初めて承認された「レムデシビル」です。
エボラ出血熱の治療薬として開発された薬で、原則として人工呼吸器をつけた重症患者などに使用されます。
もう1つが、肺炎などの薬としてすでに承認されていたステロイド剤の「デキサメタゾン」で、イギリスの臨床研究で重症者の死亡を減らす効果が示されています。
「アビガン」については、現在、承認申請中で、無症状や軽症の患者を対象にした臨床試験では、有意差はなかったもののPCR検査で早期に陰性になる傾向などが見られたと説明しています。
抗うつ薬にコロナウイルスの細胞侵入防ぐ効果か 九大など確認(3/17)
2021年3月17日
新型コロナウイルスの治療薬について、九州大学などのグループが、すでに実用化されている抗うつ薬の1つにウイルスが細胞に侵入するのを防ぐ効果があることを細胞を使った実験で確認したと発表しました。
これは、3月17日、九州大学大学院薬学研究院の西田基宏教授と国立医薬品食品衛生研究所の研究グループが発表しました。

グループでは、実験用の細胞にすでに別の病気の治療薬として使われているさまざまな薬と新型コロナウイルスを一緒に加えてそれぞれの反応を調べました。
その結果、抗うつ薬として使われている「クロミプラミン」と呼ばれる薬を使うとウイルスが細胞に侵入するのを50%程度、抑制できることが確認できたということです。
さらに、別の細胞を使った実験ではこの薬をすでに新型コロナウイルスの治療に使われている「レムデシビル」と併用することで、ウイルスの増殖を99%程度抑制できたということです。
グループでは、今後、動物での実験を行うなど有効性や安全性を検証し、新型コロナウイルスの治療薬として実用化を目指すとしています。

西田教授は「この薬でみられたウイルスの侵入を防ぐメカニズムは、変異ウイルスにも一定の効果が期待できるのではないか」と話しています。
簡単な尿検査で重症化予測 新型コロナ 500人規模の臨床研究へ(2/7)
2021年2月7日
簡単な尿検査で新型コロナウイルスに感染した人が重症化するかを予測する500人規模の臨床研究を国立国際医療研究センターのグループが実施することが分かりました。実用化されれば、入院が必要かどうかを判断するのに役立つと期待されています。
この臨床研究は、国立国際医療研究センターのグループが実施するものです。
臨床研究は、新型コロナウイルスに感染して宿泊施設で療養している人や入院している人、およそ500人を対象に、尿に含まれる「L-FABP」というたんぱく質の量を調べるということです。

これまでの研究で、このたんぱく質が正常値より多いと、症状が悪化するリスクが8倍余り、高くなっていたということです。
尿検査は、検査キットを使って自分でできるということで、療養や入院の初日と2日後に検査キットの画像をスマートフォンで送ってもらい、医師が結果を判定します。
グループでは、自治体や医療機関に協力を呼びかけ、2月にも臨床研究を始めたいとしています。
臨床研究を進めている国立国際医療研究センターの片桐大輔医師は「この検査が実用化できれば、重症化リスクの高い患者を優先的に病院に紹介したり、体調のチェックなどを行ったりすることで必要な人がスムーズに入院することに役立つはずだ」と話しています。
新型コロナ 治療薬の候補物質を発見 国立国際医療研究センター(1/26)
2021年1月26日
新型コロナウイルスに感染した患者の治療の際には、他の病気の薬で新型コロナへの効果が確認されたものなどが使われていますが、まだ特効薬はありません。国立国際医療研究センターのグループは、ウイルスの増殖に必要な酵素の働きを妨げる新たな治療薬の候補となる物質を複数見つけたことを明らかにし、今後、臨床での応用を目指して研究を進めるとしています。
これは国立国際医療研究センター研究所の満屋裕明所長が、26日に開かれたメディア向けのオンラインセミナーの中で明らかにしました。
満屋所長のグループは、新型コロナウイルスが細胞内で増殖する際に必要な「プロテアーゼ」と呼ばれる酵素に着目し、酵素の働きを妨げ、ウイルスの増殖を防ぐ治療薬の研究を去年2月から進めています。
これまでに400種類余りの化学物質を人工的に合成していて、こうした物質を使ってウイルスに感染した細胞での実験などを行ったところ、2種類の物質が酵素と結び付いて、ウイルスの増殖を抑える効果が特に高いことが分かったということです。
このうちの1つは現在、患者の治療に使われているレムデシビルと合わせると、ウイルスの増殖が1億分の1にまで抑えられたとしています。
満屋所長は「さらに効果の高いものを合成するなど、より有望な物質の探索に努めたい」と話していて、今後、動物実験を行うなど、臨床での応用を目指して研究を進めるとしています。
コロナ重篤患者 日本で開発「アクテムラ」などで死亡率低下 英大学(1/11)
2021年1月11日

新型コロナウイルスで重篤となった患者に、日本で開発された関節リウマチの治療薬を投与することで、死亡率が下がったなどとする研究成果を、イギリスの大学などのグループが公表しました。
これはイギリスの大学「インペリアル・カレッジ・ロンドン」などのグループが公表したものです。
グループでは、集中治療室で人工呼吸器をつけている重症の患者およそ800人を対象に、関節リウマチの薬「アクテムラ=一般名・トシリズマブ」や同じ仕組みの「サリルマブ」という薬を投与して効果を調べました。
その結果「アクテムラ」などを使わなかった患者およそ400人では死亡率が35.8%だったのに対し「アクテムラ」を投与したおよそ350人は死亡率が28%と7ポイント余り低くなっていました。
「サリルマブ」についても同様の効果がみられたということです。
また、いずれの薬でも、集中治療を受ける期間が10日ほど短くなったということです。
「アクテムラ」は、大阪大学の岸本忠三特任教授らのグループと中外製薬が開発した関節リウマチの薬で、免疫が暴走して自分の細胞を攻撃してしまう「サイトカインストーム」という現象を抑える効果があると期待されています。
結果を受けてイギリス政府は、重症患者に「アクテムラ」などを使うよう推奨する方針をウェブサイトで示しました。
新型コロナ治療薬レムデシビル 中等症患者にも投与拡大 厚労省(1/10)
2021年1月10日
新型コロナウイルスの治療薬「レムデシビル」について、厚生労働省は投与を認める対象をこれまでの重症患者に加え、肺炎になった中等症患者にも拡大しました。
「レムデシビル」は新型コロナウイルスの治療薬として2020年5月に厚生労働省が特例承認し、原則、人工呼吸器や人工心肺装置=ECMOをつけている重症患者などに投与が限定されていました。
その後、製薬企業から追加で臨床試験のデータが提出され、厚生労働省は「重症患者以外でも有効性が確認された」などとして、投与を認める対象を肺炎になった中等症患者にも拡大しました。
一方、日本への供給量が限られていることから、当面は重症患者への使用を希望する医療機関に限定して供給するとしています。
レムデシビルをめぐっては、WHO=世界保健機関が2020年11月「死亡率の低下などにつながる重要な効果はなかった」などとして、入院患者への投与は勧められないとする指針を公表していますが、厚生労働省は「これまでの評価に影響を及ぼすものではない」としています。
コロナから回復した人の抗体を集め薬に 国際的な治験始まる(12/24)
2020年12月24日

新型コロナウイルスから回復した人の抗体で作る「特殊免疫グロブリン製剤」の国際的な治験が始まり、日本でも国立国際医療研究センターなどが参加し、実際の患者に投与して効果や安全性を調べています。
この治験は、アメリカの国立アレルギー・感染症研究所が資金を提供する国際的な枠組みが進めていて、日本からは国立国際医療研究センターと愛知県の藤田医科大学が参加しています。
「特殊免疫グロブリン製剤」は新型コロナウイルスに感染して回復した人の抗体を集め、薬にしたもので、新型コロナウイルスに対する効果が期待されています。
国立国際医療研究センターによりますと、藤田医科大学と共同で新型コロナウイルスに感染して入院が必要な国内の患者10人を対象に薬を投与し、およそ1か月間、経過を観察するということで、各国からのデータとあわせて効果や有効性を調べるということです。
また、国立国際医療研究センターでは現在、回復した人の血液から抗体が含まれた「血しょう」と呼ばれる成分をとりだして投与する「回復者血しょう治療」の臨床研究も進められていて、効果や安全性に違いがあるのかなども調べるということです。
国立国際医療研究センターは「新型コロナウイルスに対する有効な治療法が限られている中で、この治療法の効果や安全性が証明されれば、有効な治療手段の一つになる可能性がある」としています。
レムデシビル WHO 入院患者への投与勧められないとの指針公表(11/20)
2020年11月20日
新型コロナウイルスの治療薬として日本で特例承認されている、抗ウイルス薬レムデシビルについて、WHO=世界保健機関は、世界各地の臨床試験を分析した結果、「死亡率の低下などにつながる重要な効果はなかった」として、入院患者への投与は勧められないとする指針を公表しました。
レムデシビルを開発した製薬会社ギリアド・サイエンシズは、患者が回復に至るまでの期間は大幅に短縮しているなどと反論しています。
WHOは11月20日、抗ウイルス薬レムデシビルを使った世界各地の入院患者に対する臨床試験を分析し、治療に関する指針を公表しました。
それによりますと、
▽死亡率の低下や
▽人工呼吸器の必要性、
それに
▽症状の改善にかかる時間について、
「重要な効果はなかった」としています。
このため、WHOはレムデシビルについて「症状の軽い重いにかかわらず、入院患者への投与は勧められない」としています。
レムデシビルについては、アメリカのFDA=食品医薬品局が、ことし5月、緊急での使用を許可し、これを受けて日本も特例で使用を承認していて、アメリカでは10月、新型コロナウイルスの治療薬として正式に承認されています。
製薬会社 ギリアド・サイエンシズが声明
ギリアド・サイエンシズは、WHOが指針を公表したことに対して声明を出しました。
それによりますと「製品は、アメリカ、日本、イギリス、ドイツの信頼度の高い多くの治療指針で、入院患者への標準治療薬として認識されている。これらの推奨は、複数の試験からの強固なエビデンスに基づいていて行われている」としています。
そのうえで「患者が回復に至るまでの期間の大幅な短縮などの効果は、医療機関に恩恵をもたらしている。WHOの指針はこのエビデンスを軽視しているように見え、残念に思う。現在世界中で患者数が劇的に増加している中、およそ50か国で、初めてかつ唯一の承認された治療薬として、医師たちに信頼されている」としています。
厚生労働省「承認 見直す予定ない」
レムデシビルは、日本で初めての新型コロナウイルスの治療薬として、ことし5月に承認されました。
アメリカで重症患者に対する緊急的な使用が認められたことを受けて、厚生労働省は審査を大幅に簡略化する「特定承認」の制度を適用し、製薬会社の申請から3日という異例の早さで承認しました。
厚生労働省が公表している「診療の手引き」では、原則、人工呼吸器や人工心肺装置=ECMOなどを装着する重症患者に投与することとしています。
レムデシビルは新型コロナウイルスの増殖を抑える作用がある治療薬としては、今も国内で承認された唯一の薬となっています。
供給量が限定されるため、現在は厚生労働省から使用を希望する医療機関に配付されています。
今回のWHOの指針について、厚生労働省は「承認時に根拠にした治験のデータが否定されたわけではないうえ、有効性がないという結果でもないため、承認について見直す予定はない」と話しています。
加藤官房長官は閣議のあとの記者会見で、指針について「レムデシビルの効果がないとまでは証明されておらず、また、レムデシビルに効果があるとする十分なエビデンスもないという説明などが記載されている」と述べました。
そのうえで「日本ではアメリカでの緊急使用許可を契機に、複数の臨床試験の結果から一定の有効性が確認できたことから、5月に特例承認を行い、現在、レムデシビルを使った治療がなされている。厚生労働省では特段、承認について見直す必要はないというのが、現時点での認識だと承知している」と述べました。
現場の医師「効果を実感 引き続き使っていく」
これまでレムデシビルを使った治療を行ってきた、東京 渋谷区の日本赤十字社医療センターの出雲雄大呼吸器内科部長は、「日本で特例承認されてから、これまでおよそ40人の新型コロナウイルスの重症患者に対してレムデシビルを投与してきたが、生存率の向上や、人工呼吸器から離脱できるようになるなど、効果を実感してきた。レムデシビルは、1人に25万円程度かかるなど高価なこともあり、WHOは『推奨しない』と判断したのかもしれないが、命はお金より重いはずだ。ほかに特効薬が出るまでは、私たちとしては引き続き使っていくことになる」と話していました。
新型コロナ治療薬開発へ 業種を越え5社が連携し新会社設立(11/12)
2020年11月12日

新型コロナウイルスの治療薬をできるだけ早く開発するため、製薬のベンチャー企業とIT大手など、5社が共同で新会社を設立しました。企業が業種を越えて連携し、計算能力が高いコンピューターを活用することで、開発にかかる期間を大幅に短くすることをねらいます。

製薬のベンチャー企業ペプチドリームと、IT大手の富士通など5社は、新型コロナウイルスの治療薬を開発するための新会社を共同で設立しました。
開発を目指す治療薬は、ウイルスが体内の細胞に結合しないようにするもので、薬に最も適したアミノ酸の構造を素早く見つけ出せるかどうかが、開発のかぎを握ります。
新会社では、富士通が開発した計算能力が高いコンピューターなどを活用することで、ペプチドリームが進めてきた研究を加速させ、開発にかかる期間を大幅に短くすることをねらいます。
新会社は11月12日から事業を始め、国内外の大手製薬会社とも連携を図りながら、早ければ来年の秋にも臨床試験を始め、2年後の実用化を目指すとしています。
新型コロナ「回復者血しょう治療」6人に投与 臨床研究報告(11/10)
2020年11月10日
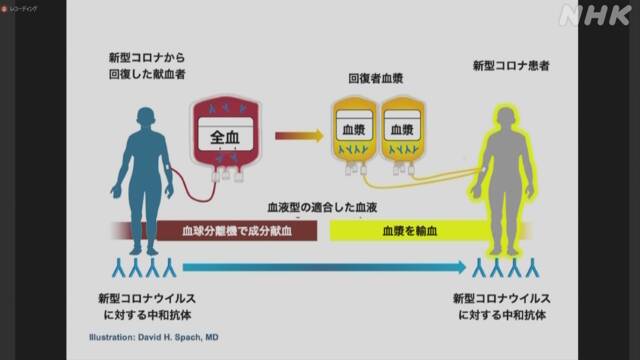
新型コロナウイルスの最前線で治療を担っている国立国際医療研究センターのシンポジウムが11月10日、オンラインで開かれ、回復した人の血液の成分を別の患者に投与する「回復者血しょう治療」の臨床研究についての最新の状況などが報告されました。

このシンポジウムは国立国際医療研究センターが開いたもので、国内外の研究者や医師が参加して、これまでの流行状況やワクチンや治療法の最新の開発状況などが報告されました。
このうち、国立国際医療研究センターの忽那賢志医師からは、回復した人の血液から抗体が含まれた「血しょう」を取り出し、別の患者に投与する「回復者血しょう治療」の臨床研究について最新の状況が報告されました。
それによりますと、これまでに97人の回復者から血しょうが提供され、30代から60代の男性、合わせて6人に血しょうが投与されたということです。
いずれの患者も現在のところ異常は見られないということで、呼吸状態が悪化した中等症以上の合わせておよそ60人に投与し、安全性や効果を判断するということです。
「回復者血しょう治療」はアメリカでは、緊急の使用が許可されていますが国内ではまだ承認されていません。

講演の中で忽那医師は「まずは安全性の評価が重要だ。今後も血しょうを提供していただける回復者の方を募集しているので、さらに研究を進めていきたい」と話していました。
米製薬会社の「抗体医薬」FDAが緊急使用許可 軽中症状に効果(11/10)
2020年11月10日

アメリカのFDA=食品医薬品局は、製薬会社イーライリリーが新型コロナウイルスの治療薬として開発中の「抗体医薬」について、軽症から中程度の症状の患者に一定の効果がみられるとして、緊急の使用許可を出したと発表しました。
FDAは11月9日、アメリカの製薬会社イーライリリーが新型コロナウイルスの治療薬として開発中の抗体医薬「バムラニビマブ」について緊急の使用許可を出したと発表しました。
使用できるのは12歳以上、体重40キロ以上で、重症化や入院に至るリスクの高い新型コロナウイルスの患者です。
抗体医薬は、体内の異物を排除する「抗体」と呼ばれる物質を人工的に作りだし、薬として患者に投与するもので、FDAによりますと、「バムラニビマブ」の臨床試験の暫定的な結果では、投与された患者の入院や救急治療を受けた割合が、投与されなかった患者より低いといった効果がみられたということです。
こうしたことからFDAは「バムラニビマブ」には軽症から中程度の症状の患者に対してリスクを上回る効果があるとしています。
一方、人工呼吸器が必要な患者などに対しては症状が悪化する可能性があるとして投与は許可されていません。
症状悪化するケースの指摘も
感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は、「これまで認可されていた新型コロナウイルスの治療薬は、いずれも重症者向けで、その前の段階の患者に使える薬が新たに登場したのは前進だ。ただ、人工的に作った抗体はコストがかかることや、症状が悪化するケースがあるという指摘されることなど課題もある。使用にあたっては重症化へのリスクが高い軽症の患者や中等症の患者に限定するべきだと思う」と話しています。
「レムデシビル」新型コロナ治療薬にアメリカで正式承認(10/23)
2020年10月23日
新型コロナウイルスの治療薬として、日本で特例承認されている抗ウイルス薬「レムデシビル」がアメリカで正式に承認されました。
アメリカの製薬会社が、エボラ出血熱の治療薬として開発を進めてきた抗ウイルス薬「レムデシビル」は、新型コロナウイルスへの治療薬として臨床試験が行われていて、アメリカFDA=食品医薬品局は、ことし5月、緊急での使用を許可し、これを受けて日本も特例で使用を承認しています。
FDAは10月22日、複数の臨床試験の結果に基づき「レムデシビル」を新型コロナウイルスの治療薬として、正式に承認したと発表しました。
対象となるのは年齢が12歳以上で、体重40キロ以上の入院が必要な患者です。
レムデシビルについては、アメリカNIH=国立衛生研究所などが行った臨床試験で、患者が回復する期間を短縮する効果があったと報告されていて、新型コロナウイルスに感染したトランプ大統領にも投与されました。
一方、WHO=世界保健機関が発表した臨床試験の結果では、患者の死亡率の改善や、入院期間の短縮について「ほとんど効果が認められないか、全く効果が認められなかったようだ」と評価が分かれています。
「アビガン」新型コロナ治療薬として国の承認求める申請(10/16)
2020年10月16日

インフルエンザの治療薬「アビガン」について、薬を開発した会社は10月16日、新型コロナウイルスの治療薬として国の承認を求める申請を行ったと発表しました。
「アビガン」は、富士フイルム富山化学が開発した抗ウイルス薬で、新型インフルエンザの治療薬として承認されていて、新型コロナウイルスでも治療効果が期待されています。
会社は9月、新型コロナウイルスの患者を対象にした治験の結果を発表し、薬を投与することで、症状が改善してPCR検査で陰性になるまでの期間が2.8日短縮される効果が確認できたとしました。
また、治験ではこれまで知られている以外の副作用は見られず、安全性に関する新たな懸念はなかったということです。
この結果を受け会社は、10月16日、アビガンについて新型コロナウイルスの治療薬として正式に承認を得るため厚生労働省に申請を行ったと発表しました。
富士フイルムグループは「新型コロナウイルスの患者に1日も早く治療薬を届けることで、感染拡大の抑止や流行の終息に貢献していきます」とコメントしています。
新型コロナウイルスの治療薬は、これまでにエボラ出血熱の治療薬として開発が進められた「レムデシビル」が承認され、ステロイド剤の「デキサメタゾン」が推奨されています。
田村厚労相「安全性や有効性精査し判断」
田村厚生労働大臣は、閣議のあとの記者会見で「安全性や有効性をしっかりと精査したうえで、最終的に承認するかを判断したい。どれくらい時間がかかるかは、データの内容を見ないと分からないが、緊急事態であると認識しており、しっかり精査させてもらう」と述べました。
レムデシビル「回復にかかる期間を短縮」臨床試験 最終報告(10/9)
2020年10月9日

アメリカ国立衛生研究所などの研究グループは、抗ウイルス薬レムデシビルの国際的な臨床試験の最終報告を公表し、新型コロナウイルスの患者の回復にかかる期間を短縮し、重症化を防ぐ効果が期待できるという見解を示しました。
アメリカのNIH=国立衛生研究所などの研究グループは10月8日、抗ウイルス薬レムデシビルの国際的な臨床試験の最終報告を医学雑誌「ニューイングランド・ジャーナル・オブ・メディシン」で公表しました。
それによりますと、試験はアメリカ、日本を含む10か国で新型コロナウイルスに感染して入院した成人およそ1000人を対象に実施され、レムデシビルを最大で10日間、投与したグループと投与しなかったグループで経過を比較しました。
その結果、投与したグループでは患者が一定程度回復するまでにかかる期間の中央値が10日間と、投与しなかったグループの15日間に比べて短く、投与開始から15日目の回復の度合いもより良好だったということです。
このため研究グループでは、新型コロナウイルスの患者の回復にかかる期間を短縮し、重症化を防ぐ効果を期待できるという見解を示しています。
レムデシビルは日本ではことし5月に特例で承認されていますが、アメリカでは緊急の使用許可にとどまり正式には承認されていません。
ただ最近は新型コロナウイルスに感染したトランプ大統領に投与されたことでも知られていて、今回の結果を受けてアメリカでも承認に向けた動きが加速するとみられます。
EU 最大50万人分の購入契約
抗ウイルス薬レムデシビルについて、EU=ヨーロッパ連合は10月8日、最大50万人分を購入する契約を薬を開発するアメリカの製薬会社と結んだと発表しました。
それによりますと、購入額は7000万ユーロ、日本円で87億円余りとなり、EU加盟国にイギリスやノルウェーなど医療物資を共同調達する協定を結ぶ国を加えた36か国が提供を受けられるということです。
EUは現時点ですでにおよそ3万人分のレムデシビルを購入していますが、多くの国で感染が再び拡大傾向にあることから、大幅に買い増すことを検討していました。
EUで保健政策を担当するキリアキデス委員は「新型コロナウイルスに対するヨーロッパの結束を示すものだ」としています。
トランプ大統領 「自身の体調改善の抗体医薬」普及努める考え強調(10/8)
2020年10月8日
新型コロナウイルスに感染したトランプ大統領は、ツイッターにビデオメッセージを投稿し、退院した10月5日以来、初めて姿を見せました。この中でトランプ大統領は、投与された抗体医薬によって体調が改善したとして、こうした薬の普及に努める考えを強調しました。
新型コロナウイルスに感染したトランプ大統領は10月7日、ツイッターにビデオメッセージを投稿し、退院した10月5日以来、初めて姿を見せました。
この中でトランプ大統領は「入院した時は体調がよくなかったが、抗体医薬の投与を受けるとすぐによくなった。完治したと言ってもよい」と述べて、薬の効果を強調しました。
アメリカの製薬会社「リジェネロン」社が開発中のこの抗体医薬は、臨床試験中で規制当局の承認はまだ受けていませんが、トランプ大統領は「皆さんが無料で手に入るようにする。準備はできている。大統領が受けられる治療を国民全員が受けられるようにしたい」と述べて、普及を進めたい考えを示しました。
そして「私が感染したのは神の恩恵だと思っている。もし感染していなければ、この薬をほかの薬と同じようにしかみていなかっただろう。本当にすばらしい薬だ」と述べて、感染の経験を感染対策に生かすと主張し、対策が不十分だったとの批判をかわしたいねらいをうかがわせました。
また、これまで「10月にも使えるようになる」と述べていたワクチンの実用化の時期については、「極めて早い時期にできる。選挙の前に実用化するべきだと思うが、政治的な事情もあり、選挙の直後になるだろう」と述べ、実用化は選挙後になるとの見通しを示しました。
「アビガン」コロナ治療薬の有効性など確認へ 早期審査 厚労相(10/6)
2020年10月6日

インフルエンザの治療薬「アビガン」について、10月中にも、新型コロナウイルスの治療薬としての承認申請が行われる見通しとなったことについて、田村厚生労働大臣は、有効性や安全性を確認するため、早期に審査を行う考えを示しました。

インフルエンザの治療薬「アビガン」について、薬を開発した会社が新型コロナウイルスに感染した患者に投与する治験で一定の有効性が確認されたと発表し、10月中にも新型コロナウイルスの治療薬としての承認申請を行うとしています。
これについて、田村厚生労働大臣は、閣議のあとの記者会見で、「新型コロナウイルスの医薬品に関しては、ことがことなので、審査を早め、集中的に行うと申し上げている。しっかりと審査し、なるべく早く、国民のニーズに沿った形で有効で安全なものを承認したい」と述べました。
一方で、田村大臣は、承認の見通しについて、「申請前から承認の時期が決まっていることはありえない。申請してもらい、有効性や安全性を確認したうえで、承認するかしないかを決めるので、いつ承認するか、予断を持って答えられる状況にない」と説明しました。
「回復者血しょう治療」患者に投与へ 臨床研究で承認(9/27)
2020年9月27日
新型コロナウイルスの患者にすでに回復した人の血液の成分を投与する「回復者血しょう治療」について国立国際医療研究センターが進めている臨床研究で実際の患者への投与が内部の倫理委員会で承認されたことが分かりました。
「回復者血しょう治療」は、回復した人の血液から抗体が含まれた「血しょう」と呼ばれる成分を取り出し、別の新型コロナウイルスの患者に投与するもので、各国で研究が進んでいてアメリカでは緊急の使用が許可されています。
国内では国立国際医療研究センターが研究を進めていて、これまでに回復した人60人分の「血しょう」が集まっているということです。
センターによりますと、9月15日に内部の倫理委員会で、実際の患者への投与が正式に承認されたということです。
臨床研究では酸素の吸入が必要な中等症の患者およそ60人に、別の感染症のリスクなどが無いことを確認した「血しょう」を投与し、安全性や効果を調べるということです。
研究を担当する国立国際医療研究センターの忽那賢志医師は「特効薬がない中、治療法の1つとして有効性と安全性を確認する意味は大きい。今後の流行状況にもよるが、なるべく早く研究を進め、慎重に効果を検証したい」と話しています。
アビガン 治験 ”一定の有効性確認” 10月中にも承認申請へ(9/23)
2020年9月23日
インフルエンザの治療薬「アビガン」について、薬を開発した会社が新型コロナウイルスに感染した患者に投与する治験で一定の有効性が確認されたと発表しました。
10月中にも新型コロナウイルスの治療薬としての承認申請を行うとしています。
「アビガン」は、富士フイルム富山化学が開発した抗ウイルス薬で、これまで、比較的症状が軽い新型コロナウイルスの患者に対して、状態を観察する研究の枠組みで投与が行われてきました。
富士フイルムによりますと、患者に投与して国の承認を目指すための治験で、20歳から74歳までの患者156人について、症状が改善してPCR検査で陰性になるまでの期間を調べたところ、アビガンを投与しなかったグループでは14.7日だったのに対し、投与したグループでは11.9日と、およそ3日間短かったということです。
また、これまでに知られている腎機能や肝機能が低下するなど以外の副作用は見られず、安全性に関する新たな懸念はなかったとしています。
これを受け、会社は来月中にも新型コロナウイルスの治療薬としての承認申請を行うとしています。
「アビガン」の治験は当初は6月末までの予定でしたが、いったん感染者が少なくなったなどの理由で予定を延長して続けられ、この間、7月には藤田医科大学などのグループが患者88人に投与した臨床研究で統計的に明確な有効性は確認できなかったなどとする結果を発表していました。
新型コロナウイルスの治療薬はこれまでにエボラ出血熱の治療薬として開発が進められた「レムデシビル」が承認され、ステロイド剤の「デキサメタゾン」が推奨されています。
名古屋大学 新型コロナ 人工の抗体 速やかに作ることに成功(9/19)
2020年9月19日

新型コロナウイルスに感染すると体内にできる「抗体」と同様のたんぱく質を速やかに人工的に作ることに名古屋大学などの研究グループが成功し、細胞への感染を抑えることも確認できたと発表しました。研究グループは、新しい治療薬の開発などに応用できる可能性があるとしています。
抗体を作ることに成功したのは、名古屋大学の村上裕教授と名古屋医療センターの研究グループです。
新型コロナウイルスに感染すると、体内に「抗体」と呼ばれるたんぱく質が作られ、その後、ウイルスが細胞に入り込むのを防ぐとされています。
これまで、抗体を人工的に作るには少なくとも数週間かかっていましたが、研究グループは10兆を超える人工の抗体の中から特定のウイルスに結びつくものを速やかに選び出す「TRAP提示法」という新しい技術を開発し、新型コロナウイルスに対する抗体を4日間で作ることに成功したということです。
また、人工的に作った抗体は新型コロナウイルスだけと非常に強く結合する特徴があり、ウイルスの細胞への感染を抑えることが確認できたということです。
研究グループでは、この抗体を感染の有無を調べる検査や新しい治療薬の開発に応用できる可能性があるとしています。
研究成果は、アメリカの科学雑誌「サイエンス・アドバンシズ」の電子版に9月19日、掲載されます。
イベルメクチン コロナ治療薬への承認目指し治験へ 北里大病院(9/17)
2020年9月17日

ノーベル医学・生理学賞を受賞した大村智さんが発見した物質をもとに開発された、感染症の薬「イベルメクチン」について、新型コロナウイルスの新たな治療薬として国の承認を目指す治験を近く始めると、北里大学病院が発表しました。
「イベルメクチン」は、北里大学の大村智特別栄誉教授が発見した物質をもとに開発された、寄生虫が引き起こす感染症の特効薬で、北里大学病院は9月17日、患者に投与して新型コロナウイルスの新たな治療薬としての承認を目指す治験を近く始めると発表しました。
治験は、新型コロナウイルスに感染して軽症から中等症となった20歳以上の患者240人を、薬を投与するグループと偽の薬を投与するグループに分け、ウイルスが検出されなくなるまでの期間や症状の変化などを比較する計画で、来年3月末までかけて有効性や安全性を確認することにしています。
この薬をめぐっては、死亡率を下げる効果があるとする研究がアメリカの大学から出されましたが、この際に患者のデータを提供した会社が関わった別の研究でデータが検証できないという問題が発覚し、影響が懸念されていました。
北里大学の学校法人、北里研究所は「細胞を使った実験では新型コロナウイルスの増殖を抑える効果が見られている。治験を通じて安全性と有効性を厳しく検証し、承認を目指したい」と話しています。
新型コロナ 投薬治療のガイドライン 学会が初めて作成(9/9)
2020年9月9日
新型コロナウイルスの治療に関する研究が進む中、日本集中治療医学会などは、世界中の論文を分析し、患者の状態別に、どの治療薬が推奨できるかをまとめたガイドラインを初めて作成しました。
新型コロナウイルスは治療に関する研究が進んでいますが、病気のメカニズムは十分解明されておらず、患者の症状に合わせてさまざまな治療薬が使われています。
こうした中、日本集中治療医学会と日本救急医学会は、世界各国の研究論文などを分析したうえで、どのような状態の患者にどの薬を投与すべきかをまとめたガイドラインを初めて作成しました。
それによりますと、ステロイド剤の「デキサメタゾン」は中等症と重症の患者には投与を強く推奨する一方で、軽症の患者には逆に投与しないことを強く推奨しています。
また、国内で初めて新型ウイルス治療薬として承認された「レムデシビル」は、軽症の患者については効果が確認されておらず現時点で推奨していませんが、中等症や重症の患者への投与は弱く推奨するとしています。
さらに国内の製薬会社が開発し臨床研究が行われている「アビガン」は、軽症患者への投与は弱く推奨し、中等症と重症の患者への投与は現時点で推奨していません。
ガイドラインは2つの学会のホームページで公開する予定で、今後、新たな論文が出ればそのつど精査し、内容を更新することにしています。
日本集中治療医学会の西田修理事長は、「治療に関してさまざまな情報があふれる中、現場に役立つよう整理した。新型コロナウイルスは一刻も早く適切な治療を行うことが必要で、参考にしてもらいたい」と話しています。
新型コロナ治療薬 回復した人の抗体もとに開発へ 福島県立医大(9/7)
2020年9月7日

新型コロナウイルスから回復した人が持つ「抗体」をもとにした薬を開発する計画について、福島県立医科大学が記者会見し、薬に適した抗体を得るため、感染を経験した人に対して血液の提供を呼びかけました。
新型コロナウイルスの治療薬は、現在、ほかの病気の治療薬で効果が確認されたものなどが使われていますが、回復した人の血液中にあるウイルスの増殖を抑える働きのある「中和抗体」と呼ばれるたんぱく質をもとに薬を作れば、効果が高いのではないかと期待されています。
福島県立医科大学の高木基樹教授らの研究グループは7日記者会見し、「中和抗体」をもとに薬を開発する計画などについて説明しました。
研究グループは微量の血液などのサンプルから多くの抗体を一度に検出できる「免疫モニターチップ」という技術を開発していて、これまでにおよそ40人から血液の提供を受けて分析しているとしています。
今後、100人分の血液を分析して薬に適した中和抗体を得ることを目標にしているということで、回復した人たちに対し協力を呼びかけました。
研究グループでは、中和抗体が得られれば、複製して大量生産することを目指していて、ワクチンが効かない人にも効果が期待できるとしています。
高木教授は「ワクチンや既存の薬ですべての感染者を治療することは難しいので、新しい治療方法として抗体医薬品を提供していきたい」と話していました。
新型コロナの治療薬開発の現状は
新型コロナウイルスの患者の治療に現在使われている薬は、もともと別の病気の治療用に開発された既存の薬で、新型コロナウイルスにも効果があるか調べる「ドラッグ・リポジショニング」と呼ばれる研究の結果、使われるようになりました。
例えば、「レムデシビル」はエボラ出血熱の治療薬として開発されてきた薬、また「デキサメタゾン」は重度の肺炎の治療に使われるステロイド剤ですが、欧米での臨床試験の結果、新型コロナウイルス患者にも効果を示すことがわかりました。
既存の薬は、どのような副作用が出るかなど、安全性や使用上の注意点がある程度わかっているため、最初から治療薬を開発するより、使えるようになるまでの時間が短縮できるのが大きな利点です。
一方で、最初から新型コロナウイルスを狙って増殖を抑える薬の開発も各国で進められています。
薬の開発の手法は複数あり、1つは薬の候補となる化合物のリストの中から、新型コロナウイルスへの効果が見込まれるものを選び、安全性や有効性を確認する方法です。
塩野義製薬と北海道大学のグループは、薬の候補となる化合物をこれまでに複数選定し、細胞を使った実験などを進めていて、来年3月までに実際に人に投与する臨床試験を目指すとしています。
また鹿児島大学のグループは、製薬ベンチャー企業とともに、C型肝炎の治療薬開発のために集められたおよそ2000種類の化合物の中から薬の候補となる物質を選び、動物実験などを通じて安全性や有効性を確かめるプロジェクトを進めています。
一方で、注目が高まっているのが「抗体医薬」で、新型コロナウイルスの働きを抑えるたんぱく質、「中和抗体」を特定して人工的に作り、治療薬として投与しようとしています。
抗体がウイルスだけを狙い撃ちにするため、効果が高いのではないかと期待されていて、国内では、7日研究発表が行われた福島県立医科大学のほか、東京大学医科学研究所や京都大学などの研究グループが中和抗体を使った治療薬の開発を目指して、細胞での実験など研究を進めています。
一方、アメリカでは、すでに複数の会社が人に投与する臨床試験を進めています。
このうち大手製薬会社「イーライリリー」は、新型コロナウイルスに感染して回復した患者から抽出した抗体をもとに作った抗体医薬の候補を、カナダの製薬会社と共同で開発していて、先月からは感染すると重症化のリスクのある高齢者施設の入所者などを対象に、最終段階の試験を始めています。
抗体医薬とは
抗体医薬は、体の中で作られ異物を排除するたんぱく質、「抗体」を人工的に作って投与することで、ウイルスやがん細胞など、病気の原因となる物質を攻撃して治療する薬です。
抗体が、特定のウイルスやがん細胞などに現れている目印に結合することでその増殖を防ぐ仕組みで、1990年代以降、さまざまな種類のがんのほか、リウマチなど免疫が関わる病気の治療薬が開発され、日本国内でも数十種類が承認されています。
新型コロナウイルスの治療を目指した抗体医薬の開発研究も進められ、アメリカなどでは実際に人に投与して安全性や有効性を検証する臨床試験が始まっています。
抗体医薬は、ウイルスなどを狙い撃ちにするため、副作用が少なく、高い効果が期待できるとされるほか、ウイルスの増殖を抑えることがわかっている抗体をもとに開発するため、実用化までにかかる期間も従来の新薬開発より短縮できるとされています。
その一方で、人工的に抗体を作るのに多くのコストがかかり、治療薬の価格が高くなる傾向があるほか、抗体が細胞にウイルスが感染する際のかけ橋となってしまい、かえって症状を悪化させてしまう現象が起きるおそれも指摘されています。
専門家「安全性検証 時間かけて入念に」
新型コロナウイルスの抗体医薬について、感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は、「新型コロナウイルスの治療薬開発の中で、抗体医薬は、従来の薬よりも開発に時間がかからず、すでに別の感染症にも抗体医薬が開発されて使われていることもあり、アメリカや中国など各国で主流になってきている。ただ、別の感染症では、抗体によってかえって症状が悪化したケースもあったと指摘されていて、安全性を検証するための臨床試験などのプロセスはほかの薬と同様、一定程度時間をかけて入念に行われるべきだ」と話しています。
鹿児島大がコロナの新治療法 炎症起こす細胞除去で重症化予防(8/31)
2020年8月31日

鹿児島大学は新型コロナウイルスの新たな治療法として、臓器に炎症を引き起こす血液中の細胞を特殊な医療機器を使って取り除くことで、重症化を予防できるとする研究成果を発表しました。

鹿児島大学大学院の金蔵拓郎教授などは8月31日、記者会見を開き、新たな研究成果について7月、アメリカの学術誌に発表したと明らかにしました。
新型コロナウイルスの重症化は、肺などの臓器に炎症を引き起こす「サイトカイン」と呼ばれる物質が、白血球など血液に含まれる免疫系の細胞で過剰にできることが原因とされていて、免疫の暴走「サイトカインストーム」と言われます。
金蔵教授によりますと、点滴のように静脈に針を刺して血液を体の外で循環させ、この際に「アダカラム」と呼ばれる医療機器を通すことで、炎症を引き起こす細胞を取り除くことができるとしています。
実際にスペインでは、新型コロナウイルスによる肺炎の患者で症状が緩和された症例も報告されているということです。
新型コロナウイルスの治療をめぐっては、ウイルスの働きを抑えるレムデシビルや、重度の感染症や肺炎の治療薬として使われているデキサメタゾンといった薬の有効性が確認されています。
この機器はすでに国内で開発され、潰瘍性大腸炎や皮膚の難病などの治療に使われているということで、研究チームは国内での実用化に向けた臨床研究を始めたいとしています。
アメリカ 新型コロナ「回復者血しょう」の緊急使用を許可(8/24)
2020年8月24日
新型コロナウイルスに感染し回復した患者の血液の成分を別の患者に投与する「回復者血しょう」について、アメリカのトランプ大統領は、FDA=食品医薬品局が緊急の使用を許可したと発表しました。
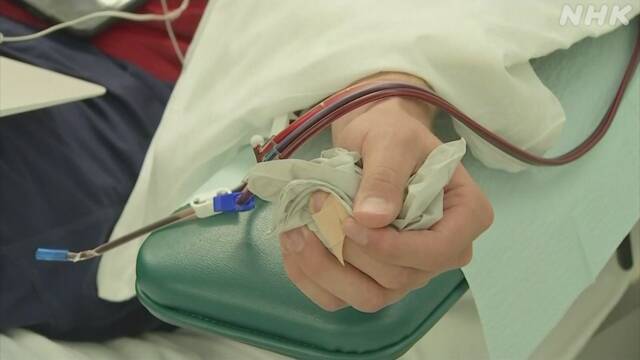
「回復者血しょう治療」と呼ばれるこの治療法は、過去に新型コロナウイルスに感染し回復した人の血液から、ウイルスなどを攻撃する「抗体」が含まれた「血しょう」と呼ばれる成分を取り出して患者に投与するもので、アメリカなどで安全性と効果を確かめる臨床試験が行われています。
トランプ大統領は8月23日の記者会見で、FDAが「回復者血しょう」の緊急の使用を許可すると発表し、「この治療法は多くの命を救うだろう」と効果に期待を示しました。
また、FDAのハーン局長は「すでに7万人以上が回復者血しょうの投与を受けていて、生存率が大幅に改善したという結果も得ている」としたうえで、緊急使用の許可によりより多くの患者がこうした治療を受けられるようになると述べました。
アメリカではウイルスに感染して回復した人に血しょうの提供を呼びかける運動が広がっていて、俳優のトム・ハンクスさんが提供したことでも話題になりました。
「回復者血しょう治療」をめぐっては、日本でも国立国際医療研究センターなどのグループが安全性や効果についての臨床研究を行うなど、各国で研究が進んでいますが、感染者数が少ない国では血しょうの確保が難しいなど、普及させるには課題も残されています。
日本国内でも臨床研究 効果に期待
新型コロナウイルスに感染して回復した患者の血液の成分を、別の患者に投与する「回復者血しょう」を使った臨床研究は、日本国内でも行われ、これまでに回復した人の血液、およそ40人分を採取して、投与の準備が進められています。
国内での臨床研究は、国立国際医療研究センターなどのグループが進めていて、新型コロナウイルスに感染して回復したおよそ50人から1人400ミリリットルの血液の提供を受けて、ウイルスなどを攻撃する「抗体」が含まれた「血しょう」を、患者50人に投与し、安全性や有効性を調べる計画です。
これまでに、およそ40人から血液の提供を受けて、投与に向けた準備を進めているということです。
臨床研究を担当する忽那賢志医師によりますと、この治療法は、酸素吸入などの呼吸管理が必要な中等症以上の患者が対象で、血しょうに含まれる新型コロナウイルスを狙い撃ちにする抗体を使うため、効果が期待されるとしています。
エボラ出血熱や「スペインかぜ」など、ほかの感染症に対しても使われてきた歴史がありますが、血液から必要な成分を分離する専用の装置や、別の感染症に感染しないかなど、安全性を確認する検査も必要で、比較的規模の大きい医療機関でないと実施できないということです。
忽那医師は、アメリカでも有効性を厳密に確認する臨床試験を経ておらず、まだ十分な科学的根拠がないほか、中国では、重症者には有効ではなかったという結果も報告されていて、今後も検証が必要だとしています。
忽那医師は「アメリカでは、すでに多くの人が受けていることもあり、かなり前倒しで緊急に許可したのではないか。特効薬がない中で、有効性が証明できれば意味は大きいため、私たちも実際の患者さんへの投与に向けて計画を進めていきたい」と話しています。
「デキサメタゾン」新型コロナ治療薬に推奨へ 厚労省(7/22)
2020年7月22日
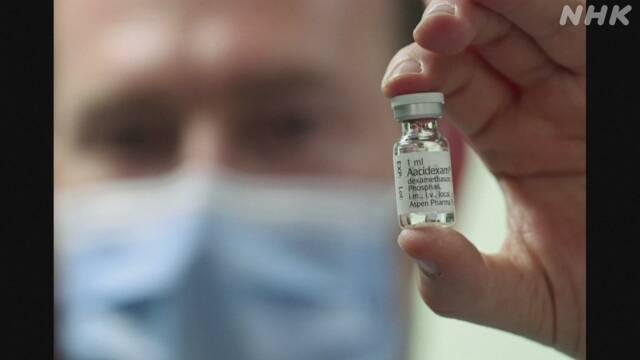
重度の肺炎などに使用されるステロイド剤の「デキサメタゾン」が新型コロナウイルスによる重症患者の治療にも効果があることが海外の研究で確認されたとして、厚生労働省は治療薬として推奨することになりました。
「デキサメタゾン」は、重度の肺炎やリウマチなどに使用されるステロイド剤で、イギリスで行われた臨床試験の結果、新型コロナウイルスによる重症患者の死亡例を減少させたことが6月に明らかになりました。
これを受け、厚生労働省は、新型コロナウイルス感染症の診療ガイドラインに「デキサメタゾン」を新たに掲載しました。
軽症患者については効果が見られなかったということで、重症患者への投与を推奨することにしています。
この薬はすでに重度の感染症や肺炎の治療薬として国内で広く使われているため新たな承認の手続きは必要ありませんが、厚生労働省は治療薬としての周知を図ることにしています。
新型コロナウイルスの治療に使われる薬として有効性が確認されたのはことし5月に特例承認された「レムデシビル」に続き2例目となります。
「アビガン」明確な有効性確認できず 藤田医大など(7/10)
2020年7月10日

新型コロナウイルスの治療薬の候補として期待されている「アビガン」について、患者に投与する臨床研究で明確な有効性は確認できなかったなどとする結果を愛知県にある藤田医科大学などのグループが発表しました。
藤田医科大学などのグループは、ことし3月からインフルエンザ治療薬の「アビガン」を軽症や無症状の入院患者、88人に投与し、有効性や安全性を確かめる臨床研究を行っていて、7月10日、オンラインでの会見で結果を公表しました。
臨床研究は「初日から最長で10日間アビガンを投与するグループ」と、「最初の5日間は投与せず入院6日目以降に投与するグループ」で比較して調べています。
発表によりますと、「初日から投与したグループ」では6日目までにウイルスが検出されなくなった患者は66.7%でしたが、「5日間投与しなかったグループ」では56.1%でした。
また熱が下がるまでにかかった平均の日数は、初日から投与すると2.1日、5日間投与しなかった場合は3.2日だったということです。
研究グループは、入院初日から投与した方がウイルスがなくなったり、熱が下がったりしやすい傾向は見られたものの、統計的に明確な有効性は確認できなかったとしています。
一方、重大な副作用は確認できなかったということです。
土井洋平教授は「早く改善する傾向はあり、有効性がなかったという結論ではないと思う。国には依頼があればデータを提供していきたい」と話しています。
厚労省「申請するかどうかは製薬企業の判断」
「アビガン」について藤田医科大学の臨床研究の結果が示されたことを受け、厚生労働省は、「今回の結果をどう扱うのかや、新型コロナウイルスの治療薬としての承認を今後申請するかどうかは製薬企業の判断だ。申請された場合は厚生労働省として改めて審議する必要がある」とコメントしています。
富士フイルム「発表内容を精査 治験は継続」
「アビガン」については、薬を開発した富士フイルムのグループ会社が新型コロナウイルスの治療薬として、国の承認を目指した治験を進めています。
今回の臨床研究の結果について、富士フイルムは「藤田医科大学の発表内容を精査しています。企業として行っている治験は現在も継続していて、引き続き行っていきます」とコメントしています。
「フサン」と「アビガン」併用投与で症状改善 東大(7/8)
2020年7月8日
新型コロナウイルスに感染して重い肺炎になった患者に、急性すい炎などの治療薬「フサン」を、抗インフルエンザ薬の「アビガン」とともに投与したあと、11人のうち10人で症状が改善したと東京大学のグループが発表しました。グループは、有効性があるかどうかなど、今後さらに確かめたいとしています。
東京大学附属病院はことし4月、新型コロナウイルスに感染して重症化し、集中治療室で治療を受けた患者11人に対し、急性すい炎や体のさまざまな部位に血栓ができる病気の薬「フサン」とともに「アビガン」を併用して投与しました。
投与したあと、人工呼吸器を使っていた75歳の男性1人が死亡しましたが、36歳から71歳の男女10人は症状が改善に向かい、このうち人工心肺装置「ECMO」や人工呼吸器を装着していた7人は、全員が1か月後には自力で呼吸ができるようになったということです。
感染した患者の一部では、血栓ができて症状の悪化につながるという報告が欧米などで相次いでいて、抗ウイルス効果や血液が固まるのを防ぐ効果があるとされる「フサン」について、東京大学附属病院などは患者160人を対象に、安全性と有効性を確認する臨床研究も進めています。
感染制御部の森屋恭爾教授は「フサン単独で効果があるか、ほかの薬と組み合わせて相乗効果を得られるのか、解明を進めたい」と話していてさらに確かめるとしています。
「レムデシビル」の価格 5日間の治療分で約25万円(6/30)
2020年6月30日
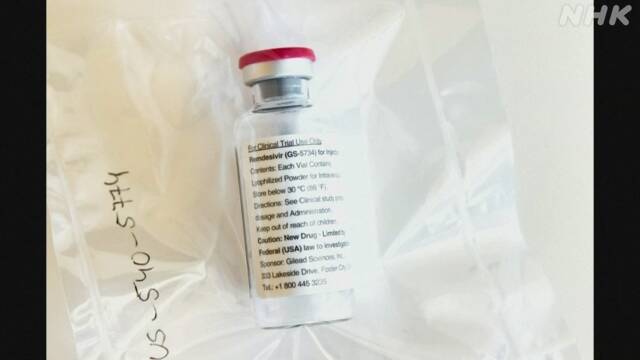
新型コロナウイルスの治療薬として、5月、日本で承認された「レムデシビル」の価格について、開発したアメリカの製薬企業は、5日間の治療に必要な分量を日本円でおよそ25万円に設定したと発表しました。

「レムデシビル」は、アメリカの製薬企業「ギリアド・サイエンシズ」が開発中の薬で、新型コロナウイルスの治療にも効果が期待されていて、5月、日本で治療薬として承認されました。
ギリアド・サイエンシズは6月29日、「レムデシビル」の価格について、患者に1回投与する分量当たり、390ドルとすると発表しました。
一般的な患者は、5日間の治療で6回投与を受けることになるため、合計で2340ドル、日本円でおよそ25万円になります。
この価格は、レムデシビルが承認されたり、使用許可が出たりしている先進国に共通した価格だということです。
一方、発展途上国に対しては、ジェネリック医薬品を製造している企業などと協力し、より低い価格で提供するとしています。
この価格設定についてギリアド・サイエンシズは、レムデシビルの投与で患者の入院期間が4日間短縮できた場合、節約できる医療費は1万2000ドルにのぼるとし「設定した価格は本来の価値を大きく下回る」と述べています。
抗炎症薬「デキサメタゾン」 “新型コロナ死亡率低下” 英大学(6/17)
2020年6月17日
イギリス、オックスフォード大学の研究チームは、炎症を抑える作用のある既存の薬を新型コロナウイルスの複数の患者に投与した結果、一定の割合で死亡率が下がったとする研究結果を発表しました。
オックスフォード大学の研究チームは6月16日、患者6000人余りを対象に行った臨床試験の結果を発表しました。
それによりますと、無作為に選んだ4321人に通常の治療を行った一方、2104人に炎症を抑える作用のあるステロイドの1つ、「デキサメタゾン」という薬を投与した結果、この薬を投与した症状の重い患者で死亡率が下がったということです。
具体的には、気管挿管や気管切開を伴う人工呼吸器をつけた患者でおよそ35%、マスクをつけて酸素を供給した患者でおよそ20%、それぞれ薬を投与しなかった患者に比べて死亡率が下がったということです。
一方、酸素供給を行わなかった患者では、効果は確認されなかったということです。
研究チームのピーター・ホービー教授は会見で「この薬は普通の病院や薬局で手に入り、非常に安い点が重要だ。世界ですぐに使うことができる」と述べました。この結果を受けて、イギリス政府は「デキサメタゾン」を新型コロナウイルスの治療薬として、緊急で承認しました。
また、WHO=世界保健機関のテドロス事務局長は、重症患者の死亡率を下げる効果を示した最初の研究だとして、評価するコメントを出しました。
研究チームは近く、研究結果を論文として発表するとしています。
専門家「非常に重要な成果」
「デキサメタゾン」について、感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は「患者が重症化する際にはウイルスが肺の中で大量に増えるほかに、免疫の仕組みが暴走する『サイトカインストーム』によって、肺の障害や多臓器不全などが進むと考えられている。デキサメタゾンは血液中に投与して免疫の働きを抑えるステロイド剤で、免疫の暴走が抑えられた可能性があり、非常に重要な成果だと思う」と評価しています。
一方で、この薬の注意点として「免疫を抑えるとウイルスが増殖してしまうおそれがある。この薬にはウイルスを抑える効果はないので、ウイルスを抑える薬との併用が必要になってくる」と指摘しています。
この薬は、国内でも喘息などのアレルギー性の病気やリューマチ、それに、さまざまな皮膚の病気や血液のがんなど、多くの病気の治療に使われています。
新型コロナウイルスに感染した患者への国内での使用について森島客員教授は「国内でも免疫の暴走を抑える治療を優先すべきと考えられる重症の患者には、医師の判断でデキサメタゾンを含めたステロイド剤の投与が行われている。今回のように臨床試験の結果が出てくれば、現場の医師がこの薬を使いやすくなると考える」と話しています。
トランプ大統領も服用の治療薬 使用許可取り消し(6/16)
2020年6月16日
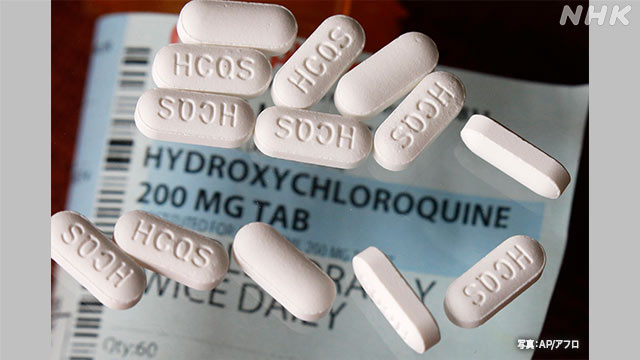
アメリカFDA=食品医薬品局は新型コロナウイルスの感染症の患者に緊急的な使用を認めてきたマラリアなどの治療薬「ヒドロキシクロロキン」に関して、検証の結果、治療効果はみられないとして、使用許可を取り消すと発表しました。
FDAはアメリカで感染が急拡大していた2020年3月、緊急的な措置として新型コロナウイルスによる感染症の患者にマラリアなどの治療薬として広く使われている「ヒドロキシクロロキン」や「クロロキン」の使用を許可しました。
これについてFDAは6月15日、「さまざまな研究を検証した結果、新型コロナウイルスの感染症への治療効果はないとみられ、心臓などへの深刻な副作用もみられる」として、使用許可を取り消すと発表しました。
「ヒドロキシクロロキン」はアメリカのトランプ大統領がみずから服用しているとして注目されましたが、その後、各国での臨床試験で新型コロナウイルスの感染症への治療効果に否定的な結果が相次いで示されていました。
一方でこの薬を巡っては5月、イギリスの医学雑誌に掲載された「治療効果は認められない」とする論文がデータの問題を理由に撤回され、WHO=世界保健機関も一度は中断するとした臨床試験の再開を発表するなど混乱も起きていて、治療薬をめぐる検証の難しさも浮き彫りになっています。
「アビガン」承認に向けた臨床試験 予定より遅れる(6/11)
2020年6月11日

新型コロナウイルスの治療薬の候補「アビガン」について、承認に向けた製薬会社による臨床試験が当初の予定より遅れ、7月以降も続けられる見通しとなりました。
「アビガン」は日本の製薬会社が開発した新型インフルエンザの治療薬で、新型コロナウイルスについても主に軽症の患者への治療薬として期待されていて、政府は手続きを大幅に短縮して当初、5月中の承認を目指すとしていました。
製薬会社は国内で96人の患者を対象にことし3月から6月末まで承認に向けた臨床試験=治験を行う計画でしたが、会社によりますと、治験は予定より遅れ7月以降も続けられる見通しとなりました。
感染者が少なくなり、治験の対象となる人が少なくなったことなどが理由だとしています。
アビガンについては、ほかにも愛知県にある藤田医科大学などで86人の患者を対象に臨床研究が行われていますが、今のところ有効性は判断できないとして、8月末までには臨床研究を終えたいとしています。
一方、安全性については動物実験などで胎児への副作用の可能性が指摘されていますが、これまでに医師による観察研究で投与された3000人余りにそのほかの深刻な副作用は報告されていないということです。
厚生労働省は治験や研究などで薬の有効性を確認したうえで承認手続きを進める考えです。
新型コロナ 治療薬の現状は(6/11)
2020年6月11日
新型コロナウイルスの治療薬については、これまでにアメリカの製薬会社が開発した「レムデシビル」が「特例承認」の制度で承認され、重症の患者などに限定して使用されることになっています。
このほかにも「アビガン」のように、ほかの病気に使われている既存の治療薬を新型コロナウイルスの治療に応用するための研究が国内で進められています。承認に向けた「治験」や、薬を投与し患者の状態を観察する「観察研究」、未承認の薬の有効性や安全性を調べる「臨床研究」などが行われています。
●オルベスコ
ぜんそくの治療薬「オルベスコ」は初期の患者に使うことで重症化を防ぐ効果が期待されていて、観察研究のほか、国立国際医療研究センターで90人を対象に臨床研究も進められています。
●フサン
すい炎などの治療薬の「フサン」はウイルスの増殖を防ぐと共に、血栓を予防し重症化を防ぐ可能性もあるとして、観察研究や、東京大学の研究グループによる臨床研究が進められています。
●フオイパン
同じくすい炎などの治療薬「フオイパン」もウイルスの体内への侵入を抑えられる可能性があるとして、製薬会社が治験を始めています。
●アクテムラ
関節リウマチなどの治療薬「アクテムラ」は新型コロナウイルスによる免疫の暴走を押さえる効果が期待されていて、製薬会社が国内外で治験を進めています。
●その他
このほか、寄生虫による感染症の治療薬「イベルメクチン」も北里大学での臨床研究が予定されています。
また、エイズの発症を抑える「カレトラ」も国内の流行早期に観察研究が行われましたが、これまでのところ十分な効果は確認されていません。
ヒドロキシクロロキン コロナ治療に効果なしとする論文を撤回(6/5)
2020年6月5日
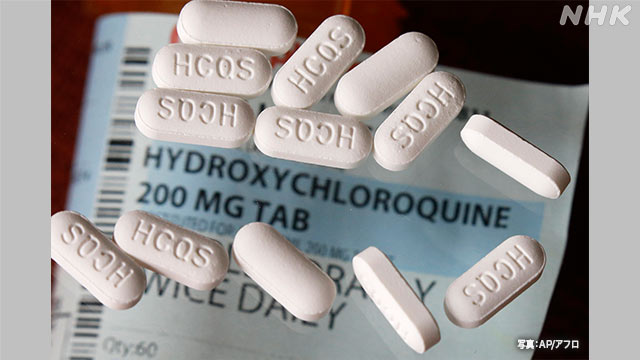
新型コロナウイルスの治療に効果があるかどうか世界各地で臨床試験が行われているマラリアなどの治療薬「ヒドロキシクロロキン」について、治療の効果は認められなかったと5月発表した研究グループがデータの真実性を確認できないとして論文を取り下げたことを明らかにしました。

マラリアなどの治療薬として知られる「ヒドロキシクロロキン」や「クロロキン」について、アメリカやスイスの研究グループはおよそ9万6000人分の患者のデータを分析した結果、新型コロナウイルスの治療について、「効果は認められなかった」とする論文を5月、イギリスの医学誌「ランセット」に発表しました。
ところが、研究グループは分析に使われたデータに問題があるという指摘を受けたため外部の専門家に検証を依頼していました。
研究グループによりますと、専門家が患者のデータを提供した会社にデータ全体を公開するよう求めたところデータの提供者との合意に反するとして拒否されたということです。
このため研究グループのうち3人の研究者が「データの真実性を確認できない」としてこの論文を取り下げると発表しました。
「ランセット」の編集部によりますと、今回の研究にデータを提供した会社はほかにも複数の研究にも関わっています。
研究の中には2015年にノーベル医学・生理学賞を受賞した北里大学の大村智特別栄誉教授が発見した物質をもとに開発された「イベルメクチン」が、新型コロナウイルスの患者の死亡率を下げたと報告したアメリカの大学の研究も含まれていて、「ランセット」は「これらのデータの真実性について国際的な調査が必要だ」としています。
米医学誌に掲載の論文も取り下げ
データの真実性に問題を指摘された会社は、5月発表された心臓の疾患と高血圧の薬などとの関係を分析した論文を発表した研究グループにも患者のデータを提供していました。
この論文を掲載したアメリカの医学誌「ニューイングランド・ジャーナル・オブ・メディシン」は4日、研究グループが「オリジナルのデータを参照することが認められなかった」として、論文を取り下げたことを明らかにしました。
北里研究所「コメントする立場ではない」
今回撤回された論文で、データを提供した会社が関わった研究には、ノーベル医学・生理学賞を受賞した北里大学の大村智特別栄誉教授が発見した物質をもとに開発された、寄生虫による感染症の特効薬「イベルメクチン」が、新型コロナウイルスの患者の死亡率を下げたと報告した、アメリカのユタ大学の研究も含まれています。
北里大学は、イベルメクチンが新型コロナウイルスの治療に効果があるかどうか、患者に投与して調べる治験を計画しています。
北里大学の学校法人、北里研究所の広報は「イベルメクチンの有効性を確認するため、本学において医師主導治験を行う予定です。ユタ大学のデータはあくまで観察研究として拝見しています。その科学的詳細はわからないので、われわれはコメントする立場ではありません」としています。
WHO「ヒドロキシクロロキン」の臨床試験再開へ(6/4)
2020年6月4日
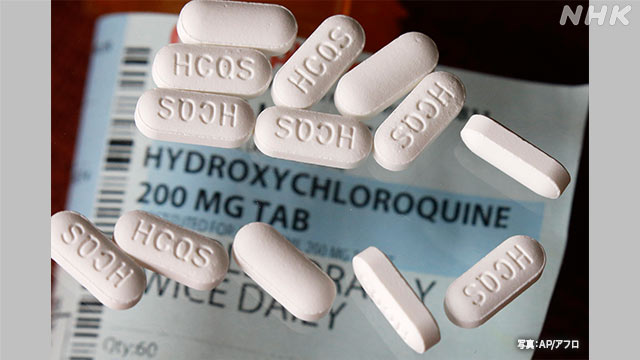
WHO=世界保健機関は、新型コロナウイルスの治療への効果の可能性が指摘されてきた、マラリアなどの治療薬について、臨床試験を中断していましたが、薬を投与することで死亡率が上がるデータはないとして、再開することを明らかにしました。
マラリアなどの治療薬「ヒドロキシクロロキン」は、新型コロナウイルスの治療への効果の可能性が指摘され、WHOは臨床試験を行ってきましたが、アメリカとスイスの研究グループが、投与された患者の一部に心拍の異常が見られたとする研究結果を発表したことを受けて、5月25日、臨床試験を中断したと明らかにし、安全性に関するデータを調査してきました。
WHOのテドロス事務局長は6月3日、スイスのジュネーブにある本部で開いた定例の記者会見で、「臨床試験の安全性を監視している委員会は、計画を変える理由はないと勧告し、これを受けてヒドロキシクロロキンを含めた臨床試験を続けることにした」と述べ、臨床試験を再開することを明らかにしました。
WHOのチーフサイエンティストのスワミナサン氏は、薬の投与によって死亡率に変化はなかったとしています。
このほかテドロス事務局長は、感染が新たに確認された人の数は過去5日間連続で10万人を超えているとしたうえで、「ここ数週間、アメリカ大陸での新たな感染者数は、世界のほかの地域の合計を超えている」と述べる一方、「ヨーロッパでの新たな感染者数は減り続け、きのう報告を受けた数は、3月22日以降最も少なかった」と述べ、ヨーロッパで爆発的に感染が広がる前の時期の水準に戻っていることを明らかにしました。
記者会見では… 中国との関係について質問相次ぐ
AP通信は6月2日、WHOは、中国の対応に不満を持ちながらも、協力を得るために、表向き、中国を評価するような態度をとったことがうかがえると、独自に入手した会議の録音など内部情報をもとに報じ、6月3日のWHOの定例記者会見では、この点に関する質問が相次ぎました。
これについて、危機対応を統括するライアン氏は「WHOのルールに従って、加盟国を等しく支援し、情報を共有するために昼夜問わず仕事をしてきたことを伝えたい」と述べるにとどめました。
内部情報に関する質問はその後も相次ぎましたが、会見の司会を務めるヤシャレビチ報道官は、いずれについても「すでに答えているので、次の質問に移りましょう」と述べ、追加の質問を受け付けませんでした。
ぜんそく薬「オルベスコ」臨床研究 有効性の検証へ 新型コロナ(5/29)
2020年5月29日

新型コロナウイルスの治療薬として期待されているぜんそく薬の「オルベスコ」について、国立国際医療研究センターは薬を投与する患者と投与しない患者に分けて比較する臨床研究を行い、有効性の検証を進めていることを明らかにしました。
新型コロナウイルスに対する特効薬はなく、世界各国で既存の薬に有効性があるかどうか確かめる治験や臨床研究が行われています。
東京 新宿区にある国立国際医療研究センターは29日、オンラインで開いたセミナーで、吸い込むタイプのせんそくの治療薬「オルベスコ」について、患者に投与して有効性を確かめる臨床研究を進めていることを明らかにしました。
臨床研究は、軽症の患者90人を薬を使う患者と使わない患者に分けて、1週間後にCT検査で肺炎の症状を比較する計画で、すでに26人が登録されているということです。
臨床研究は10月末まで行われ、有効性を判断したいとしています。
杉山温人病院長は「複数の医療機関で患者の症状が改善したという報告はあるものの、有効性は科学的に証明されていない。しっかりと検証したい」と話しています。
またセンターでは全国で入院した患者について、医師らが症状の経過や受けた治療などを登録するデータベースを構築していることも明らかにしました。
すでに1500人余りが登録されているということで、詳しく分析して、予防や治療の開発に役立てることにしています。
レムデシビル 投与期間 5日間と10日間大差なし 新型コロナ(5/28)
2020年5月28日

新型コロナウイルスの治療薬として5月、日本で承認されたレムデシビルは、投与する期間が5日間でも、10日間投与する場合と大きな違いはないとする研究結果が公表されました。
エボラ出血熱の治療薬としてアメリカで開発されたレムデシビルは、5月5日、世界で初めて、日本で新型コロナウイルスの治療薬として承認されましたが、各国では安全性や有効性を確かめる複数の臨床試験が続いています。
こうした中、レムデシビルの製薬会社ギリアド・サイエンシズは、新たな臨床試験の結果をまとめ、論文は27日、アメリカの医学雑誌「ニュー・イングランド・ジャーナル・オブ・メディシン」に掲載されました。
それによりますと、薬の投与を始めてから2週間以内に退院した患者の割合は、投与が5日間の場合は、患者200人のうち120人で全体の60%、投与が10日間の場合は、患者197人のうち103人で全体の52%でした。
また、退院までの期間はそれぞれ中央値で、投与が5日間の場合は7日、10日間の場合は8日でした。
論文では、「今回の研究では薬がどの程度効果を示したのかはわからない」としたうえで、分析の結果、薬の投与期間が5日間でも、10日間投与する場合と、回復の経過などに大きな違いはなかったと結論づけています。
新型コロナウイルスの治療薬としての安全性や有効性を確かめる国際共同治験の最終的な結果はまだ明らかになっておらず、その結果に注目が集まっています。
「アビガン」5月中の承認見送り 臨床研究を続ける必要 厚労相(5/26)
2020年5月26日

新型コロナウイルスの治療薬の候補、「アビガン」について、加藤厚生労働大臣は、有効性を確認するための臨床研究を続ける必要があるとして、目標としていた5月中の承認を見送る考えを明らかにしました。
「アビガン」は、日本の製薬会社が開発した新型インフルエンザの治療薬で、政府は、臨床研究などで、有効性と安全性が確認されれば、手続きを大幅に短縮して5月中に承認することを目指していました。
加藤厚生労働大臣は記者会見で「臨床研究の結果を評価する第三者委員会が、科学的に有効性を評価するのは時期尚早との考え方を示したと承知している。6月以降も臨床研究や治験を継続する」と述べ、5月中の承認を見送る考えを明らかにしました。
そのうえで「これまでの観察研究で3000人以上に投与が行われたが、安全性に関して問題となる新たな副作用は報告されていない。有効性が確認され次第、迅速に薬事承認を行う方針には全く変わりない」と述べました。
菅官房長官「有効性など確認なら迅速に承認」
菅官房長官は閣議のあとの記者会見で、5月中の承認を目指していた「アビガン」について「引き続き、6月以降も研究を継続し、企業から承認申請があればデータに基づいて速やかに審査を行い、有効性や安全性が確認されれば迅速に薬事承認を行う方針に変わりはない」と述べました。
またワクチンの開発について「国内では東京大学などで開発が進められており、早ければ7月には治験が始まる予定だ。ワクチン開発の官民プラットフォームへの資金供出など国際社会と協力しながら、第2次補正予算案での対応を含め、ワクチン開発をしっかり進めていきたい」と述べました。
そのうえで「いまだ有効な治療薬やワクチンが見つかっていない疾病について、治療薬やワクチンの開発と成果が特定の企業や国に限らず広く共有されることを目指して、国際的に特許権をプールする構想をG7各国に提案している。世界中で開発が促進されることを期待するとともに日本が開発をリードしたい」と述べました。
新型コロナ治療薬 臨床試験は約1000件 その結果は?(5/24)
2020年5月24日

世界中の研究機関や製薬企業が新型コロナウイルスの治療薬の研究を急ぐ中、候補となる薬の効果を確かめるための臨床試験の結果が出始めていて、治療法の確立につながるか注目されます。
新型コロナウイルスをめぐっては、別の病気の治療のために開発された薬に治療効果が認められないか臨床試験が進められています。
このうち、アメリカの製薬企業「ギリアド・サイエンシズ」がエボラ出血熱の治療薬として開発中だった「レムデシビル」は5月、臨床試験の一部の結果をもとに、アメリカで緊急の使用許可が出されました。
5月22日に発表されたNIH=アメリカ国立衛生研究所などによる臨床試験の初期段階の結果では、患者が退院できる状態になるまでの期間を短縮する効果が見られたとしています。
一方、マラリアなどの治療薬として広く使われている「ヒドロキシクロロキン」は、治療薬となる可能性が指摘され世界中で広く使われましたが、5月22日に発表された大規模な患者の分析では効果は認められなかったと報告されています。
このほか、アメリカの製薬企業などがウイルスの抗体を薬にしたものや、回復した患者の血しょうから作る免疫グロブリン製剤などの開発を進めていますが、臨床試験の開始はこの夏以降になる見通しです。
アメリカなどでは、感染者の増加がゆるやかになりつつありますが、再び感染者が増え始めた場合に備えて薬の効果の検証が急務となっています。
開発中の治療薬 現状は
新型コロナウイルスの治療法についてまとめている民間の団体によりますと、5月22日現在、治療効果を確かめるための薬の臨床試験は世界でおよそ1000件、行われています。
これまでアメリカの製薬会社が開発した「レムデシビル」がアメリカで緊急使用が認められ、それを受けて国内でも特例承認の制度を使って承認されました。ただ、副作用など安全性についての情報がまだ限られていることなどから、重症の患者などに限定して慎重に使用されることになっています。このほかに国内や海外で進められている薬や治療法の研究の現状はー。
<アビガン>
日本の製薬会社が開発した新型インフルエンザの治療薬「アビガン」は、遺伝子のRNAが増えるのを妨げてウイルスの増殖を防ぐ働きがあり、新型コロナウイルスでも同じ仕組みで効果があると期待されています。
これまでに中国などで一定の効果が認められたとする研究結果が報告されていますが、日本国内では、企業による治験や、全国の40余りの医療機関が参加する臨床研究などが進められているところで、まだ有効性などについて結果は出ていません。
政府は5月中の承認を目指し、手続きを短縮して審査を進める方針を示していますが、効果や安全性を慎重に見極めるべきとする声もあり、今後、企業の治験や、臨床研究の結果が注目されています。
<オルベスコ>
ぜんそくの治療薬、「オルベスコ」は国立感染症研究所が新型コロナウイルスに対して効果がある可能性を見つけた薬で、初期の患者に使うことで重症化を防ぐ効果が期待されています。
300人以上を対象にした観察研究の結果が近くまとまる見込みで、ほかにも国立国際医療研究センターでも臨床研究が進められています。
<フサン>
東京大学の研究グループが新型コロナウイルスの増殖を抑える可能性を見つけ出した「フサン」、一般名「ナファモスタット」は、すい炎や全身で血栓ができる病気の治療薬として国内で長く使われてきました。
新型コロナウイルスは血液の塊、「血栓」ができやすくなり、重症化するという報告があり、グループでは「フサン」を使うことで、ウイルスの増殖を防ぐとともに、血栓を予防できる可能性もあるとして臨床研究を進めています。
<イベルメクチン>
このほか、2015年にノーベル医学・生理学賞を受賞した北里大学の大村智特別栄誉教授が発見した物質をもとに開発された「イベルメクチン」も効果が期待されています。
本来は寄生虫による感染症の特効薬ですが、アメリカの大学がこの薬を新型コロナウイルスの患者に投与して死亡率が下がったという報告があり、北里大学が今後、臨床研究を行うことにしています。
<リウマチ薬・アクテムラ>
日本の研究者の成果をもとに開発された関節リウマチなどの治療薬「アクテムラ」は、新型コロナウイルスによる免疫の暴走を抑える効果が期待されています。
新型コロナウイルスでは一部の患者で免疫の仕組みが暴走する「サイトカインストーム」が起こり、重症化するとされていて、「アクテムラ」を使うことで症状の改善につながる可能性があるということです。
開発した製薬会社では効果を確かめる治験を国内で行うと発表したほか、海外でも治験が進められています。
<そのほか>
このほか、エイズの発症を抑える「カレトラ」や、マラリアなどの治療薬、「ヒドロキシクロロキン」なども研究されていますが、これまでのところ十分な効果は確認されていません。
ほかの病気の治療薬に期待
新型コロナウイルスは、当初は発熱やせきなどいわゆる「かぜ」の症状で、8割程度の人は特別な治療をしなくてもそのまま治るとされています。
ただ、肺炎になるなどして重症化すると、人工呼吸器や集中治療室での治療が必要で、死亡する人も出てくることから、重症化を防ぐ治療薬の開発が求められています。このため、世界中で新型コロナウイルスの治療薬の開発が急ピッチで進められています。
最近、注目されているのは一から新たな薬を開発するのではなく、これまで、ほかの病気の治療薬として開発が進められていたり、すでに実用化されていたりする薬の中から新型コロナウイルスへの効果を捜し出す方法です。
こうした薬では、すでに人に使用されていたり、副作用の情報が集められていたりすることから、新型コロナウイルスに対しての効果や安全性を改めて確かめる必要はあるものの、新たな薬を開発するのに比べて実用化が迅速に進むと期待されています。
専門家「第2波までに準備を」
感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は、新型コロナウイルスに対する治療薬の開発について「薬として実用化するには適切な臨床研究の形で効果を確かめることが絶対に必要だ。今、候補になっている薬ではアビガンがいちばん早く結果が出ると考えている。また、オルベスコも6月以降、結果が出てくるとみられ、フサンやアクテムラなどもスピード感を持って研究が進んでいる。感染の第2波、第3波が来ると言われているので、それまでにしっかりと準備をしておく必要がある」と話しています。
一方で、森島客員教授は「いま研究されている治療薬は、すべて既存薬から捜し出していて、新型コロナウイルスに特化して開発された薬ではないため一定の限界がある。長所と短所を理解したうえで使っていくことが重要だ」と指摘しました。
クロロキンは新型コロナ治療に「効果認められず」研究結果(5/23)
2020年5月23日
この論文はその後、撤回されました。
「ヒドロキシクロロキン コロナ治療に効果なしとする論文を撤回(6/5)」をご覧ください。

新型コロナウイルスの治療に効果がある可能性があるとして、研究が行われているマラリアなどの治療薬「クロロキン」について、「効果は認められない」とする大規模な患者を対象にした研究結果が発表されました。
マラリアなどの治療薬「クロロキン」は、新型コロナウイルスの働きを抑える可能性が指摘されたことから、アメリカでは新型コロナウイルスの患者に対しての緊急の使用許可が出るなど、すでに医療現場でも使われていますが、患者に対する効果はまだ実証されていません。
アメリカやスイスの研究グループは、2019年12月20日から4月14日までに、新型コロナウイルスに感染して入院した患者、9万6000人余りのデータを分析した結果を発表しました。
このうち「クロロキン」、または性質が近い「ヒドロキシクロロキン」を投与された患者はおよそ1万5000人、投与されていない患者はおよそ8万1000人で、致死率は「クロロキン」を投与された患者は16.4%、「ヒドロキシクロロキン」の場合は18%だったのに対し、投与されていない患者は9.3%で、投与された患者のほうが高かったということです。
また、抗菌薬を併せて投与された場合では、致死率は「クロロキン」が22.2%、「ヒドロキシクロロキン」が23.8%と、さらに高くなったということです。
研究グループは入院した時の症状の重さや患者の持病などの影響を踏まえて分析をしても、「クロロキン」や「ヒドロキシクロロキン」に治療の効果は認められなかったとしています。
また、「ヒドロキシクロロキン」と抗菌薬を並行して投与された患者では、8%の人に心拍の異常がみられたということです。
「クロロキン」や「ヒドロキシクロロキン」の新型コロナウイルスへの治療効果については、5月に入って否定的な研究結果が相次いで発表されています。
「レムデシビル」に回復期間の短縮効果か 新型コロナ(5/23)
2020年5月23日

新型コロナウイルスの治療薬として期待されている「レムデシビル」について、NIH=アメリカ国立衛生研究所などの研究グループは、患者の回復期間を短縮する効果が見られたとする臨床試験の結果を発表しました。
「レムデシビル」は、実験で新型コロナウイルスの増殖を抑える効果がみられたことから、患者の治療に使える可能性があるとして、臨床試験が進められています。
5月22日、NIHなどの研究グループは、アメリカの医学雑誌「ニューイングランド・ジャーナル・オブ・メディシン」に臨床試験の初期段階の結果を発表しました。
試験は主に症状の重い患者およそ1000人を対象に行い、レムデシビルを投与するグループと、そうでないグループに分け、薬を10日間投与したあと、およそ4週間にわたり経過を観察しました。
その結果、退院できる状態になるまでの期間の中央値は、レムデシビルを投与されたグループが11日で、投与されなかったグループの15日より4日短かく、患者の回復期間を短縮する効果が見られたとしています。
また、試験開始から14日後に死亡した患者の割合は、レムデシビルを投与した患者のグループのほうが低くなりましたが、投与されなかったグループと大きな違いはなかったということです。
こうした結果から研究グループは「レムデシビルの有効性が示された」としたうえで、人工呼吸器が必要になる前に投与を開始することや、致死率を下げるためにレムデシビルの投与と並行して行うべき、ほかの治療法の開発が必要だとしています。
レムデシビルはすでにアメリカで緊急使用の許可が出ているほか、日本ではアメリカでの許可に基づいて、治療薬として承認されています。
アビガン「有効性判断には時期尚早 臨床研究継続」新型コロナ(5/20)
2020年5月20日
新型コロナウイルスの治療薬の候補として期待されている「アビガン」について、国内で行われている臨床研究ではこれまでのところ、有効性については判断できず、さらに臨床研究を進めて検証する必要があることが分かりました。
アビガンは日本の製薬会社が開発した新型インフルエンザの治療薬で、中国政府はことし3月、臨床研究で新型コロナウイルスへの効果が認められたと発表し、日本国内でも有効性や安全性を確かめるための臨床研究や治験が行われています。
このうち、国内での臨床研究は、愛知県にある藤田医科大学など複数の施設に入院している軽症や無症状の患者86人を対象に入院初日から最長で10日間アビガンを投与する人たちと入院6日目以降に投与する人たちに分けて、ウイルスが6日目の時点で減っているかどうか比較するという方法で行われています。
臨床研究は、第三者の委員会が評価することになっていて、関係者によりますと、半分に当たる患者40人余りについての中間段階での解析の結果、「有効性の判断には時期尚早のため、臨床研究を継続すること」とする意見が出されたということです。
中間段階で明らかな効果か安全性への懸念がある場合には研究を中断するよう求める意見が出されますが、この段階では、有効性を評価するにはさらに研究を継続する必要があるという結論になったとしています。
アビガンについて厚生労働省は、5月中に治療薬として承認するため手続きを大幅に短縮して審査を進める方針だとしています。
菅官房長官「有効性確認なら5月中の承認目指す」
菅官房長官は、午前の記者会見で「現在、観察研究、臨床研究、企業による治験が進められていると承知している。企業からの承認申請があればデータに基づき速やかに審査を行い、審議会での専門家の議論を経て有効性・安全性が確認されれば、5月中の承認を目指す考えに変わりはない」と述べました。
新型コロナ治療薬の候補 “臨床試験通じて投与を” 日本医師会(5/19)
2020年5月19日
新型コロナウイルスの治療薬の候補について、日本医師会の有識者会議は、拙速に特例的な承認を行うのではなく、臨床試験などを通じて安全性に注意して投与すべきだとする緊急の提言を出しました。
新型コロナウイルスの特効薬は現時点でないため、患者に対して新型インフルエンザの治療薬「アビガン」など、ほかの薬の投与が治験などの枠組みで行われています。
こうした中、日本医師会の有識者会議は5月18日、治療薬開発について緊急の提言を出しました。
提言の中では、「有事であるため、新薬承認を早める特例措置は理解するところであるが、安全性や有効性の証明が不十分でも良いということには断じてならない」として、新型コロナウイルスは自然に回復する患者もいることから、多くの患者を対象とした適切な臨床試験が必要だとしています。
そのうえで、赤ちゃんに深刻な障害を引き起こしたサリドマイドなどの薬害を忘れてはならないとして、拙速に特例的な承認を行うのではなく、科学的に安全性や有効性が証明されるまでは臨床試験などを通じて投与すべきだとしています。
提言作成に関わった国立国際医療研究センターの國土典宏理事長は、「既存の薬でも副作用の情報が十分ではないものもある。一度承認されると本当に有効なのか確認が難しくなるので、科学的に適切な方法で進めていくべきだ」と話しています。
東大 新型コロナウイルスの治療薬候補 フサンの臨床研究始める(5/8)
2020年5月8日
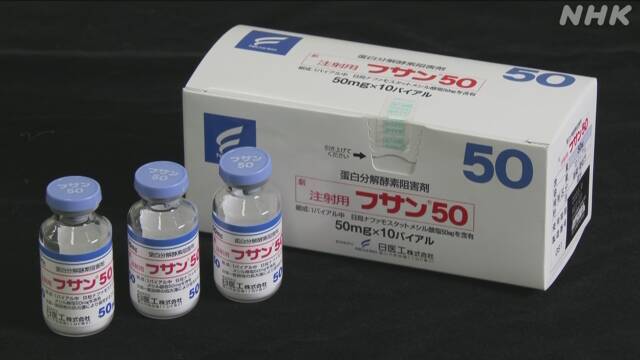
新型コロナウイルスの治療薬の候補で、急性すい炎などの治療に使われてきた「フサン」を患者に投与して、安全性と有効性を確認する臨床研究を始めたと東京大学が発表しました。
東京大学は8日、急性すい炎や体のさまざまな部位に血栓ができる病気の治療に使われてきた薬「フサン」、一般名「ナファモスタット」を新型コロナウイルスに感染した肺炎の患者に投与する臨床研究を始めたと発表しました。
臨床研究は、東京大学附属病院など国内の6か所の医療施設で患者160人を対象に行われ、インフルエンザの治療薬「アビガン」とともに「フサン」を投与するグループと、「アビガン」だけを投与するグループに分けて、安全性と有効性を確かめるということです。
東京大学は新型コロナウイルスを使った実験から、「フサン」にウイルスの増殖を抑える効果が期待できることが示されたとしています。
また、患者の一部では、血栓ができることが症状の悪化につながっているとする報告もあることから、研究グループは、血液が固まるのを防ぐ作用がある「フサン」の効果が期待できるとしています。
効果がある可能性を示した東京大学の井上純一郎特命教授は「成果の発表から最速で臨床研究に入れたと思っている。多くの患者に薬が届くよう結果に期待したい」と話しています。
新型コロナウイルスの治療薬に「レムデシビル」承認 国内初(5/7)
2020年5月7日

新型コロナウイルスの治療に効果が期待されている「レムデシビル」について、厚生労働省は国内初の治療薬として承認しました。重症患者に限定して提供されるということです。
承認されたのは、新型コロナウイルスの治療薬としてアメリカの製薬会社「ギリアド・サイエンシズ」が申請していた「レムデシビル」です。
「レムデシビル」はエボラ出血熱の治療薬として開発が進められてきましたが、新型コロナウイルスの治療にも効果が期待されていて、アメリカでは5月1日、重症患者に対する緊急的な使用が認められました。
日本国内でも5月4日に製薬会社から申請され、7日夜、専門家らが出席する厚生労働省の審議会が安全性や有効性などについて議論した結果、承認を認める意見をまとめました。
これを受けて、加藤厚生労働大臣は、審査を大幅に簡略化する「特例承認」の制度を適用し、国内で初めての新型コロナウイルスの治療薬として承認しました。
「レムデシビル」は重症患者への効果が期待されていますが、流通量が限られる中、必要な量を確保できるかが課題となっています。さらに、有効性や安全性に関する情報が極めて限られていることなどから、重症患者に限定して提供されるということです。
レムデシビルとは
レムデシビルはアメリカに本社がある製薬会社「ギリアド・サイエンシズ」がエボラ出血熱の治療薬として開発を進めてきました。
エボラ出血熱の薬としては承認されていませんが、コロナウイルスの一種によって引き起こされたSARSやMERSに対して効果があるとする研究結果が示されていたことから、新型コロナウイルスの治療薬になるのではないかと注目されてきました。
レムデシビルは、新型コロナウイルスがのどの近くの「上気道」と呼ばれる場所で感染して、細胞の中に入り込んだあと、増殖するのを防ぐ作用があるとされています。
ウイルスは、細胞の中で、みずからの「RNA」という遺伝子をコピーして増殖しますが、ウイルスの増殖に必要なRNAのコピーをできなくさせるとしています。
アメリカのNIH=国立衛生研究所は、各国の医療機関が共同で行っている臨床試験の一部を分析した結果、レムデシビルの投与を受けた患者は、回復までの日数が投与されなかった患者よりおよそ4日早い11日で患者の回復を早めることが確認されたとしています。
ただ、効果を示す報告がある一方で、副作用を懸念する声もあります。
日本やアメリカ、ヨーロッパの研究グループが4月、アメリカの医学雑誌に発表した研究結果によりますと、薬を投与したあとで患者53人のうち、68%にあたる36人に改善が見られた一方、23%にあたる12人では、多臓器不全や敗血症、急性の腎臓の障害などの重い症状が出たということです。ほかにも、重くはないものの、肝機能障害、下痢や発疹などの症状も報告されています。
感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は、「国内で難しい手続きを経ずに使うことができるようになり、新型コロナウイルスの治療が一歩前進したことを意味すると思う。ただ、投与した患者に腎臓や肝臓の機能障害も報告されていて、供給量も限られるため、治療の経験を積んでいる医療施設で、重い肺炎の患者に対して使われるべきだ」と話しています。
ほかに検証が進められている薬は
レムデシビル以外にも、別の病気の治療薬が新型コロナウイルスに効果がある可能性があるとして患者への投与が行われ、効果や安全性の検証が進められています。
抗インフルエンザ薬アビガン
このうち、日本の製薬会社が開発したインフルエンザの治療薬「アビガン」は、レムデシビルと同様にウイルスがRNAをコピーするのを妨げる作用があります。
開発した企業が安全性と有効性を確かめる治験を始めていて、国は5月中にも治療薬として承認するため、手続きを大幅に短縮して審査を進める方針です。
また、厚生労働省によりますと、国内の1000あまりの医療機関が参加して、治療薬の効果を分析する「観察研究」が行われていて、4月26日の時点で2194人の患者に投与されているということです。
研究班は、患者に投与したあとで症状の改善が見られたと報告する一方、現時点のデータだけでは有効性を判断することは難しいともしています。
中国政府は、臨床研究でアビガンに症状を改善させる効果が認められたとしています。
開発した企業は、アメリカでも治験を行うことを発表しています。
ぜんそく薬オルベスコ
吸引するタイプのぜんそくの治療薬「オルベスコ」は、国立感染症研究所が多くの薬の候補を調べ、新型コロナウイルスに効く可能性があることを示しました。
4月開かれた日本感染症学会のシンポジウムでは、感染後、肺炎になった患者75人に投与した観察研究の結果、この薬を使わない場合に比べて悪化する割合を下げられる可能性があると報告されています。
すい炎や血栓症の薬フサン
また、すい炎や全身で血栓ができる病気の治療薬として国内で長年使われてきた「フサン」、一般名「ナファモスタット」は、東京大学の研究グループが新型コロナウイルスを使った実験の結果、ウイルスが細胞に侵入するのを妨げ、増殖するのを抑える効果が期待できると発表しました。
現在、東京大学附属病院で、患者に投与して効果を検証する観察研究が行われています。
リウマチ薬アクテムラ
さらに、免疫の異常によって起きる病気の治療薬についても効果の検証が進められています。
日本の研究者の成果をもとにつくられた関節リウマチなどの治療薬「アクテムラ」は、開発した製薬会社が感染して重症の肺炎になった患者に投与して効果を確かめる治験を国内で行うと発表したほか、アメリカなどでも海外の製薬会社が治験を始めています。
新型コロナウイルスに感染すると、一部の患者では、免疫の働きを高める「インターロイキン6」という物質が過剰に作られて免疫の仕組みが暴走し、重症の呼吸器不全が引き起こされると考えられています。
製薬会社は「アクテムラ」によって、「インターロイキン6」の働きを抑えることで、重症化した患者の症状の改善につながるか、確認するとしています。
寄生虫薬イベルメクチン
このほか、2015年にノーベル医学・生理学賞を受賞した北里大学の大村智特別栄誉教授が発見した物質をもとにつくられた「イベルメクチン」も効果を確かめる研究が行われています。
この薬は、寄生虫によって引き起こされる病気の一種に対する特効薬で、新型コロナウイルスに感染した患者に投与すると、死亡率が下がったと、アメリカの大学のグループが報告しています。
北里大学は患者に投与する臨床研究を今後、本格化させる計画を、新型コロナウイルス対策を担当する西村経済再生担当大臣に説明しています。
感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は、「多くの研究がすでにある薬を新型コロナウイルスの治療に応用することを目指すもので、安全性も効果も100点満点の特効薬が出てくることは見込めない。それぞれの薬の持つ長所と短所を見極めながら、医療の現場が使いやすい薬を見つけることが重要だ」と話しています。
アビガン 新型コロナ治療薬承認へ 手続き大幅短縮で審査方針(5/4)
2020年5月4日
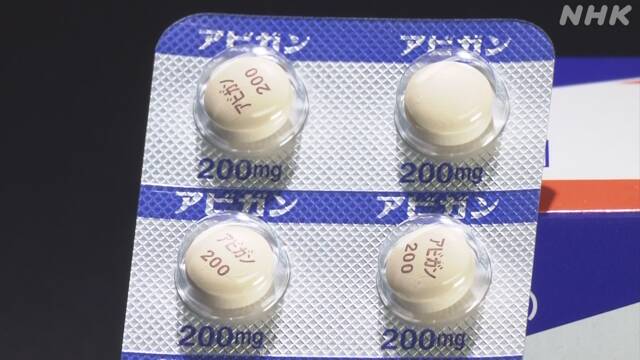
国内の製薬会社が開発し新型コロナウイルスの治療効果が期待されている「アビガン」について、厚生労働省は、5月中に治療薬として承認するため、手続きを大幅に短縮して審査を進める方針です。
新型コロナウイルスの治療薬をめぐって厚生労働省は、すでにアメリカで開発された「レムデシビル」について、海外で使用が認められた薬の国内での審査を簡略化する「特例承認」の手続きを進めていて、週内にも承認される見通しです。
これとは別に日本の製薬会社が開発したインフルエンザの薬「アビガン」も新型コロナウイルスの治療効果が期待されていることから、政府は5月中の承認を目指す方針です。
厚生労働省によりますと、「アビガン」は研究の一環として4日までに国内でおよそ3000人の患者に投与され、愛知県の藤田医科大学病院などで臨床研究なども行われています。
その結果はまだまとまっておらず、海外で使用が認められている「レムデシビル」と異なり「特例承認」を適用することもできませんが、厚生労働省は、通常1年ほどかかる承認の手続きを大幅に短縮して審査を進める方針です。
ただし「アビガン」は、これまでの動物実験などで胎児への副作用の可能性も指摘されています。
厚生労働省は「審査期間は可能なかぎり短くするが、副作用や用量などを慎重に検討して判断する」としています。
「レムデシビル」厚労省 特例承認手続き開始 1週間程度目指す(5/2)
2020年5月2日

新型コロナウイルスへの治療効果が期待されている「レムデシビル」について、厚生労働省はアメリカで緊急的な使用が認められたことを受け、「特例承認」と呼ばれる制度を活用して早期の承認に向けた手続きに入りました。早ければ1週間程度での承認を目指していて、承認されれば国内で初めての新型コロナウイルスの治療薬となります。
「レムデシビル」はエボラ出血熱の治療薬として海外で開発が進められ、新型コロナウイルスにも効果が期待できるとして日本でも臨床試験が進められています。
加藤厚生労働大臣は海外での動向を見ながら、国内でも審査を大幅に簡略化できる「特例承認」と呼ばれる制度を活用して早期の承認を目指す考えを示していました。
こうした中、アメリカ政府が5月1日、緊急的な使用を認めたことから、厚生労働省はレムデシビルの「特例承認」に向けた手続きを始めました。
5月2日午後、レムデシビルに「特例承認」が適用されるよう政令改正に向けた閣議を持ち回りで行うとともに製薬会社からの申請を受け次第、審議会を開いてアメリカ政府に提出された治験のデータについて専門家の意見を求めることにしています。
厚生労働省は早ければおおむね1週間での承認を目指していて、承認されれば国内で初めての新型コロナウイルスの治療薬となります。
一方、レムデシビルは流通量にかぎりがあるため、当面は厚生労働省の管理の下で特定の病院にのみ供給される可能性があります。
「特例承認」とは
「特例承認」は緊急性の高い医薬品について手続きを大幅に簡略化し、早期に承認できる法律上の仕組みです。
健康に重大な影響を与えるおそれがある病気がまん延し、他に治療薬がない場合に、緊急に使う必要がある医薬品が対象で、他に治療薬などがないことや日本と同じような承認制度がある海外の国ですでに販売されていることなどが条件となっています。
これまでに、新型インフルエンザのワクチン2品目について、「特例承認」が行われたことがあります。
「特例承認」をレムデシビルに適用するためには、新型コロナウイルスの治療薬を対象とすることなどの政令の改正が必要ですが、通常は1年程度かかる承認手続きが大幅に短縮でき、厚生労働省は早ければおおむね1週間程度での承認を目指しています。
レムデシビルとは
レムデシビルはアメリカに本社がある「ギリアド・サイエンシズ」がエボラ出血熱の治療薬として開発を進めてきました。
試験管内の実験で、新型コロナウイルスの動きを抑える効果があったことから、治療効果が期待されるようになりました。
このため、日本を含む各国が参加する国際的な臨床試験が行われていて、製薬会社によりますと国内でもおよそ90人に投与されることになっています。
このうち、アメリカの臨床試験では、結果の一部を分析したところ投与された患者がそうではない患者に比べて回復にかかる期間が4日短いことなどが確認されたということです。
こうした試験結果を受け、アメリカでは、緊急的な使用にかぎり、許可されることになりました。
ただ、アメリカの当局は、緊急で使用を認める手続きについては正式な審査を受けた承認とは異なり、効果や安全性については、まだ、限定的な情報しか得られていないとしています。
レムデシビルをめぐっては、腎機能の低下などの副作用も指摘されているほか、イギリスの医学雑誌には、中国での臨床試験の結果「統計上、有意な効果はみられなかった」とする論文が掲載されるなど、海外では評価がわかれています。
専門家「重症患者向け治療薬として期待できるか」
厚生労働省が、レムデシビルの早期の承認に向けた手続きを始めたことについて、感染症の治療に詳しい愛知医科大学の森島恒雄客員教授は、「新型コロナウイルスについてはまだ特効薬がなく、既存の薬の中からよく効く薬を探しているのが現状だ。レムデシビルは、飲み薬ではなく、静脈注射で10日間ほどの期間投与するもので、海外では、これまでに、肺炎を起こして人工呼吸器が必要になるなど、重症の患者に使うことで、ウイルスの増殖を抑える効果が確認されている。国内で承認されれば、主に重症の患者向けの治療薬として期待できるのではないか」と話しています。
その一方で、副作用については「かなりの確率で腎臓に機能障害が出ることがわかっているので、重症の患者を数多く治療している医療機関や薬の扱いに慣れた専門施設などで使われることが望ましい」としています。
米当局 「レムデシビル」緊急使用認める 新型コロナに効果か(5/2)
2020年5月2日

アメリカのトランプ大統領は、新型コロナウイルスに効果があるか研究が進められている薬「レムデシビル」について、薬の審査を行う当局が緊急使用を認めたと明らかにしました。
レムデシビルは、アメリカに本社のある「ギリアド・サイエンシズ」がエボラ出血熱の治療薬として開発を進めてきた薬で、新型コロナウイルスの治療にも効果がある可能性が指摘されています。
トランプ大統領は5月1日、ホワイトハウスで記者団に対して、アメリカで薬の審査を行うFDA=食品医薬品局がレムデシビルの緊急使用を認めたと明らかにしました。
アメリカ政府はレムデシビルの使用を一部で可能にする「拡大使用」をことし1月に認めていますが、緊急使用を認めることによって、重症の患者に対してより広く使用することが可能になります。
トランプ大統領は「非常に期待ができる状況だ。すばらしい結果が出るだろう」と述べ、期待を示しました。
レムデシビルをめぐっては各国で効果や安全性を確認する臨床試験が進められていて、4月にはアメリカのNIH=国立衛生研究所が、新型コロナウイルスの患者への治療効果などを調べる臨床試験の一部を分析した結果、患者の回復を早めることが確認されたと発表しています。
FDAは、緊急で使用を認める手続きについては正式な審査を受けた承認とは異なり、効果や安全性については、まだ限定的な情報しか得られていないとしています。
医師「命を救う可能性持っている」
アメリカで新型コロナウイルスに感染し、「レムデシビル」を投与したという57歳の男性はAP通信の取材に対し、「この薬を投与したことでわずか4日で症状が改善した。他の人にとっても症状の改善につながることを願っている」と述べ、薬の効果を実感したと証言しました。
また中西部ネブラスカ州のネブラスカ大学医療センターでこの薬の臨床試験に関わっているアンドレ・カリル医師はAP通信に対し「この薬を使えば、本来必要だったはずの治療をせずに4日早く退院させることができる。万能薬ではないが患者の症状を改善し、命を救う可能性を持っている」と述べ、「レムデシビル」の使用により一定程度症状が改善するという認識を示しました。
米 新型コロナに有効か 研究進む「レムデシビル」を緊急使用か(5/1)
2020年5月1日

新型コロナウイルスに効果があるか研究が進められている薬「レムデシビル」について、アメリカで薬の審査を行うFDA=食品医薬品局は、患者への使用に向けて迅速に手続きを進める方針を示し、アメリカでは、近く、緊急使用が認められるという見方が強まっています。
「レムデシビル」は、エボラ出血熱の治療のために開発が進められてきた薬で、29日にはアメリカのNIH=国立衛生研究所が、新型コロナウイルスの患者への治療効果などを調べる臨床試験の一部を分析した結果、患者の回復を早めることが確認されたと発表し、注目が高まっています。
こうした中、FDAのスティーブン・ハーン局長は30日、通信社の取材の中で、レムデシビルについて「どのような患者に投与するのが適切か見極めるために、試験結果全体を見たい」としたうえで、患者への使用に向けて「最速で動いている」と述べ、迅速に手続きを進める考えを示しました。
また、NIHで新型コロナウイルス対策を率いるアンソニー・ファウチ博士も30日、テレビ局のインタビューで「手続きは早く進むだろう」と述べました。
トランプ大統領も29日、臨床試験の一部の分析結果について「とても前向きな動きだ」と述べていて、アメリカでは、近く、緊急使用が認められるという見方が強まっています。
厚生労働省 「アビガン」投与の注意事項まとめる 新型コロナ(5/1)
2020年5月1日
新型コロナウイルスの治療効果が期待されているインフルエンザの薬「アビガン」について、厚生労働省は、研究としての投与が2000人あまりに行われたことを明らかにし、今後、投与を希望する医療機関に向けた注意事項をまとめました。
インフルエンザの薬「アビガン」は、新型コロナウイルスの治療薬としては承認されていませんが、効果が期待されていて、愛知県の藤田医科大学病院などの研究班を中心に、全国の医療機関で研究としての投与が行われています。
厚生労働省によりますと、4月26日の時点で、国内1100の医療機関で、2194人の患者に投与されたということです。
一方で、動物実験などで胎児への副作用の可能性が指摘されているため、十分な安全管理対策が必要だとしています。
このため厚生労働省は医療機関に向けた注意事項をまとめました。
それによりますと、アビガンを投与するには、▽医療機関の倫理委員会などで承認を得たうえで、研究班に参加することが条件で、▽患者本人の同意を必ず得ることとしています。
また▽妊婦には投与せず、子どもを持つ可能性がある男女への投与も慎重な検討が必要だとしています。
厚生労働省は、こうした研究のほか、製薬会社による治験の結果などで有効性が確認できれば、承認に向けた審査を進めたいとしていて「1日でも早く、国民の不安を解消できるよう、有効な治療薬の開発を加速していきたい」としています。
「レムデシビル」早期承認目指す考え 加藤厚労相 新型コロナ(4/28)
2020年4月28日
新型コロナウイルスの治療薬の候補の1つである「レムデシビル」について、加藤厚生労働大臣は、緊急の場合に、審査を大幅に簡略化できる「特例承認」と呼ばれる制度を活用して、早期の承認を目指す考えを示しました。
「レムデシビル」は、エボラ出血熱の治療薬として海外で開発中の薬ですが、新型コロナウイルスにも効果がある可能性があるとして、国内外で臨床試験が進められています。
この薬について、加藤厚生労働大臣は4月28日、閣議のあとの記者会見で、「現在の医薬品の承認の仕組みの中には、疾病のまん延防止のため、緊急の使用が必要である場合などに、迅速に承認ができる『特例承認』という制度がある」と述べ、「特例承認」の制度を活用する方針を明らかにしました。
「特例承認」を活用するには、海外で販売が認められることなどが条件となっていて、加藤大臣は、「海外で緊急的に使用される許可がおりた場合は、承認審査を速やかに進めていきたい。いくつかの国で承認の検討が行われており、その結果を踏まえての対応となる」と述べました。
「レムデシビル」の承認の検討は、ドイツやアメリカが先行しているということで、厚生労働省は、これらの国の検討結果が出しだい、早期の承認を目指す方針です。承認されれば国内では初めての新型コロナウイルスの治療薬となる見通しです。
新型コロナ治療でヒドロキシクロロキンの使用に注意呼びかけ(4/25)
2020年4月25日
新型コロナウイルスに感染した患者への治療に効果があるかどうかを調べる臨床試験が行われているマラリアの治療薬「クロロキン」の一種について、アメリカFDA=食品医薬品局は使った患者の一部に心拍の異常などの症状がみられたとして使用にあたって注意を呼びかけました。
マラリアなどの治療薬として知られる「ヒドロキシクロロキン」は新型コロナウイルスの治療に効果がある可能性が指摘され、FDAは3月、緊急での使用を認めたほか臨床試験も行われています。
この治療薬をめぐって、FDAは24日、医師や患者に対し、処方や使用の際に注意を呼びかける文書を公表しました。
それによりますと、使った患者の一部に心拍に異常がみられたという複数の報告があったということで、医師や患者にリスクを理解して使用するよう求めるとともに、さらに詳しく調査するとしています。
また、24日付のイギリスの医学専門誌にも「ヒドロキシクロロキン」と抗菌薬を同時に投与された患者の多くに心拍の異常がみられたとする論文が公表されています。
「ヒドロキシクロロキン」はトランプ大統領が「画期的な薬だ」などと記者会見で述べたことで注目が集まりましたが、実際に効果があるかどうかは、これまでのところ十分に確認されていません。
「回復者血しょう治療」臨床研究開始へ 新型コロナウイルス(4/25)
2020年4月25日

新型コロナウイルスの患者に、感染して回復した人の血液の成分を投与する新しい治療法の臨床研究を国立国際医療研究センターなどのグループが始めることがわかりました。中国では重症患者への効果が報告されていて、担当する医師は「重症患者の治療の切り札になる可能性もある」としています。
この臨床研究は新型コロナウイルスの治療の中核を担う国立国際医療研究センターなどのグループが進めているもので、23日、病院内の倫理委員会で正式に承認されたということです。
「回復者血しょう治療」と呼ばれるこの治療法は、過去に新型コロナウイルスに感染し、回復した人の血液からウイルスなどを攻撃する「抗体」が含まれた「血しょう」と呼ばれる成分を取り出し、患者に投与するもので、中国では症例数は少ないものの重症患者の症状が改善したという報告があります。
計画では、回復した人およそ50人から1人400ミリリットルの血液の提供を受け、血しょうを患者50人に投与し、安全性や効果を調べるということです。
グループでは来週以降、回復した人に血液の提供を呼びかけ、早ければ5月にも患者への投与を始めたいとしています。

臨床研究を担当する忽那賢志医師は「回復した人の抗体を使う治療法はエボラ出血熱などでも効果が出ており、一定の効果がみられると期待している。確実な治療薬がない中で、重症患者の治療の切り札になる可能性がある」と話しています。
新たな治療薬候補になるか 2種類の物質発見 新型コロナ(4/22)
2020年4月22日
新型コロナウイルスの治療薬を開発しようと国内を中心に25の研究機関が集まって進めている共同研究で、エイズの発症を抑える薬など2種類の物質が新型コロナウイルスの増殖を妨げることが発見され、薬の新たな候補になるとして今後、臨床研究の実施を目指すとしています。
新型コロナウイルスの治療薬を開発するため国立感染症研究所や東京理科大学など国内を中心に25の研究機関の専門家は緊急の共同研究を開始しています。
共同研究では日本や欧米で承認されている300種類余りの薬の中から新型コロナウイルスの増殖を妨げる作用があり、薬の候補になるものを調べたところ、エイズの発症を抑える薬である「ネルフィナビル」と白血球が減少する病気などの薬として使われている「セファランチン」の合わせて2種類の物質を見つけたということです。
「ネルフィナビル」はウイルスが増殖する際に働く酵素を阻害し、「セファランチン」はウイルスが細胞に侵入するのを防ぐことがコンピューターによるシミュレーションで推定されたとしています。
そして、発症の半日後にこの2つの物質を同時に患者に投与した場合を推計すると、ウイルスが体内からなくなるまでの期間がおよそ10日間と、何も投与しなかった場合と比べて5日程度早めることができる可能性が示されたということです。
グループは今後、安全性や効果を確かめる臨床研究の実施を目指すとしています。
共同研究の取りまとめをしている国立感染症研究所の渡士幸一主任研究官は「新型コロナウイルスの薬の開発はいくつか臨床研究が進んでいるが、今回の2種類の物質も実験レベルでの効果は高く、新たな候補として提案したい」としています。
日本感染症学会で状況報告「アビガン」「オルベスコ」で改善例も(4/18)
2020年4月18日

新型コロナウイルスの感染が拡大する中、日本感染症学会の緊急シンポジウムが開かれ、患者の治療について、インフルエンザ薬やぜんそく薬の投与で改善したケースもあったことなどが報告されました。今後さらに、効果を見極める必要があるとしています。
日本感染症学会は18日、感染対策のため、観覧者を入れずに講演をインターネットで配信する形で、東京都内でシンポジウムを開き、新型コロナウイルス対策にあたる政府の専門家会議のメンバーや、治療にあたる医師などが状況を報告しました。
新型コロナウイルスには特効薬はなく、別の病気の治療に使われている薬の投与が行われていて、藤田医科大学の土井洋平教授は、インフルエンザ治療薬の「アビガン」を患者に投与した状況について報告しました。
それによりますと、アビガンを投与された300人のうち、軽症と中等症の患者ではおよそ9割、人工呼吸器が必要な重症患者では6割で2週間後に症状の改善が見られたということで、土井教授は現在行われている治験などでさらに効果を確かめる必要があるという考えを示しました。
また、吸い込むタイプのぜんそくの治療薬「オルベスコ」についても報告され、肺炎になったあとで投与された75人のうち、症状が悪化して人工呼吸器が必要になった患者が少なくとも3人、亡くなった患者は2人だったということで、この薬を使わない場合に比べて悪化する割合を下げられる可能性があるとしています。
土井教授は、「既存薬で改善したケースも出てきているが、有効性を確かめるには、薬の投与がない患者との比較や投与するタイミングなどの検証が今後必要だ」と話しています。
「医療崩壊」防ぐうえで重要な役割も
国の研究班の班長としてぜんそく薬の「オルベスコ」を患者に投与する臨床研究に関わる愛知医科大学の森島恒雄客員教授は、「今回のデータだけではまだ断定はできないが、オルベスコを投与することで、重症の肺炎になって人工呼吸器が必要になる患者を減らせる可能性がある。全国で感染拡大が続く中、医療機関で受け入れ可能な患者数を超えて患者を助けられなくなる『医療崩壊』を防ぐうえで、重要な役割を持つ薬と考えられるので、さらに分析を進めたい」と話しています。
エボラ出血熱治療薬「レムデシビル」日本でも治験始まる(4/14)
2020年4月14日

新型コロナウイルスの治療薬の候補の1つとして注目されている、エボラ出血熱の薬として開発中の「レムデシビル」について、開発した製薬企業が、国内の医療機関で実用化を目指して患者への投与を行う治験を、14日から始めたことが分かりました。

「レムデシビル」は、アメリカに本社のある「ギリアド・サイエンシズ」が、エボラ出血熱の治療薬として開発を進めてきた薬で、新型コロナウイルスの治療にも効果がある可能性が指摘されることから、すでに日本やアメリカなどの各国の医師が、共同で実用化を目指した治験を進めています。
ギリアド・サイエンシズでは、レムデシビルの効果について、さらに多くのデータを集めるため、これまでの治験とは別に、新たに横浜市立市民病院など国内の3つの医療機関と連携し、新型コロナウイルスの患者に薬の投与を行う治験を14日から始めたということです。
治験は、日本だけでなく、アメリカやイタリアなどの合わせて4000人を対象に、重症や中程度などのグループに分けて薬の安全性や有効性を確かめるということで、国内ではまず、90人ほどの患者の参加を目指すということです。
「ギリアド社」日本法人の表雅之開発本部長は「5月中には、有効性に関するデータが一定程度得られる見込みだ。1日でも早く治療法の確立に結び付けられるよう治験を進めたい」としています。
エボラ出血熱治療薬「レムデシビル」“コロナ患者 約7割で改善”(4/11)
2020年4月11日

アメリカの製薬会社が開発中のエボラ出血熱の治療薬を新型コロナウイルスに感染した患者に投与したところ、人工呼吸器などを必要とする患者のうち、およそ7割の人で改善が見られたとする報告がアメリカの医学雑誌に発表されました。
アメリカの製薬会社が開発中のエボラ出血熱の治療薬「レムデシビル」は、新型コロナウイルスに感染した患者に効果がある可能性があるとして、人道的な理由から日本や中国など一部の国ですでに投与が始まっています。
日本やアメリカ、ヨーロッパの研究者のグループが、10日付けのアメリカの医学雑誌「ニュー・イングランド・ジャーナル・オブ・メディシン」に発表した報告によりますと、基礎データが確認された入院患者53人を対象にレムデシビルを投与したところ、68%に当たる36人で改善が見られたということです。
具体的には、重症な患者に使われる気管に管を通す「挿管」が必要な人工呼吸器を着けていた30人のうち、17人が挿管を外すことができたほか、人工心肺装置=ECMOを使用していた患者4人のうち3人がECMOを必要としなくなったということです。
研究グループは「重症患者にある程度の効果があることが示唆される」としながらも、今回の研究では患者のウイルス量のデータが得られなかったとして「効果を結論づけるには各国で行われている臨床試験の結果が必要だ」としています。
インフルの治療薬「アビガン」 新型コロナ治療の臨床試験開始(4/1)
2020年4月1日

新型インフルエンザ治療薬、「アビガン」を製造している日本の製薬会社は、新型コロナウイルスの治療薬として国の承認を受けるための臨床試験を始めたと発表しました。
「アビガン」、一般名「ファビピラビル」は、新型インフルエンザの治療薬として、6年前、製薬会社の富士フイルム富山化学が開発したもので31日、新型コロナウイルスの治療のための臨床試験を始めたと発表しました。
臨床試験は東京都内の病院で新型コロナウイルスに感染した患者、およそ100人を対象に6月末まで行われ、治療の効果や安全性を確認するということです。
「アビガン」は動物実験で胎児への副作用が報告されたことから、妊娠中の女性には投与できず、ほかの薬が効かない感染症が発生し、国が使用すると判断した場合に限って投与されることになっています。
すでに中国では、新型コロナウイルスに感染した患者に投与する臨床研究を行った結果、肺炎の症状などを改善させる効果が認められたと報告されています。
日本でも、新型コロナウイルスに対して効果があるかどうか調べる臨床研究が3月から愛知県の藤田医科大学病院などで始まっています。
富士フイルム富山化学は臨床試験の結果、効果や安全性が確認されれば、新型コロナウイルスの治療薬として国に承認申請を行う方針です。
「アビガン」新型コロナ治療薬としての承認目指す 政府方針(3/30)
2020年3月30日
新型コロナウイルスの感染が世界的に広がるなか、政府はインフルエンザ治療薬「アビガン」について、治験プロセスを経たうえで、新型コロナウイルスの治療薬としての正式な承認を目指すことにしており、有効な治療薬の開発に向けて研究を後押しする方針です。
世界的に感染が拡大している新型コロナウイルスをめぐっては、今のところ特効薬はありません。
新型コロナウイルスに対しては、別の感染症などの治療薬が使える可能性があるとして、国内外で効果や安全性の検証が進められていますが、このうち、日本の製薬会社が開発したインフルエンザ治療薬「アビガン」について、政府は治験プロセスを経たうえで、新型コロナウイルスの治療薬としての正式な承認を目指すことにしています。
「アビガン」は、中国で治療効果が認められたとされ、国内でも愛知県の藤田医科大学病院などで臨床研究が始まっていて、政府は、今後、希望する国と協力しながら臨床研究を拡大し、薬の増産も開始する方針です。
また、すい炎の治療薬「フサン」についても、臨床研究として事前に患者の同意を得たうえで投与が始まる予定で、政府は有効な治療薬の開発に向けて研究を後押しすることにしています。
エボラ出血熱治療薬「レムデシビル」臨床試験開始へ(3/23)
2020年3月23日

新型コロナウイルスに感染し、肺炎になった患者の治療に、エボラ出血熱の治療薬として開発が進められた薬が効くかどうか調べる臨床試験を、東京の国立国際医療研究センターが3月中にも始めると発表しました。
これは、新型コロナウイルスに感染した患者への治療を行っている国立国際医療研究センターの大曲貴夫国際感染症センター長が説明会を開いて明らかにしました。
それによりますと、臨床試験では新型コロナウイルスに感染し、肺炎か、酸素の吸入が必要な状態になった入院患者に対して、アメリカの企業がエボラ出血熱の治療薬として開発を進めてきた抗ウイルス薬「レムデシビル」を1日1回投与する計画です。
この薬が誰に投与されるか、患者も医師も分からないようにして、投与から2週間後に、対症療法と偽の薬の投与を受けた患者と比較し、薬の効果を判定します。
臨床試験はアメリカと韓国、シンガポールの医療機関と共同で合わせておよそ440人の患者を対象に行われる予定で、国立国際医療研究センターでは早ければ3月中にも投与を始めたいとしています。
新型コロナウイルスに対する特効薬はなく、現在、エイズの発症を抑える薬やインフルエンザの治療薬、それにぜんそくの治療薬などについて、実際の患者で効果や安全性の検証が進められています。
大曲医師は「標準的な治療を確立するために1日でも早く、レムデシビルの検証を進めたい」と話しています。
ぜんそく薬「オルベスコ」に効果の可能性 新型コロナウイルス(3/22)
2020年3月22日

新型コロナウイルスに対して、ぜんそくの治療薬が効果がある可能性を突き止めた研究者がNHKのインタビューに応じ、「安全だと分かっている薬を使えば、開発にかかる時間の短縮になるうえ、薬の適用を変えるだけなので医師も使いやすい」と述べ、既存の薬の効果を確かめる意義を強調しました。
新型コロナウイルスに対するワクチンの開発には1年以上かかるとされ、特効薬もないことから、世界各地で既存の薬が使えるかどうか調べる取り組みが行われています。
このうち、日本国内からは、免疫の働きを抑えるステロイドを吸入するタイプのぜんそく治療薬、「オルベスコ」、一般名「シクレソニド」という薬を患者に投与したあと、症状が改善したケースが報告されていて、この薬に効果がある可能性を突き止めた国立感染症研究所の松山州徳室長がNHKのインタビューに応じました。
松山室長によりますと、国立感染症研究所では、コロナウイルスの一種による感染症で、中東などで広がったMERSに効く薬を探そうと、2年前からおよそ1200種類の薬の候補物質をウイルスに感染させた細胞に投与する実験を進め、「オルベスコ」が効果がある可能性を見いだしていたということです。
同様の実験を新型コロナウイルスに感染させた細胞でも行ったところ、細胞の中のウイルスは、100分の1程度にまで減ったということで、ウイルスの増殖を抑えることを実験で確認できたとしています。
松山室長は、ウイルスの増殖を抑えると同時に炎症を抑える効果があると見ています。
松山室長は「MERSはいまだに中東で感染が続いているうえ、コロナウイルスの病気はほかにもあるので研究を続けていた。薬の開発や安全性の確認には時間がかかるため、新たに開発すると間に合わない。人に投与しても安全だと分かっている薬は、薬の適用を変えるだけなので医師も使いやすい」と述べ、新たな感染症に対して既存の薬の効果を確かめる意義を強調しました。
一方、国の研究班ではオルベスコを含めた複数の既存の薬が、新型コロナウイルスに効果があるかどうか、患者に投与した際のデータを集めて分析することにしています。
研究班の班長で愛知医科大学の森島恒雄客員教授は「薬を使った治療法が決まってくれば、肺炎の重症化を防ぎ、集中治療、医療の崩壊を防ぐことができる。3月終わりから4月初めごろにはある程度、薬のデータがそろってきて、きちんと評価できると考えている」と話しています。
ぜんそく薬投与した医師は期待
神奈川県松田町にある神奈川県立足柄上病院では、これまでに新型コロナウイルスに感染した患者、10人に対して治療を行ってきました。
このうち、2月クルーズ船「ダイヤモンド・プリンセス」で感染した患者3人は、いずれも高齢で、搬送されてきた当初から肺炎になっているなど症状が重く、ベッドから起き上がるのもやっとという状態で、中国などで投与の報告があったエイズの発症を抑える薬を試しても症状は改善しなかったということです。
こうした中で、病院で患者を診ていた総合診療科の岩渕敬介医長は、2月中旬に開かれた新型コロナウイルスへの治療を検討する会議に出席し、国立感染症研究所からぜんそく薬の「オルベスコ」が効く可能性があるという報告を聞き、これまでに長年使われている薬で副作用が少ないことから患者の同意を得たうえで投与することを決めました。
投与したあとはいずれの患者も2日ほどで肺炎などの症状が改善し、中には日課の体操ができるほどに体調が戻る人もいたということです。
岩渕医長は「当初は、とんでもない感染症を診ているのではないかと感じ、必死に診療していた。本当にこの薬が効いたのか分からないが、つらい闘いだったので救われたと思った。人工呼吸器などを必要とする患者は普通の病院ではなかなか診ることができないので、こうした薬を早期に使って重症化が防げるのであれば、非常に意味があると思う」と話しています。
新型コロナウイルス 「アビガン」の臨床研究 日本でも(3/22)
2020年3月22日
新型コロナウイルスの治療に使えるのではないかと期待されている薬の1つ、「アビガン」は、中国で治療効果がみられたとされ、日本国内でも患者に投与する臨床研究が始まっています。
「アビガン」、一般名「ファビピラビル」は、インフルエンザの治療薬として、6年前、日本の製薬会社が開発しましたが、動物実験で胎児への副作用が報告されたことから、妊娠中の女性には投与できず、ほかの薬が効かない感染症が発生し、国が使用すると判断した場合に限って投与されることになっています。
中国では、新型コロナウイルスに感染した患者に投与する臨床研究を行った結果、肺炎の症状などを改善させる効果が認められたと報告され、中国政府は、アビガンを新型コロナウイルスの治療薬の1つとして、治療指針に正式に採用する方針を明らかにしました。
日本でも、国が200万人分を備蓄していますが、3月からはこの備蓄分の薬を使って新型コロナウイルスに対して効果があるかどうか調べる臨床研究が、愛知県の藤田医科大学病院などで始まりました。
臨床研究では、ウイルスに感染し、軽症や無症状のおよそ80人を対象に、薬の投与によってウイルスの量が減るかどうか比較することにしていて、藤田医科大学病院では研究に参加する全国の医療機関とテレビ会議を行って、患者への投与の計画や、薬や採取キットの準備状況などを確認していました。
藤田医科大学病院の土井洋平教授は、「新型コロナウイルスに対する有効な治療法を確立することが最優先の課題になっている。アビガンが有望な薬であるのかどうかを研究ではっきり示したい」と話しています。
新型コロナウイルス 治療薬の開発 国内外の状況は?(3/18)
2020年3月18日

新型コロナウイルスには、今のところ、特効薬はありませんが、すでに別の感染症などに使われている薬が使える可能性があるとして、国内外で実際に患者への投与が行われ、効果や安全性の検証が進められています。
別の感染症に使われている薬で新型コロナウイルスに感染した患者への投与が行われているのはエイズの発症を抑える「カレトラ」、インフルエンザの治療薬「アビガン」、エボラ出血熱の治療薬として開発が進められた「レムデシビル」、抗マラリア薬の「リン酸クロロキン」です。
抗HIV薬「カレトラ」
このうち、エイズの発症を抑える抗ウイルス薬「カレトラ」は、中国やタイ、それに国内の複数の患者にすでに投与されていて、日本感染症学会は2月、おおむね50歳以上で、肺炎になって血液中の酸素が不足し酸素吸入が必要な状態の患者に対しては、投与を検討するという考え方を示しています。
抗インフルエンザ薬「アビガン」
また、日本の製薬会社が開発したインフルエンザの治療薬「アビガン」は、国内でも愛知県の藤田医科大学病院などで患者に投与する臨床研究が始まっています。アビガンについて、中国政府は臨床研究で治療効果が認められたとして、政府の診療指針に正式に採用する方針を明らかにしています。
エボラで開発の「レムデシビル」
アメリカでは、エボラ出血熱の治療薬として開発が進められた抗ウイルス薬「レムデシビル」が患者に対して投与されたほか、日本国内でも臨床研究が始まる予定です。
抗マラリア薬「リン酸クロロキン」
さらに2月、中国政府は、抗マラリア薬の「リン酸クロロキン」で治療効果があったと示し、国内でも類似の薬を患者に投与したケースが報告されています。このほか、感染症の薬以外でも患者に投与して効果を確かめようとしているものがあります。
ぜんそく治療薬「オルベスコ」
吸引するタイプのぜんそくの治療薬「オルベスコ」一般名「シクレソニド」は、国立感染症研究所が多くの薬の候補を調べ、新型コロナウイルスに効く可能性があることを示しました。
実際に国内で呼吸状態が悪くなった患者に投与したあと、数日のうちに症状の改善が見られたという報告が複数あり、日本感染症学会が全国の医療機関から報告を集めて効果の検証を進めています。
回復患者の「血しょう」も治療に
さらに、中国では、新型コロナウイルスに感染し、治癒した患者から提供を受けた血しょうを使った治療で、症状が改善したとする報告も出されています。
薬の使用までには
薬を全国の医療機関で広く使用できるようにするためには、患者に投与して安全性や効果を確かめる臨床試験を行い、医薬品医療機器総合機構での審査を経て厚生労働大臣の承認を受ける必要があります。
すでに使われている薬を別の病気の治療にも使う場合、薬を最初の段階から開発するのに比べて、開発期間を短縮できますが、それでも承認を得るには一定の時間がかかるため、新型コロナウイルスの患者に対しては、患者の同意を得て医療機関内で審査したうえで薬を使用する「適応外使用」という方法で投与が行われています。
急性すい炎の治療薬「ナファモスタット」新型コロナに効果か(3/18)
2020年3月18日

新型コロナウイルスに感染した患者の治療に、急性すい炎などの薬が使える可能性があると、東京大学のグループが発表しました。早ければ、3月中にも実際に患者への投与を始め、効果の検証を行うとしています。

これは、東京大学医科学研究所の井上純一郎教授らが記者会見で明らかにしました。
井上教授のグループは、新型コロナウイルスのたんぱく質を使った細胞での実験で、国内で急性すい炎などの治療に使われる「ナファモスタット」という薬がウイルスが細胞に侵入するのを妨げ、増殖するのを抑える効果が期待できることを突き止めたということです。
この薬は、およそ30年にわたって急性すい炎などに対して使用されていて、どう作用するかも分かっているということで、早ければ3月中にも国立国際医療研究センターなどと共同で実際に薬を患者に投与して、安全性や効果を確かめる臨床研究を始めるとしています。
新型コロナウイルスに対して、国内ではエイズの発症を抑える薬やインフルエンザの治療薬などを実際に患者に投与して効果や安全性の検証が進められています。
研究グループは、「ナファモスタット」が中東などで感染が広がったコロナウイルスの一種、MERSに対して効果が期待できるとする研究を4年前に出しており、井上教授は「効果が期待されているほかの薬との併用も考えながら、早く臨床研究を始めたい」と話しています。
中国政府 「アビガン」に治療効果 診療指針に正式採用へ(3/18)
2020年3月18日

中国政府は、日本の製薬会社が開発したインフルエンザ治療薬の「アビガン」に、新型コロナウイルスによる肺炎の症状などを改善させる効果が認められたとして、重症化を防ぐ治療薬の1つとして、政府の診療指針に正式に採用する方針を明らかにしました。
中国の科学技術省生物センターの張新民主任は、17日に北京で開いた記者会見で、新型コロナウイルスをめぐり国内の2つの医療機関が行った臨床研究の結果、日本の製薬会社が開発したインフルエンザ治療薬「アビガン」、一般名「ファビピラビル」に、治療効果が認められたことを明らかにしました。
このうち、湖北省武漢の医療機関が行った患者240人を対象にした臨床研究では、「アビガン」を投与した場合は熱が下がるまでの平均日数が2.5日で、投与しなかった場合の4.2日よりも短かったとということです。
また、せきの症状が緩和されるのも「アビガン」を投与した場合は平均で4.57日で、投与しなかった場合の5.98日よりも短く、明らかな副作用も見られなかったと指摘しています。
一方、広東省深センの医療機関が行った患者80人を対象にした臨床研究では、「アビガン」を投与した患者ではウイルス検査の結果が陽性から陰性になる日数の中央値が4日だったのに対し、投与しなかった患者では11日だったということです。
また、エックス線の画像で肺炎の症状に改善が認められた患者の割合は、「アビガン」を投与した場合91%と、投与しなかった場合の62%より高かったとしています。
張主任は、臨床研究で効果が確認された抗マラリア薬の「リン酸クロロキン」とともに、「アビガン」についても患者が重症化するのを防ぐ治療薬の1つとして政府の診療指針に正式に採用する方針を明らかにしました。
一方、すでに重症化した患者については治癒した患者から提供を受けた血しょうなどが効果的だとしていて、症状にあわせて使い分けていく姿勢を示しています。
中国政府 臨床試験で「アビガン」に治療効果 治療薬として使用へ(3/17)
2020年3月17日
中国政府は、新型コロナウイルスによる患者を対象に行った臨床研究の結果を公表し、日本の製薬会社が開発したインフルエンザ治療薬「アビガン」に治療効果が認められ、明らかな副作用もみられなかったとして、医療現場で治療薬の1つとして使用を勧めていく方針を明らかにしました。
中国では、16日新たに21人の新型コロナウイルスの感染者が確認され、感染者は合わせて8万人を超え、死者も3226人となりました。
こうした中、北京で17日開かれた記者会見で、科学技術省生物センターの張新民主任は、国内の2つの医療機関が行った臨床研究の結果、日本の製薬会社が開発したインフルエンザ治療薬「アビガン」、一般名「ファビピラビル」に、新型コロナウイルスによる肺炎などへの治療効果が認められ、明らかな副作用もみられなかったと述べました。
臨床研究は、湖北省武漢と広東省深※センの医療機関が、それぞれ240人と80人の患者を対象に行い、このうち深※センでは「アビガン」を投与しなかった場合は、ウイルス検査の結果が陽性から陰性になる日数の中央値が11日だったのに対し、投与した患者では4日だったということです。
また、エックス線の画像で肺炎の症状の改善が認められた患者の割合は、「アビガン」を投与した場合は91%と、投与しなかった場合の62%より高かったとしています。
張主任は「安全性が高く、効果も明らかで正式に推薦する」と述べ、治療薬の1つとして医療現場で使用を勧めていく方針を明らかにしました。
「アビガン」の一般名である「ファビピラビル」をめぐっては、日本の会社とライセンス契約を結んでいる中国の製薬企業が2月、中国政府の許可をとって量産が可能な体制をとっています。
※セン=「土」へんに「川」